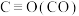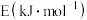1 . 下列提供了有关物质的熔点,根据表中的数据,下列判断错误 的是
| 物质 | NaCl | AlF3 | AlCl3 | CO2 | SiO2 |
| 熔点/℃ | 801 | 1291 | 190(2.5×105Pa) | -56.5 | 1723 |
| A.CO2晶体是分子晶体,SiO2晶体是共价晶体 |
| B.CO2、SiO2、AlCl3晶体中都含有极性共价键 |
| C.AlF3晶体是离子晶体,AlCl3晶体是分子晶体 |
| D.AlF3晶体和NaCl晶体熔化时克服的作用力都是范德华力 |
您最近一年使用:0次
名校
解题方法
2 . 请回答下列问题:
(1)根据分子中所含官能团可预测有机化合物的性质。
①分子中所有碳原子位于同一条直线上的是___________ (填字母)。
a.丙烷 b.丙烯 c.丙炔
②能发生加成反应的有机物是___________ (填字母)。
a.CH3CH2Br b.CH3CH2OH c.葡萄糖
(2)扁桃酸(C6H5CHOHCOOH)是一种重要的化工原料,扁桃酸分子中有___________ 种不同化学环境的氢。
(3)化合物C是一种医药中间体,可通过下列方法合成:___________ 和___________ 。
②B的结构简式为___________ 。
(1)根据分子中所含官能团可预测有机化合物的性质。
①分子中所有碳原子位于同一条直线上的是
a.丙烷 b.丙烯 c.丙炔
②能发生加成反应的有机物是
a.CH3CH2Br b.CH3CH2OH c.葡萄糖
(2)扁桃酸(C6H5CHOHCOOH)是一种重要的化工原料,扁桃酸分子中有
(3)化合物C是一种医药中间体,可通过下列方法合成:

②B的结构简式为
您最近一年使用:0次
名校
3 . 能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。请回答下列问题。
(1)工业合成氨反应: 是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知
是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知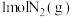 完全反应生成
完全反应生成 可放出
可放出 热量。如果将
热量。如果将 和足量
和足量 混合,使其充分反应,放出的热量
混合,使其充分反应,放出的热量_______ (填“大于”、“小于”或“等于”)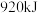 。
。
(2)实验室模拟工业合成氨时,在容积为 的密闭容器内,反应经过
的密闭容器内,反应经过 后,生成
后,生成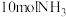 ,用
,用 表示的化学反应速率为
表示的化学反应速率为_______ 。
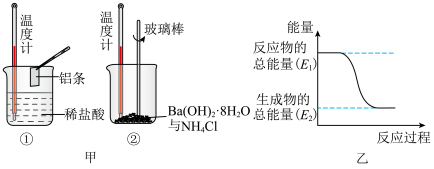
(3)某实验小组同学进行如图甲所示实验,以检验化学反应中的能量变化。请根据你掌握的反应原理判断,②中的温度_______ (填“升高”或“降低”),反应过程_______ (填“①”或“②”)的能量变化可用图乙表示。_______ (填字母)。
A.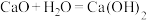
B.
C.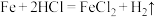
(5)如图为原电池装置示意图。 为
为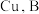 为石墨,电解质为
为石墨,电解质为 溶液,工作时的总反应为
溶液,工作时的总反应为 。
。_______ 极(填“正”或“负”)。
②该电池在工作时,溶液中 向
向_______ (填“A”或“B”)移动, 电极的质量将
电极的质量将_______ (填“增加”、“减小”或“不变”)。
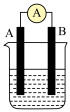
(6)化学反应均涉及相应的能量变化,为探究这些能量变化,某同学设计了如图两个实验,已知两个实验除了是否有导线连接两个金属棒外,其余均相同。_______ 。
②有关反应一段时间后的实验现象,下列说法正确的是_______ (填字母)。
A.图1中温度计的示数高于图2的示数
B.图1和图2中温度计的示数相等,且均高于室温
C.图1和图2的气泡均产生于锌棒表面
D.图2中产生气体的速率比1慢
(1)工业合成氨反应:
 是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知
是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知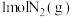 完全反应生成
完全反应生成 可放出
可放出 热量。如果将
热量。如果将 和足量
和足量 混合,使其充分反应,放出的热量
混合,使其充分反应,放出的热量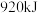 。
。(2)实验室模拟工业合成氨时,在容积为
 的密闭容器内,反应经过
的密闭容器内,反应经过 后,生成
后,生成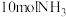 ,用
,用 表示的化学反应速率为
表示的化学反应速率为(3)某实验小组同学进行如图甲所示实验,以检验化学反应中的能量变化。请根据你掌握的反应原理判断,②中的温度
A.
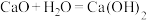
B.

C.
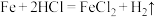
(5)如图为原电池装置示意图。
 为
为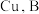 为石墨,电解质为
为石墨,电解质为 溶液,工作时的总反应为
溶液,工作时的总反应为 。
。
②该电池在工作时,溶液中
 向
向 电极的质量将
电极的质量将(6)化学反应均涉及相应的能量变化,为探究这些能量变化,某同学设计了如图两个实验,已知两个实验除了是否有导线连接两个金属棒外,其余均相同。
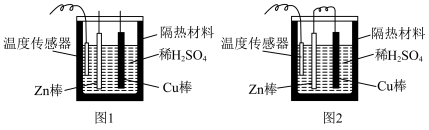
②有关反应一段时间后的实验现象,下列说法正确的是
A.图1中温度计的示数高于图2的示数
B.图1和图2中温度计的示数相等,且均高于室温
C.图1和图2的气泡均产生于锌棒表面
D.图2中产生气体的速率比1慢
您最近一年使用:0次
名校
4 . 回答下列问题。
(1)已知反应 中相关的化学键键能数据如表:
中相关的化学键键能数据如表:
若有 生成,该反应
生成,该反应_______ (填“吸收”或“放出”)_______  能量。
能量。
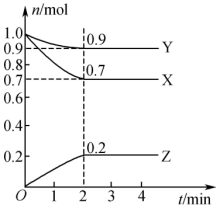
某温度时,在2L的密闭容器中,X、Y、Z(均为气体)的物质的量随时间的变化曲线如图所示。请回答下列问题:_______ 。
(3)反应从开始至2min,用Z的浓度变化表示的平均反应速率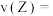
_______ 。
(4)2min后反应达到平衡,容器内混合气体的平均相对分子质量比起始时_______ (填“增大”“减小”或“不变”下同);混合气体的密度_______ 。
(5)将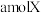 与
与 的混合气体通入
的混合气体通入 的密闭容器中并发生上述反应,反应到某时刻各物质的物质的量恰好满足:
的密闭容器中并发生上述反应,反应到某时刻各物质的物质的量恰好满足: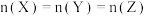 ,则原混合气体中
,则原混合气体中
_______ 。
(6)下列措施能加快反应速率的是_______ (填序号,下同)。
A.恒压时充入 B.恒容时充入He
B.恒容时充入He
C.恒容时充入X D.及时分离出
E.升高温度 F.选择高效的催化剂
(7)下列说法正确的是_______ 。
A.升高温度改变化学反应的限度
B.已知正反应是吸热反应,升高温度正反应速率加快,逆反应速率减慢
C.化学反应的限度与时间长短无关
D.化学反应的限度是不可能改变的
E.增大Y的浓度,正反应速率加快,逆反应速率减慢
(1)已知反应
 中相关的化学键键能数据如表:
中相关的化学键键能数据如表:化学键 |
|
|
|
|
|
| 436 | 343 | 1076 | 465 | 413 |
 生成,该反应
生成,该反应 能量。
能量。某温度时,在2L的密闭容器中,X、Y、Z(均为气体)的物质的量随时间的变化曲线如图所示。请回答下列问题:
(3)反应从开始至2min,用Z的浓度变化表示的平均反应速率
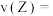
(4)2min后反应达到平衡,容器内混合气体的平均相对分子质量比起始时
(5)将
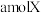 与
与 的混合气体通入
的混合气体通入 的密闭容器中并发生上述反应,反应到某时刻各物质的物质的量恰好满足:
的密闭容器中并发生上述反应,反应到某时刻各物质的物质的量恰好满足: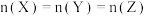 ,则原混合气体中
,则原混合气体中
(6)下列措施能加快反应速率的是
A.恒压时充入
 B.恒容时充入He
B.恒容时充入HeC.恒容时充入X D.及时分离出

E.升高温度 F.选择高效的催化剂
(7)下列说法正确的是
A.升高温度改变化学反应的限度
B.已知正反应是吸热反应,升高温度正反应速率加快,逆反应速率减慢
C.化学反应的限度与时间长短无关
D.化学反应的限度是不可能改变的
E.增大Y的浓度,正反应速率加快,逆反应速率减慢
您最近一年使用:0次
5 . 下列各组物质均由一种干燥气体和一种液体组成,其中可以进行喷泉实验,且液体几乎充满烧瓶的组合是
A. ,稀盐酸 ,稀盐酸 | B. ,稀硫酸 ,稀硫酸 | C. ,饱和食盐水 ,饱和食盐水 | D. ,水 ,水 |
您最近一年使用:0次
名校
解题方法
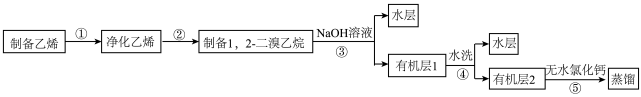
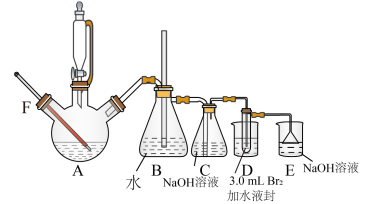
6 . 汽车用汽油的抗爆剂约含17%的1,2−二溴乙烷,某学习小组用如图所示装置制备少量1,2−二溴乙烷。(1,2−二溴乙烷的沸点为131℃,熔点为9.3℃,摩尔质量为188g/mol。)
②待温度升到150℃左右时,连接C与D,并迅速将A内反应温度升温至160~180℃,从滴液漏斗中慢慢滴加乙醇和浓硫酸混合液。
③装置D试管中装有6.0mL10mol/LBr2的CCl4溶液,待Br2的CCl4溶液褪色后,经洗涤、干燥、蒸馏得到1,2-二溴乙烷7.896g。
(1)仪器A的名称___________ ;反应一段时间后C溶液碱性___________ (填“增强”、“减弱”或“不变”)。
(2)滴液漏斗中导管的作用是___________ 。
(3)反应过程中应用冷水冷却装置D,因为乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是___________ 。
(4)流程图步骤③中加入1%的氢氧化钠水溶液的化学方程式是:___________ 。
(5)下列操作中,不会导致产物产率降低的是___________。
②待温度升到150℃左右时,连接C与D,并迅速将A内反应温度升温至160~180℃,从滴液漏斗中慢慢滴加乙醇和浓硫酸混合液。
③装置D试管中装有6.0mL10mol/LBr2的CCl4溶液,待Br2的CCl4溶液褪色后,经洗涤、干燥、蒸馏得到1,2-二溴乙烷7.896g。
(1)仪器A的名称
(2)滴液漏斗中导管的作用是
(3)反应过程中应用冷水冷却装置D,因为乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是
(4)流程图步骤③中加入1%的氢氧化钠水溶液的化学方程式是:
(5)下列操作中,不会导致产物产率降低的是___________。
| A.装置D中试管内物质换成液溴 |
| B.装置E中的NaOH溶液用水代替 |
| C.去掉装置D烧杯中的冷水 |
| D.去掉装置C |
您最近一年使用:0次
名校
解题方法
7 . 根据有机化学基础,请回答下列问题:
(1)如图是含C、H、O三种元素的某有机分子模型(图中球与球之间的连线代表单键、双键等化学键),其含氧官能团的名称为___________ 。 的名称(系统命名)为
的名称(系统命名)为___________ ,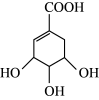 的分子式为
的分子式为___________ 。
(3)分子式为C5H10,且属于烯烃的同分异构体有___________ 种(考虑顺反异构)。
(4)对有机化合物X的结构进行探究。
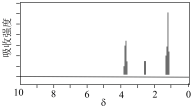
有机化合物X分子式为C2H6O,其核磁共振氢谱如图所示,共有3组峰且峰面积之比为3:2:1。则X的结构简式为___________ 。___________ 。反应类型是___________ 。
(1)如图是含C、H、O三种元素的某有机分子模型(图中球与球之间的连线代表单键、双键等化学键),其含氧官能团的名称为
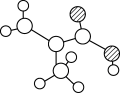
 的名称(系统命名)为
的名称(系统命名)为 的分子式为
的分子式为(3)分子式为C5H10,且属于烯烃的同分异构体有
(4)对有机化合物X的结构进行探究。
有机化合物X分子式为C2H6O,其核磁共振氢谱如图所示,共有3组峰且峰面积之比为3:2:1。则X的结构简式为
您最近一年使用:0次
名校
解题方法
8 . 现有:乙醇、乙醛、乙酸、甲酸、甲酸甲酯、苯、四氯化碳七种失去标签的试剂,只用一种试剂进行鉴别(可以加热),这种试剂是
| A.溴水 | B.新制的Cu(OH)2悬浊液 |
| C.酸性高锰酸钾溶液 | D.FeCl3溶液 |
您最近一年使用:0次
名校
解题方法
9 . 某有机物的结构简式如图所示。下列关于该有机物的说法正确的是
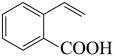
| A.1mol该有机物最多与4molH2反应生成C9H16O2 |
| B.该有机物不能使酸性高锰酸钾溶液褪色 |
| C.该有机物能发生酯化、加成、氧化、水解等反应 |
| D.与该有机物具有相同官能团的同分异构体有2种 |
您最近一年使用:0次
10 . 空气湿度增大,水汽凝结就易形成雾,灰尘、硫酸、硝酸、有机碳氢化合物等颗粒物的浓度增大就易形成霾。下列说法不正确的是
| A.防雾霾口罩的原理与过滤类似,防雾霾效果好的口罩往往呼吸阻力较大 |
| B.PM2.5是直径小于或等于2.5微米的污染物颗粒,属于胶体粒子的直径范围 |
| C.汽车车灯在雾霾天照出“通路”的现象属于丁达尔效应 |
| D.可通过在燃煤烟囱上加装高压静电装置除去煤灰中的固体颗粒物 |
您最近一年使用:0次