名校
1 . 有机氟化学在材料科学、催化化学以及生物化学等领域引起了越来越多的重视。一种以Ni的配合物Ni(IMes)L催化氟苯的碳—氟键芳基化反应制备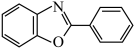 的机理如图所示。下列说法正确的是
的机理如图所示。下列说法正确的是
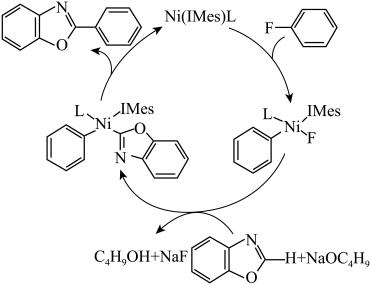
| A.该总反应原子利用率为100% |
| B.该历程涉及C-H键的断裂和形成 |
| C.该反应过程中涉及四种中间产物 |
D.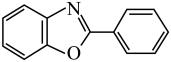 中苯环上的一氯代物7种 中苯环上的一氯代物7种 |
您最近一年使用:0次
昨日更新
|
124次组卷
|
2卷引用:2024届河南省信阳市高三下学期高考考前押题理科综合试卷-高中化学
名校
2 . 在体积为1L的恒温密闭容器中,充入1mol CO和4mol  ,一定条件下发生反应:
,一定条件下发生反应: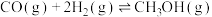
 ,测得CO和
,测得CO和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
(1)0~3 min,平均速率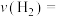
______ 。
(2)①若保持容器体积不变.向容器中充入Ne,则该反应达到平衡的时间t______ 8min(填“>”“<”或“=”)。
②若调节容器的体积为2L,则该反应中CO和 浓度相等的时间t
浓度相等的时间t______ 3min(填“>”“<”或“=”)。
(3)第3min时,正、逆反应速率的大小关系为
______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(4)能说明上述反应达到平衡状态的是______(填字母)。
(5)平衡时 的转化率为
的转化率为______ 。
(6)反应达到平衡时,体系内压强与开始时的压强之比为______ 。
(7)反应达到平衡后,若降低反应的温度,则该反应的逆反应速率将______ (填“加快”“减慢”或“不变”)。
 ,一定条件下发生反应:
,一定条件下发生反应: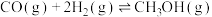
 ,测得CO和
,测得CO和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。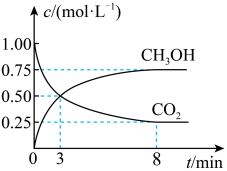
(1)0~3 min,平均速率
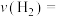
(2)①若保持容器体积不变.向容器中充入Ne,则该反应达到平衡的时间t
②若调节容器的体积为2L,则该反应中CO和
 浓度相等的时间t
浓度相等的时间t(3)第3min时,正、逆反应速率的大小关系为

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(4)能说明上述反应达到平衡状态的是______(填字母)。
A.反应中CO与 的物质的量浓度之比为1∶1 的物质的量浓度之比为1∶1 |
| B.混合气体中CO的浓度不再改变 |
C.单位时间内生成1 mol  ,同时生成1 mol ,同时生成1 mol  |
| D.混合气体的平均相对分子质量不随时间的变化而变化 |
(5)平衡时
 的转化率为
的转化率为(6)反应达到平衡时,体系内压强与开始时的压强之比为
(7)反应达到平衡后,若降低反应的温度,则该反应的逆反应速率将
您最近一年使用:0次
名校
解题方法
3 . FeO粉末在极稀的硝酸(过量)溶液中,发生反应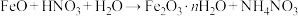 (未配平),下列说法错误的是
(未配平),下列说法错误的是
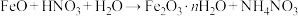 (未配平),下列说法错误的是
(未配平),下列说法错误的是| A.该反应中硝酸体现氧化性和酸性 |
| B.硝酸和硝酸铵受热均易分解 |
| C.该反应中氧化剂与还原剂的物质的量之比为1∶4 |
D.理论上,每转移8 mol电子,反应消耗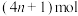  |
您最近一年使用:0次
名校
4 . 下列类比推理的结果正确的是
| A.Na能在空气中燃烧生成Na2O2,故同主族的Li在空气中燃烧生成Li2O2 |
| B.H2S与SO2能反应生成S,故NH3与NO2能在一定条件下反应生成N2 |
| C.Al(OH)3无法通过化合反应制取,推测Fe(OH)3也无法通过化合反应制取 |
| D. Na2O2与CO2反应生成Na2CO3和O2,故Na2O2与SO2反应生成Na2SO3和O2 |
您最近一年使用:0次
名校
解题方法
5 . 反应 在10L密闭容器中进行,半分钟后,D的物质的量增加了0.45mol,则下列说法正确的是
在10L密闭容器中进行,半分钟后,D的物质的量增加了0.45mol,则下列说法正确的是
 在10L密闭容器中进行,半分钟后,D的物质的量增加了0.45mol,则下列说法正确的是
在10L密闭容器中进行,半分钟后,D的物质的量增加了0.45mol,则下列说法正确的是A.半分钟时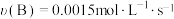 | B.半分钟内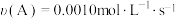 |
C.半分钟内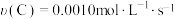 | D.半分钟内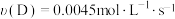 |
您最近一年使用:0次
名校
解题方法
6 . 下列离子方程式正确的是
A.次氯酸钠溶液中通入少量的二氧化硫: |
B.FeO与稀硝酸反应: |
C.澄清石灰水与过量碳酸氢钠溶液混合: |
D.硫化钠溶液中加入少量氯化铁溶液: |
您最近一年使用:0次
名校
7 . NA为阿伏加德罗常数的值。下列说法正确的是
| A.常温下,将足量的Zn投入50mL 18mol/L浓硫酸中,转移的电子数为0.9NA |
| B.12.8g Cu和0.2 mol S充分反应转移电子数为0.4NA |
| C.常温下,将2.7g铝片投入足量的浓硝酸中,铝失去的电子数为0.3NA |
| D.2.0g ND3中含有的质子数、中子数、电子数均为NA |
您最近一年使用:0次
8 . 下列说法中正确的是
| A.氧化铝常用来制造耐火坩埚,可用于加热熔融烧碱固体 |
| B.不锈钢是最常见的一种合金钢,它的合金元素主要是锌和镍 |
| C.“天问一号”探测器搭载的太阳能帆板是一种将光能转化为电能的原电池装置 |
| D.制备陶瓷和水泥的共同主要原料是黏土 |
您最近一年使用:0次
名校
9 . 学习化学反应速率和限度能够指导促进工业生产。
Ⅰ.汽车发动机工作时会引发 和
和 反应,生成
反应,生成 等污染大气,其中生成NO的能量变化如图所示,
等污染大气,其中生成NO的能量变化如图所示,___________ ;若反应生成2mol NO气体应___________ (填“释放”或“吸收”)___________ kJ能量。
Ⅱ.某研究小组用CO和 模拟工业合成甲醇,发生反应:
模拟工业合成甲醇,发生反应: 在1L的恒容密闭容器内充入1mol CO和2mol
在1L的恒容密闭容器内充入1mol CO和2mol  ,加入合适催化剂后保持某温度不变发生上述反应,并用压力计监测容器内压强的变化如下:
,加入合适催化剂后保持某温度不变发生上述反应,并用压力计监测容器内压强的变化如下:
(2)①下列说法正确的是___________ (填标号)。
a.容器内气体的密度不变,则反应达到平衡
b.容器内气体的平均相对分子质量不变,则反应达到平衡
c.若向平衡体系中充入Ar后,甲醇的生成速率降低
d.容器内CO和 物质的量之比不变,则反应达到平衡
物质的量之比不变,则反应达到平衡
e.CO的转化率不再变化,则反应达到平衡
②从反应开始到20min时, 的平均反应速率为
的平均反应速率为___________ 。
③该条件下,反应 达到平衡时CO的转化率为
达到平衡时CO的转化率为___________ 。
(3)利用反应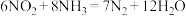 构成原电池的装置如图所示。此方法既能实现有效清除氮化物的排放,减轻环境污染,又能充分利用化学能,回答下列问题:
构成原电池的装置如图所示。此方法既能实现有效清除氮化物的排放,减轻环境污染,又能充分利用化学能,回答下列问题:___________ (填“正极”或“负极”),电极B上发生的电极反应为___________ 。
(4)用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。 和
和 ,其离子方程式为
,其离子方程式为___________ 。
②NaClO溶液的初始pH越小,NO转化率越高,其原因是___________ 。
Ⅰ.汽车发动机工作时会引发
 和
和 反应,生成
反应,生成 等污染大气,其中生成NO的能量变化如图所示,
等污染大气,其中生成NO的能量变化如图所示,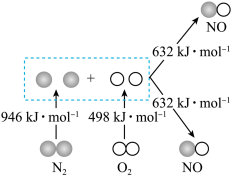
Ⅱ.某研究小组用CO和
 模拟工业合成甲醇,发生反应:
模拟工业合成甲醇,发生反应: 在1L的恒容密闭容器内充入1mol CO和2mol
在1L的恒容密闭容器内充入1mol CO和2mol  ,加入合适催化剂后保持某温度不变发生上述反应,并用压力计监测容器内压强的变化如下:
,加入合适催化剂后保持某温度不变发生上述反应,并用压力计监测容器内压强的变化如下:| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 30 |
| 压强/MPa | 25.2 | 21.6 | 18.9 | 17.4 | 16.8 | 16.8 |
(2)①下列说法正确的是
a.容器内气体的密度不变,则反应达到平衡
b.容器内气体的平均相对分子质量不变,则反应达到平衡
c.若向平衡体系中充入Ar后,甲醇的生成速率降低
d.容器内CO和
 物质的量之比不变,则反应达到平衡
物质的量之比不变,则反应达到平衡e.CO的转化率不再变化,则反应达到平衡
②从反应开始到20min时,
 的平均反应速率为
的平均反应速率为③该条件下,反应
 达到平衡时CO的转化率为
达到平衡时CO的转化率为(3)利用反应
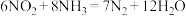 构成原电池的装置如图所示。此方法既能实现有效清除氮化物的排放,减轻环境污染,又能充分利用化学能,回答下列问题:
构成原电池的装置如图所示。此方法既能实现有效清除氮化物的排放,减轻环境污染,又能充分利用化学能,回答下列问题: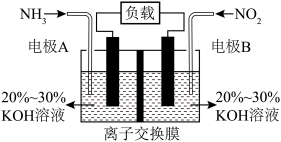
(4)用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为
 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。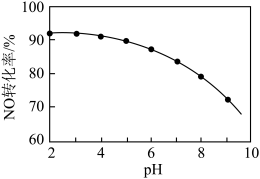
 和
和 ,其离子方程式为
,其离子方程式为②NaClO溶液的初始pH越小,NO转化率越高,其原因是
您最近一年使用:0次
名校
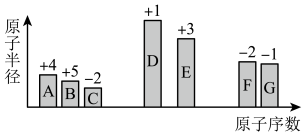
10 . 元素周期律和周期表有力地论证了事物变化中量变引起质变的规律性,以及结构决定性质的化学观念。随着原子序数的递增,七种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示,请回答下列问题:___________ 。
(2)C、D、E、G四种元素对应的简单离子半径由大到小的顺序为___________ (用元素的离子符号表示)。
(3)用电子式表示元素D与F形成化合物的过程___________ 。
(4)元素A与C形成的电子总数为22的分子的结构式为___________ 。
(5)D的最高价氧化物的水化物与E的最高价氧化物反应的离子方程式为___________ 。
(6)元素C与D按原子个数比1∶1形成的化合物所含的所有化学类型为___________ 。
(7)下列有关物质性质的推断,正确的是___________ (填标号)。
a.单质的氧化性: b.金属性:
b.金属性:
c.气态氢化物的稳定性: d.最高价氧化物的水化物酸性:
d.最高价氧化物的水化物酸性:
(2)C、D、E、G四种元素对应的简单离子半径由大到小的顺序为
(3)用电子式表示元素D与F形成化合物的过程
(4)元素A与C形成的电子总数为22的分子的结构式为
(5)D的最高价氧化物的水化物与E的最高价氧化物反应的离子方程式为
(6)元素C与D按原子个数比1∶1形成的化合物所含的所有化学类型为
(7)下列有关物质性质的推断,正确的是
a.单质的氧化性:
 b.金属性:
b.金属性:
c.气态氢化物的稳定性:
 d.最高价氧化物的水化物酸性:
d.最高价氧化物的水化物酸性:
您最近一年使用:0次



