2024·黑龙江吉林·模拟预测
1 . 我国科学家提出的聚集诱导发光机制已成为研究热点之一。一种具有聚集诱导发光性能的物质,其分子结构如图。下列说法错误的是
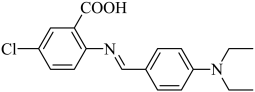
| A.分子中碳原子有sp2、sp3两种杂化轨道类型 | B.该物质既有酸性又有碱性 |
| C.该物质可发生取代反应、加成反应、氧化反应 | D.该分子不存在立体异构 |
您最近一年使用:0次
名校
解题方法
2 . 下列化学用语表达正确的是
A.次氯酸钠的电子式: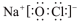 | B. 分子的空间填充模型为 分子的空间填充模型为 |
C. 分子中共价键电子云轮廓图: 分子中共价键电子云轮廓图: | D.2-丁烯的键线式: |
您最近一年使用:0次
真题
解题方法
3 . 下列离子方程式正确的是
A.用 溶液除 溶液除 气体: 气体: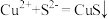 |
B. 溶液中滴加 溶液中滴加 溶液: 溶液: |
C. 溶液中通入少量 溶液中通入少量 : :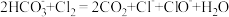 |
D.用 溶液刻蚀覆铜板制作印刷电路板: 溶液刻蚀覆铜板制作印刷电路板: |
您最近一年使用:0次
真题
解题方法
4 . 矿物资源的综合利用有多种方法,如铅锌矿(主要成分为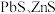 )的利用有火法和电解法等。
)的利用有火法和电解法等。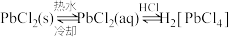 ;
;
②电解前后 总量不变;③
总量不变;③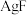 易溶于水。
易溶于水。
请回答:
(1)根据富氧煅烧(在空气流中煅烧)和通电电解(如图)的结果, 中硫元素体现的性质是
中硫元素体现的性质是_______ (选填“氧化性”、“还原性”、“酸性”、“热稳定性”之一)。产物B中有少量 ,该物质可溶于浓盐酸,
,该物质可溶于浓盐酸, 元素转化为
元素转化为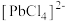 ,写出该反应的化学方程式
,写出该反应的化学方程式_______ ;从该反应液中提取 的步骤如下:加热条件下,加入
的步骤如下:加热条件下,加入_______ (填一种反应试剂),充分反应,趁热过滤,冷却结晶,得到产品。
(2)下列说法正确的是_______。
(3)D的结构为 (
( 或
或 ),设计实验先除去样品D中的硫元素,再用除去硫元素后的溶液探究X为何种元素。
),设计实验先除去样品D中的硫元素,再用除去硫元素后的溶液探究X为何种元素。
①实验方案:取D的溶液,加入足量 溶液,加热充分反应,然后
溶液,加热充分反应,然后_______ ;
②写出D(用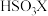 表示)的溶液与足量
表示)的溶液与足量 溶液反应的离子方程式
溶液反应的离子方程式_______ 。
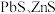 )的利用有火法和电解法等。
)的利用有火法和电解法等。
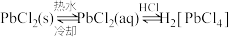 ;
;②电解前后
 总量不变;③
总量不变;③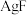 易溶于水。
易溶于水。请回答:
(1)根据富氧煅烧(在空气流中煅烧)和通电电解(如图)的结果,
 中硫元素体现的性质是
中硫元素体现的性质是 ,该物质可溶于浓盐酸,
,该物质可溶于浓盐酸, 元素转化为
元素转化为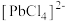 ,写出该反应的化学方程式
,写出该反应的化学方程式 的步骤如下:加热条件下,加入
的步骤如下:加热条件下,加入(2)下列说法正确的是_______。
A.电解池中发生的总反应是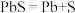 (条件省略) (条件省略) |
| B.产物B主要是铅氧化物与锌氧化物 |
C. 化合物C在水溶液中最多可中和 化合物C在水溶液中最多可中和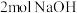 |
D. 的氧化性弱于 的氧化性弱于 |
 (
( 或
或 ),设计实验先除去样品D中的硫元素,再用除去硫元素后的溶液探究X为何种元素。
),设计实验先除去样品D中的硫元素,再用除去硫元素后的溶液探究X为何种元素。①实验方案:取D的溶液,加入足量
 溶液,加热充分反应,然后
溶液,加热充分反应,然后②写出D(用
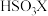 表示)的溶液与足量
表示)的溶液与足量 溶液反应的离子方程式
溶液反应的离子方程式
您最近一年使用:0次
5 . 锰的化合物用途与性质的探究,有关物质及颜色: (白色)、
(白色)、 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。回答问题:
(紫色)。回答问题:
Ⅰ.用 溶液氧化甲苯制苯甲酸,按如下流程分离苯甲酸和回收甲苯。
溶液氧化甲苯制苯甲酸,按如下流程分离苯甲酸和回收甲苯。
(1)操作Ⅰ为______ ,操作Ⅱ为______ 。
(2)无色液体A是______ ,.定性检验A的试剂是______ ,现象是____________ 。
(3)该同学推测白色固体B是苯甲酸与少量KCl的混合物,简述提纯过程____________ 。
Ⅱ.探究 在一定条件下被
在一定条件下被 或
或 氧化成的产物,实验装置如图(夹持装置略):
氧化成的产物,实验装置如图(夹持装置略): 前产生白色沉淀,在空气中缓慢变成棕黑色沉淀;通入
前产生白色沉淀,在空气中缓慢变成棕黑色沉淀;通入 后棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀。
后棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀。
实验ⅱ:物质a为40% KOH溶液,C中通入 前后与实验ⅰ现象一样。
前后与实验ⅰ现象一样。
(4)通入 前,C中沉淀由白色变为黑色的化学方程式为
前,C中沉淀由白色变为黑色的化学方程式为____________ 。
(5) 的氧化性与溶液的酸碱性无关,KClO的氧化性随碱性减弱而增强。取ⅰ中放置后的1 mL悬浊液,再加入4 mL水,溶液紫色缓慢加深,发生的反应是
的氧化性与溶液的酸碱性无关,KClO的氧化性随碱性减弱而增强。取ⅰ中放置后的1 mL悬浊液,再加入4 mL水,溶液紫色缓慢加深,发生的反应是____________ 。
(6)浓碱条件下, 可被
可被 还原为
还原为 。取ⅱ中放置后的1 mL悬浊液,再加4 mL 40% KOH溶液,溶液紫色迅速变为绿色,溶液紫色变为绿色的离子方程式为
。取ⅱ中放置后的1 mL悬浊液,再加4 mL 40% KOH溶液,溶液紫色迅速变为绿色,溶液紫色变为绿色的离子方程式为____________ 。
(7)从反应速率的角度,分析实验ⅱ未得到绿色溶液的可能原因____________ 。
 (白色)、
(白色)、 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。回答问题:
(紫色)。回答问题:Ⅰ.用
 溶液氧化甲苯制苯甲酸,按如下流程分离苯甲酸和回收甲苯。
溶液氧化甲苯制苯甲酸,按如下流程分离苯甲酸和回收甲苯。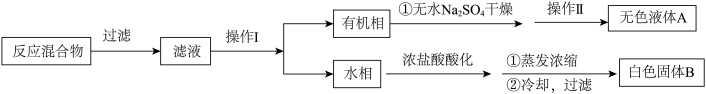
(1)操作Ⅰ为
(2)无色液体A是
(3)该同学推测白色固体B是苯甲酸与少量KCl的混合物,简述提纯过程
Ⅱ.探究
 在一定条件下被
在一定条件下被 或
或 氧化成的产物,实验装置如图(夹持装置略):
氧化成的产物,实验装置如图(夹持装置略):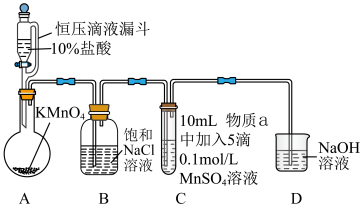
 前产生白色沉淀,在空气中缓慢变成棕黑色沉淀;通入
前产生白色沉淀,在空气中缓慢变成棕黑色沉淀;通入 后棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀。
后棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀。实验ⅱ:物质a为40% KOH溶液,C中通入
 前后与实验ⅰ现象一样。
前后与实验ⅰ现象一样。(4)通入
 前,C中沉淀由白色变为黑色的化学方程式为
前,C中沉淀由白色变为黑色的化学方程式为(5)
 的氧化性与溶液的酸碱性无关,KClO的氧化性随碱性减弱而增强。取ⅰ中放置后的1 mL悬浊液,再加入4 mL水,溶液紫色缓慢加深,发生的反应是
的氧化性与溶液的酸碱性无关,KClO的氧化性随碱性减弱而增强。取ⅰ中放置后的1 mL悬浊液,再加入4 mL水,溶液紫色缓慢加深,发生的反应是(6)浓碱条件下,
 可被
可被 还原为
还原为 。取ⅱ中放置后的1 mL悬浊液,再加4 mL 40% KOH溶液,溶液紫色迅速变为绿色,溶液紫色变为绿色的离子方程式为
。取ⅱ中放置后的1 mL悬浊液,再加4 mL 40% KOH溶液,溶液紫色迅速变为绿色,溶液紫色变为绿色的离子方程式为(7)从反应速率的角度,分析实验ⅱ未得到绿色溶液的可能原因
您最近一年使用:0次
名校
6 . 设NA为阿伏伽德罗常数的值,下列说法不正确的是
| A.含0.2molH2SO4的浓硫酸和足量的镁反应,转移电子数大于0.2NA |
| B.将1molSO2和1molO2充分反应后,其分子总数为1.5NA |
| C.7.8gNa2S与Na2O2的混合物,含离子总数为0.3NA |
D.含1molNH4Cl溶液中加入适量氨水使溶液呈中性,此时溶液中 数为NA 数为NA |
您最近一年使用:0次
真题
7 . 二氧化碳氧化乙烷制备乙烯,主要发生如下两个反应:
I.
II.
向容积为 的密闭容器中投入
的密闭容器中投入 和
和 ,不同温度下,测得
,不同温度下,测得 时(反应均未平衡)的相关数据见下表,下列说法
时(反应均未平衡)的相关数据见下表,下列说法不正确 的是
注:乙烯选择性
I.

II.

向容积为
 的密闭容器中投入
的密闭容器中投入 和
和 ,不同温度下,测得
,不同温度下,测得 时(反应均未平衡)的相关数据见下表,下列说法
时(反应均未平衡)的相关数据见下表,下列说法温度( ) ) | 400 | 500 | 600 |
乙烷转化率( ) ) | 2.2 | 9.0 | 17.8 |
乙烯选择性( ) ) | 92.6 | 80.0 | 61.8 |

A.反应活化能: |
B. 时, 时,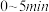 反应I的平均速率为: 反应I的平均速率为: |
C.其他条件不变,平衡后及时移除 ,可提高乙烯的产率 ,可提高乙烯的产率 |
D.其他条件不变,增大投料比 投料,平衡后可提高乙烷转化率 投料,平衡后可提高乙烷转化率 |
您最近一年使用:0次
真题
解题方法
8 . 利用 可将废水中的
可将废水中的 转化为对环境无害的物质后排放。反应原理为:
转化为对环境无害的物质后排放。反应原理为: (未配平)。下列说法正确的是
(未配平)。下列说法正确的是
 可将废水中的
可将废水中的 转化为对环境无害的物质后排放。反应原理为:
转化为对环境无害的物质后排放。反应原理为: (未配平)。下列说法正确的是
(未配平)。下列说法正确的是A.X表示 |
B.可用 替换 替换 |
C.氧化剂与还原剂物质的量之比为 |
D.若生成标准状况下的 气体 气体 ,则反应转移的电子数为 ,则反应转移的电子数为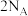 ( ( 表示阿伏加德罗常数的值) 表示阿伏加德罗常数的值) |
您最近一年使用:0次
真题
解题方法
9 . X、Y、Z、M四种主族元素,原子序数依次增大,分别位于三个不同短周期,Y与M同主族,Y与Z核电荷数相差2,Z的原子最外层电子数是内层电子数的3倍。下列说法不正确 的是
A.键角: | B.分子的极性: |
C.共价晶体熔点: | D.热稳定性: |
您最近一年使用:0次
真题
10 . 为探究化学平衡移动的影响因素,设计方案并进行实验,观察到相关现象。其中方案设计和结论都正确的是
| 选项 | 影响因素 | 方案设计 | 现象 | 结论 |
| A | 浓度 | 向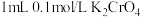 溶液中加入 溶液中加入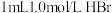 溶液 溶液 | 黄色溶液变橙色 | 增大反应物浓度,平衡向正反应方向移动 |
| B | 压强 | 向恒温恒容密闭玻璃容器中充入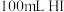 气体,分解达到平衡后再充入 气体,分解达到平衡后再充入 | 气体颜色不变 | 对于反应前后气体总体积不变的可逆反应,改变压强平衡不移动 |
| C | 温度 | 将封装有 和 和 混合气体的烧瓶浸泡在热水中 混合气体的烧瓶浸泡在热水中 | 气体颜色变深 | 升高温度,平衡向吸热反应方向移动 |
| D | 催化剂 | 向 乙酸乙酯中加入 乙酸乙酯中加入  溶液,水浴加热 溶液,水浴加热 | 上层液体逐渐减少 | 使用合适的催化剂可使平衡向正反应方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



