1 . 已知选项中的反应均在常温下进行,有关常数近似处理为: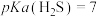 ,
,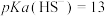 ;
;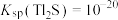 ,
,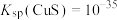 。下列说法
。下列说法不正确 的是
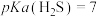 ,
,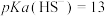 ;
;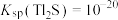 ,
,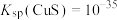 。下列说法
。下列说法A.物质的量浓度均为0.1mol/L的 与 与 的混合溶液的 的混合溶液的 约为13 约为13 |
B.0.05mol 气体通入1L 0.5mol/L的硫酸铜溶液,能观察到黑色沉淀 气体通入1L 0.5mol/L的硫酸铜溶液,能观察到黑色沉淀 |
C.0.1mol/L 溶液中 溶液中 |
D.0.1mol 固体不能溶解在1L 固体不能溶解在1L 的一元强酸(无络合性、无强氧化性)中 的一元强酸(无络合性、无强氧化性)中 |
您最近一年使用:0次
2024-04-15更新
|
325次组卷
|
3卷引用:河南省焦作市博爱县第一中学2023-2024学年高三下学期5月月考化学试题
名校
2 . 某课题组合成了一种非天然氨基酸X,合成路线如下(Ph—表示苯基):
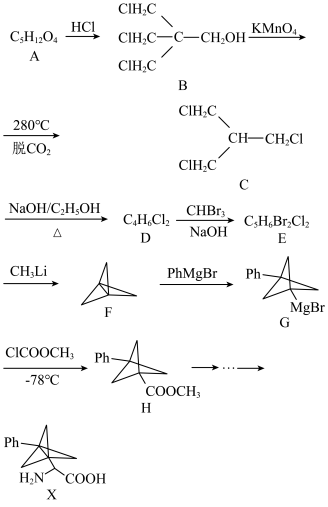
已知: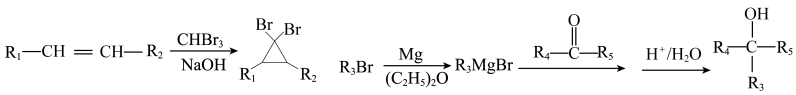
请回答:
(1)下列说法正确的是_____。
(2)化合物A的结构简式是_____ ;化合物E的结构简式是_____ 。
(3)C→D的化学方程式是_____ 。
(4)写出3种同时符合下列条件的化合物H的同分异构体的结构简式(不包括立体异构体)_____ 。
①包含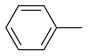 ;
;
②包含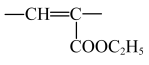 (双键两端的C不再连接H)片段;
(双键两端的C不再连接H)片段;
③除②中片段外只含有1个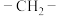
(5)以化合物F、溴苯和甲醛为原料,设计下图所示化合物的合成路线(用流程图表示,无机试剂、有机溶剂任选)_____ 。
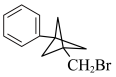 (也可表示为
(也可表示为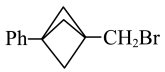 )
)

已知:

请回答:
(1)下列说法正确的是_____。
| A.化合物B的分子结构中含有亚甲基和次甲基 |
B. 谱显示化合物F中有2种不同化学环境的氢原子 谱显示化合物F中有2种不同化学环境的氢原子 |
| C.G→H的反应类型是取代反应 |
D.化合物X的分子式是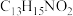 |
(3)C→D的化学方程式是
(4)写出3种同时符合下列条件的化合物H的同分异构体的结构简式(不包括立体异构体)
①包含
 ;
; ②包含
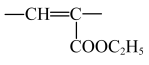 (双键两端的C不再连接H)片段;
(双键两端的C不再连接H)片段;③除②中片段外只含有1个
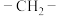
(5)以化合物F、溴苯和甲醛为原料,设计下图所示化合物的合成路线(用流程图表示,无机试剂、有机溶剂任选)
 (也可表示为
(也可表示为 )
)
您最近一年使用:0次
名校
解题方法
3 .  的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和四面体。电池充放电时,
的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和四面体。电池充放电时, 脱出或嵌入
脱出或嵌入 形成结构示意图如(b)所示。下列说法正确的是
形成结构示意图如(b)所示。下列说法正确的是
 的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和四面体。电池充放电时,
的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和四面体。电池充放电时, 脱出或嵌入
脱出或嵌入 形成结构示意图如(b)所示。下列说法正确的是
形成结构示意图如(b)所示。下列说法正确的是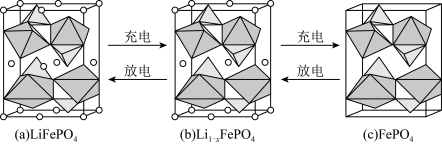
A.每个 晶胞中 晶胞中 个数为1-x 个数为1-x |
| B.图(b)中x=0.1875 |
C.图(b)中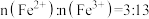 |
D.当 转化为 转化为 时,每转移电子 时,每转移电子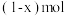 ,嵌入 ,嵌入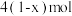  |
您最近一年使用:0次
2023-03-24更新
|
1173次组卷
|
3卷引用:河南省焦作市博爱县第一中学2022-2023学年高二下学期5月月考化学试题
4 . 常温下,用NaOH调节不同浓度的二元酸(H2CO3)的酸碱性,在其pH为10时溶液中pHCO 与pH2CO3或pCO
与pH2CO3或pCO 的关系如图所示[pX=-lgc(X)]。下列说法错误的是
的关系如图所示[pX=-lgc(X)]。下列说法错误的是
 与pH2CO3或pCO
与pH2CO3或pCO 的关系如图所示[pX=-lgc(X)]。下列说法错误的是
的关系如图所示[pX=-lgc(X)]。下列说法错误的是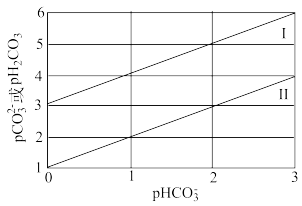
A.II代表pCO |
B.NaHCO3溶液中:c(Na+)<c(HCO )+2c(CO )+2c(CO ) ) |
| C.相同浓度的Na2CO3溶液和NaHCO3溶液的pH:前者大于后者 |
| D.碳酸的第一步电离常数为1×10-7 |
您最近一年使用:0次
2023-02-05更新
|
510次组卷
|
3卷引用:河南省焦作市普通高中2022-2023学年高二下学期开学诊断考试化学试题
名校
解题方法
5 . 25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是
| A.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| B.0.1mol/LNa2CO3溶液与0.1mol/LNaHCO3溶液等体积混合:2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3) |
| C.0.1mol/LNH4Cl溶液与0.1mol/L氨水等体积混合(pH>7):c(NH3·H2O)>c(NH4+)>c(Cl-)>c(OH-) |
| D.0.1mol/LNa2C2O4溶液与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+) |
您最近一年使用:0次
2018-02-06更新
|
1093次组卷
|
4卷引用:河南省焦作市博爱县英才学校2020-2021学年高二上学期11月月考化学试题
真题
名校
6 . 常温下将NaOH溶液滴加到己二酸(H2X)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是
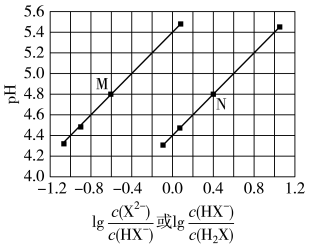

| A.Ka2(H2X)的数量级为10–6 |
B.曲线N表示pH与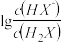 的变化关系 的变化关系 |
| C.NaHX溶液中c(H+)>c(OH-) |
| D.当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(OH-)=c(H+) |
您最近一年使用:0次
2017-08-09更新
|
17090次组卷
|
70卷引用:河南省焦作市博爱县英才学校2020-2021学年高二上学期11月月考化学试题
河南省焦作市博爱县英才学校2020-2021学年高二上学期11月月考化学试题河北省安平中学2016-2017学年高二下学期期末考试化学试题2017年全国普通高等学校招生统一考试理综化学(新课标Ⅰ卷精编版)黑龙江省哈尔滨市第六中学2017-2018学年高二12月月考化学试题黑龙江省哈尔滨六中2017-2018学年高二12月月考化学试卷辽宁省沈阳市东北育才学校2017-2018学年高二上学期期中考试化学试题云南民族大学附属中学2017-2018学年高二下学期第一次月考化学试题(已下线)《考前20天终极攻略》6月4日 专项四 化学坐标曲线图分析(已下线)《考前20天终极攻略》-5月23日 溶液中的离子平衡(已下线)解密12 盐类的水解——备战2018年高考化学之高频考点解密2018-2019学年鲁科版高中化学选修四:第3章检测题(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第5讲 数形结合思想的应用【教学案】【全国百强校】四川省棠湖中学2019届高三上学期第三次月考理综-化学试题【全国百强校】山西省晋中市平遥县平遥中学2019届高三上学期12月月考化学试题河南省辉县市一中2018-2019学年高二上学期第二次阶段性考试化学试题【全国百强校】内蒙古自治区杭锦后旗奋斗中学2018-2019学年高二下学期期中考试化学试题安徽省阜阳市颍上二中等三校2020届高三上学期入学考试化学试题河北安平中学2020届高三上学期第二次月考化学试题天津市耀华中学2019-2020学年度高二上学学期期中考试化学试题2019年秋高三化学复习强化练习—— 电解质溶液中的曲线问题江西省上饶中学2019-2020学年高二上学期期中考试(零班、培优班)化学试题吉林省长春市田家炳实验中学2019-2020学年高二上学期期末考试化学试题辽宁省锦州市滨海实验中学2019-2020学年高三上学期期末考试化学试题备考突破2020高三化学专题强化集训——电解质溶液中的曲线问题辽宁省锦州市滨海实验中学2020届高三模拟考试理综化学试题重庆市江北中学2019-2020学年高二上学期期末模拟考试化学试题四川省泸县第四中学2020届高三下学期第一次在线月考理综化学试题(已下线)专题十二 水溶液中的离子平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训云南省大理白族自治州祥云县第一中学2020届高三下学期4月月考理综化学试题河北省沧州市盐山中学2019-2020学年高二上学期期末考试(B)化学试题(已下线)考点11 弱电解质的电离及溶液pH-2020年高考化学命题预测与模拟试题分类精编(已下线)2020年高考化学押题预测卷02(新课标Ⅲ卷)--《2020年高考押题预测卷》河北衡水中学2020届高三下学期三月份教学质量监测理科综合化学试题(已下线)广东省深圳中学2020届高三3月份教学质量监测卷理综化学试题四川省成都市第七中学2020年高中毕业班教学质量监测卷理科综合化学试题湖南省长沙市礼雅中学2020届高三下学期三月份网络教学质量监测理科综合化学试题广东省深圳中学2020年高中毕业班教学质量监测卷理科综合化学试题贵州省贵阳市第一中学2020届高三教学质量监测理科综合化学试题安徽省合肥市第一中学2019-2020学年高二上学期段二(期中)考试化学试题鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第2节 弱电解质的电离盐类的水解(已下线)第03章 物质在水溶液中的行为 (B卷能力提升卷) -2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)(已下线)易错18 电解质溶液图像-备战2021年高考化学一轮复习易错题鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 过高考 3年真题强化闯关甘肃省白银市会宁县第一中学2020-2021学年高二上学期第二次月考化学试题广东省广州市第一一三中学2020-2021学年高二上学期第二阶段考试化学(选考)试题四川省成都市龙泉中学2021届高三上学期1月月考理综化学试题江西省抚州市金溪县第一中学2020-2021学年高二上学期第二次月考化学试题(已下线)专题12 水溶液中离子平衡(攻克各种图像问题)-2021年高考化学必做热点专题(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)河北省尚义一中2020-2021学年高二下学期期中考试化学试题四川省遂宁市射洪中学2020—2021学年高二下学期第三次月考化学试题(已下线)考点25 盐类的水解-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点25 盐类的水解-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)课时44 滴定曲线、分布系数曲线的分析-2022年高考化学一轮复习小题多维练(全国通用)湖北省武汉市华中师范大学第一附属中学2020届高三3月份网络教学质量监测卷理综化学试题重庆育才中学2021-2022学年高二上学期第三次定时练习化学试题山西省太原市第五中学2021-2022学年高二上学期12月月考化学试题(已下线)考点28 盐类的水解-备战2023年高考化学一轮复习考点帮(全国通用)江西省抚州市金溪县第一中学2021-2022学年高二下学期第二次月考化学试题(已下线)专题06 水溶液中的离子平衡(练)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)专题21 电解质溶液图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题11 水溶液中的离子平衡图像(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(已下线)专题四 电解质溶液图象(讲)广东省中山大学附属中学2023-2024学年高三上学期8月阶段性检测化学试题湖南省张家界市民族中学2023-2024学年高二上学期第二次月考化学试题山西省实验中学2023-2024学年高二上学期期中考试化学试题内蒙古呼伦贝尔市海拉尔第二中学2023-2024学年高二上学期期末考试化学试题浙江省杭州市源清中学2023-2024学年高二上学期期末考试化学试题江西省宜春市宜丰中学2023-2024学年高一上学期1月期末化学试题
7 . 氯化亚铜(CuCl)是白色粉末,微溶于水,不溶于乙醇,在空气中会被迅速氧化成绿色碱式盐。从酸性电镀废液(主要含Cu2+、Fe3+)中制备氯化亚铜的工艺流程图如图:
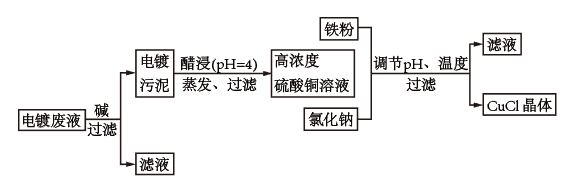
金属离子含量与混合液pH、CuCl产率与混合液pH的关系图如图。
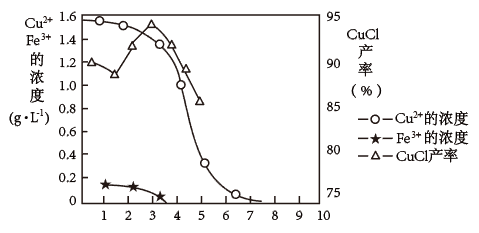
【已知:金属离子浓度为1 mol·L-1时,Fe(OH)3开始沉淀和沉淀完全的pH分别为1.4和3.0,Cu(OH)2开始沉淀和沉淀完全的pH分别为4.2和6.7】
请回答下列问题:
(1)酸浸时发生反应的离子方程式是_______ ;析出CuCl晶体时的最佳pH在_______ 左右。
(2)铁粉、氯化钠、硫酸铜在溶液中反应生成CuCl的离子反应方程式为_______ 。
(3)析出的CuCl晶体要立即用无水乙醇洗涤,在真空干燥机内于70℃干燥2 h、冷却密封包装。70℃真空干燥、密封包装的目的是_______ 。
(4)产品滤出时所得滤液的主要分成是_______ ,若想从滤液中获取FeSO4·7H2O晶体,还需要知道的是_______ 。
(5)若将铁粉换成亚硫酸钠也可得到氯化亚铜,试写出该反应的化学方程式:_______ 。为提高CuCl的产率,常在该反应体系中加入稀碱溶液,调节pH至3.5。这样做的目的是_______ 。

金属离子含量与混合液pH、CuCl产率与混合液pH的关系图如图。

【已知:金属离子浓度为1 mol·L-1时,Fe(OH)3开始沉淀和沉淀完全的pH分别为1.4和3.0,Cu(OH)2开始沉淀和沉淀完全的pH分别为4.2和6.7】
请回答下列问题:
(1)酸浸时发生反应的离子方程式是
(2)铁粉、氯化钠、硫酸铜在溶液中反应生成CuCl的离子反应方程式为
(3)析出的CuCl晶体要立即用无水乙醇洗涤,在真空干燥机内于70℃干燥2 h、冷却密封包装。70℃真空干燥、密封包装的目的是
(4)产品滤出时所得滤液的主要分成是
(5)若将铁粉换成亚硫酸钠也可得到氯化亚铜,试写出该反应的化学方程式:
您最近一年使用:0次
2016-12-09更新
|
539次组卷
|
5卷引用:2015届河南省焦作市高三上学期期中化学试卷
(已下线)2015届河南省焦作市高三上学期期中化学试卷(已下线)2014届高考化学二轮复习必做训练 化学与技术练习卷2015届湖南省五市十校高三下学期3月模拟考试理综化学试卷2015届湖南省长望浏宁四县高三一模考试化学试卷2015届江西省鹰潭市高三第二次模拟考试理综化学试卷
11-12高三上·江苏南京·阶段练习
8 . 过氧化钙可以用于改善地表水质、处理含重金属粒子废水和治理赤潮,也可用于应急供氧等。工业上生产过氧化钙的主要流程如下:
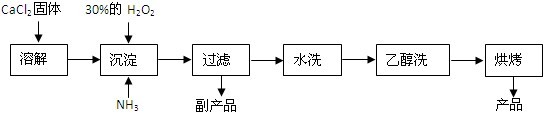
已知CaO2·8H2O呈白色,微溶于水,加热至350℃左右开始分解放出氧气。
(1)用上述方法制取CaO2·8H2O的化学方程式是______ ;
(2)检验“水洗”是否合格的方法是______ ;
(3)沉淀时常用冰水控制温度在0℃左右,其可能原因是(写出两种):①______ ;②______ 。
(4)测定产品中CaO2的含量的实验步骤是:
第一步:准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2 mol/L的H2SO4溶液,充分反应。
第二步:向上述锥形瓶中加入几滴淀粉溶液。
第三步:逐滴加入浓度为c mol·L-1的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液V mL。【已知:I2+2S2O = 2I-+S4O
= 2I-+S4O 】
】
①CaO2的质量分数为______ (用字母表示);
②某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的CaO2的质量分数可能______ (填“不受影响”、“偏低”或“偏高”),原因是______ 。

已知CaO2·8H2O呈白色,微溶于水,加热至350℃左右开始分解放出氧气。
(1)用上述方法制取CaO2·8H2O的化学方程式是
(2)检验“水洗”是否合格的方法是
(3)沉淀时常用冰水控制温度在0℃左右,其可能原因是(写出两种):①
(4)测定产品中CaO2的含量的实验步骤是:
第一步:准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2 mol/L的H2SO4溶液,充分反应。
第二步:向上述锥形瓶中加入几滴淀粉溶液。
第三步:逐滴加入浓度为c mol·L-1的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液V mL。【已知:I2+2S2O
 = 2I-+S4O
= 2I-+S4O 】
】①CaO2的质量分数为
②某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的CaO2的质量分数可能
您最近一年使用:0次



