名校
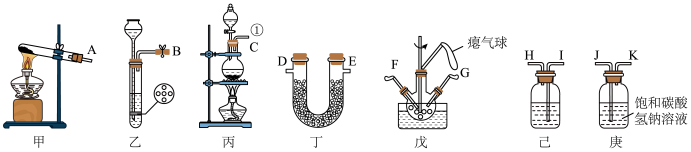
1 . 氨基甲酸铵(NH2COONH4)是一种易分解、易与水反应的白色固体、难溶于CCl4。实验室可将干燥二氧化碳和氨气通入CCl4中进行制备,反应原理为2NH3(g)+CO2(g)=NH2COONH4(s) ,反应放热,回答下列问题: _______ ,装置己中盛放的试剂为_______ ,庚中饱和碳酸氢钠溶液的作用_______ 。
(2)简述检验装置乙气密性的操作_______ 。
(3)氨气的发生装置可以选择上图中的_______ ,制取氨气的化学方程式为_______ 。
(4)预制备产品,选择上图中必要的装置,其连接顺序为_______ :
发生装置→_______→FG←_______←KJ←_______(按气流方向,用大写字母表示)。
(5)反应结束后,从反应后的混合物中分离出产品的实验操作是_______ 。
(2)简述检验装置乙气密性的操作
(3)氨气的发生装置可以选择上图中的
(4)预制备产品,选择上图中必要的装置,其连接顺序为
发生装置→_______→FG←_______←KJ←_______(按气流方向,用大写字母表示)。
(5)反应结束后,从反应后的混合物中分离出产品的实验操作是
您最近一年使用:0次
名校
2 . 科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程,其示意图如下。下列说法正确的是
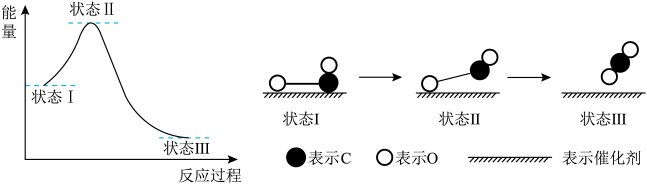
| A.由状态I→状态III,既有旧键的断裂又有新键的形成 |
| B.催化剂没有参与化学反应 |
C.CO和 分子中都含有极性共价键 分子中都含有极性共价键 |
D.CO与O反应生成 是吸热反应 是吸热反应 |
您最近一年使用:0次
名校
3 . 按要求回答下列问题:
(1)反应A+B→C(放热)分两步进行①A+B→X(吸热);②X→C(放热)。下列示意图中,能正确表示总反应过程中能量变化的是_______。
(2)下图是一氧化碳和氧在钌催化剂的表面形成化学键的过程。下列说法正确的是_______。
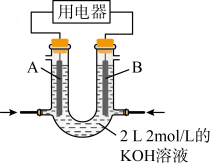
(3)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是_______ (填序号)。_______ 。
(4)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。_______ (填“A”或“B”)处电极入口通甲烷,其电极反应式为_______ 。当消耗甲烷的体积为33.6 L(标准状况)时,假设电池的能量转化率为80%,导线中转移电子的物质的量为_______ 。
(1)反应A+B→C(放热)分两步进行①A+B→X(吸热);②X→C(放热)。下列示意图中,能正确表示总反应过程中能量变化的是_______。
A.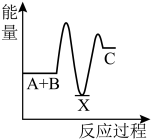 | B.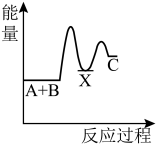 | C.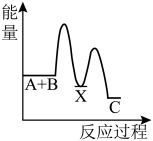 | D.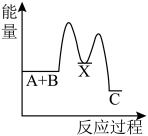 |
(2)下图是一氧化碳和氧在钌催化剂的表面形成化学键的过程。下列说法正确的是_______。
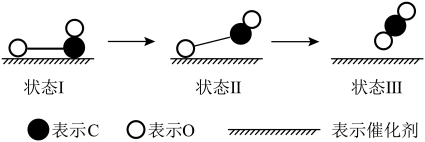
A. 和 和 均为酸性氧化物 均为酸性氧化物 | B.该过程中, 先断键成C和O 先断键成C和O |
| C.状态I到状态Ⅲ为放热过程 | D.图示表示 和 和 反应生成 反应生成 的过程 的过程 |
(3)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是
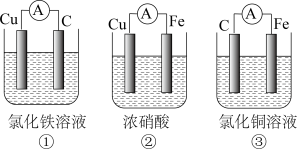
(4)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。
您最近一年使用:0次
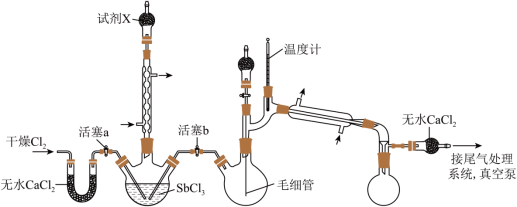
4 . 超酸是一类比纯硫酸更强的酸。某兴趣小组的同学对超酸HSbF6的制备及性质进行了探究。制备HSbF6的初始实验装置如图(毛细管连通大气,夹持、加热及搅拌装置略)。
①制备HSbF6的反应为SbCl3+Cl2 SbCl5,SbCl5+6HF =HSbF6+5HCl。
SbCl5,SbCl5+6HF =HSbF6+5HCl。
②有关物质的性质如表。
③蒸馏:利用混合溶液中各物质沸点不同进行分离提纯的方法。
回答下列问题:
(1)试剂X的作用为_______ 、_______ 。
(2)反应完成后,关闭活塞a、打开活塞b,减压转移三颈烧瓶中生成的SbCl5至双口烧瓶中。用真空泵抽气减压蒸馏前,必须关闭的活塞是_______ (填“a”或“b”);用减压蒸馏而不用常压蒸馏的主要原因是_______ 。
(3)由SbCl5制备HSbF6时,没有选择玻璃仪器,其原因为_______ (写反应的化学方程式)。
①制备HSbF6的反应为SbCl3+Cl2
 SbCl5,SbCl5+6HF =HSbF6+5HCl。
SbCl5,SbCl5+6HF =HSbF6+5HCl。②有关物质的性质如表。
| 物质 | 熔点 | 沸点 | 性质 |
| SbCl3 | 73.4℃ | 223.5℃(常压) | 极易与水反应 |
| SbCl5 | 2.8℃ | 140℃分解(常压),压强为2.9 kPa时沸点是79℃ | 极易与水反应 |
回答下列问题:
(1)试剂X的作用为
(2)反应完成后,关闭活塞a、打开活塞b,减压转移三颈烧瓶中生成的SbCl5至双口烧瓶中。用真空泵抽气减压蒸馏前,必须关闭的活塞是
(3)由SbCl5制备HSbF6时,没有选择玻璃仪器,其原因为
您最近一年使用:0次
5 . 下列关于化学物质的用途或性质的叙述正确的说法有
①浓硫酸可以干燥SO2
②燃煤中添加CaO可以减少SO2和温室气体的排放
③工业上用氢氟酸溶液腐蚀玻璃生产磨砂玻璃
④足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe2+
⑤标准状况下,O2与NO2按1∶4充满烧瓶,烧瓶倒置水中充分反应后,烧瓶内溶液的浓度接近
①浓硫酸可以干燥SO2
②燃煤中添加CaO可以减少SO2和温室气体的排放
③工业上用氢氟酸溶液腐蚀玻璃生产磨砂玻璃
④足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe2+
⑤标准状况下,O2与NO2按1∶4充满烧瓶,烧瓶倒置水中充分反应后,烧瓶内溶液的浓度接近

| A.②③ | B.①⑤ | C.①③ | D.③⑤ |
您最近一年使用:0次
6 . 实验室为探究铁与足量浓硫酸的反应,并验证SO2的性质,设计如图所示装置进行实验,下列说法错误的是
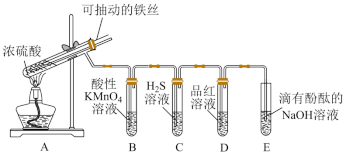
| A.常温下,可以用铁制容器盛装浓硫酸 |
| B.B中溶液紫色褪去,C中生成淡黄色沉淀,均体现了SO2的还原性 |
| C.D中品红溶液褪色,体现了SO2的漂白性 |
| D.E中溶液红色变浅,体现了SO2酸性氧化物的性质 |
您最近一年使用:0次
名校
7 . 某温度下,降冰片烯(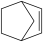 )在一定条件下聚合,反应物浓度与时间关系如图。已知反应物消耗一半所需的时间称为半衰期,下列说法正确的是
)在一定条件下聚合,反应物浓度与时间关系如图。已知反应物消耗一半所需的时间称为半衰期,下列说法正确的是
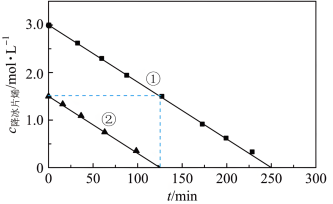
| A.降冰片烯与乙烯互为同系物 |
| B.其他条件相同时,降冰片烯浓度越大,反应速率越大 |
C.条件①,降冰片烯起始浓度为 时,半衰期为62.5min 时,半衰期为62.5min |
D.条件②,反应速率为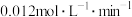 |
您最近一年使用:0次
名校
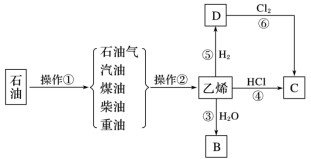
8 . 石油是工业的血液,与我们的生产、生活息息相关,乙烯的产量通常用来衡量一个国家的石油化工水平。根据下面转化关系回答下列问题:___________ 。
(2)写出乙烯和水反应生成B的反应③的化学方程式(注明条件):___________ ,反应类型为___________ 。写出反应⑥的化学方程式(注明条件):___________ ,反应类型为___________ 。
(3)物质C的沸点为12.27℃,常用于局部冷冻麻醉应急处理。物质C可通过反应④和反应⑥制得,其中最好的方法是反应___________ (填“④”或“⑥”),理由是___________ 。
(2)写出乙烯和水反应生成B的反应③的化学方程式(注明条件):
(3)物质C的沸点为12.27℃,常用于局部冷冻麻醉应急处理。物质C可通过反应④和反应⑥制得,其中最好的方法是反应
您最近一年使用:0次
名校
9 . 以黄铁矿为原料制硫酸会产生大量废渣,合理利用废渣可以减少环境污染,变废为宝。工业上利用废渣(含 、
、 的硫酸盐及少量CaO和MgO)制备高档颜料铁红
的硫酸盐及少量CaO和MgO)制备高档颜料铁红 ,同时回收
,同时回收 ,具体生产流程如图:
,具体生产流程如图:
(2)“过滤”操作所用到的玻璃仪器有___________ 。
(3)为了提高废渣的浸取率,可采取的措施有哪些?___________ (至少写出两点)。
(4)写出一种回收到的滤液的用途:___________ 。
(5)物质A的作用是___________ ,工业上物质A最好选用___________ (填标号)。
A.空气 B. C.
C. D.
D.
写出所选用试剂发生反应的离子方程式:___________ 。
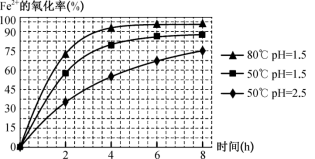
(6)根据如图所示的有关数据,你认为工业上进行“氧化”操作时应控制的条件有___________ (从温度、pH和氧化时间三方面说明)。
 、
、 的硫酸盐及少量CaO和MgO)制备高档颜料铁红
的硫酸盐及少量CaO和MgO)制备高档颜料铁红 ,同时回收
,同时回收 ,具体生产流程如图:
,具体生产流程如图: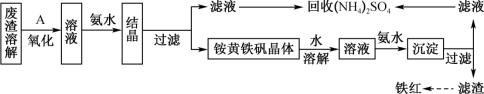
| A.水 | B.氢氧化钠溶液 | C.盐酸 | D.硫酸 |
(3)为了提高废渣的浸取率,可采取的措施有哪些?
(4)写出一种回收到的滤液的用途:
(5)物质A的作用是
A.空气 B.
 C.
C. D.
D.
写出所选用试剂发生反应的离子方程式:
(6)根据如图所示的有关数据,你认为工业上进行“氧化”操作时应控制的条件有
您最近一年使用:0次
10 . ⅰ.某学习小组在实验室中利用下图装置制备 并进行其相关性质的探究。
并进行其相关性质的探究。
(1)装置C中的现象为___________ ;装置D中的现象为___________ 。
(2)装置A中发生反应的化学方程式为___________ 。
(3)装置E中___________ (填现象)可说明 具有还原性。
具有还原性。
(4)装置F中过量的NaOH溶液吸收尾气,发生反应的离子方程式为___________ 。
ⅱ.某学习小组设计实验探究NO与铜粉的反应并检验NO,实验装置如图所示(夹持装置略),已知在溶液中: (棕色),该反应可用于检验NO。
(棕色),该反应可用于检验NO。 ,目的是
,目的是___________ 。
(6)写出装置E中发生反应的离子方程式:___________ 。
(7)若观察到装置H中红色粉末变黑,则NO与Cu发生反应,同时生成一种单质,写出该反应的化学方程式:___________ 。
 并进行其相关性质的探究。
并进行其相关性质的探究。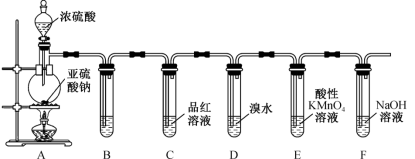
(1)装置C中的现象为
(2)装置A中发生反应的化学方程式为
(3)装置E中
 具有还原性。
具有还原性。(4)装置F中过量的NaOH溶液吸收尾气,发生反应的离子方程式为
ⅱ.某学习小组设计实验探究NO与铜粉的反应并检验NO,实验装置如图所示(夹持装置略),已知在溶液中:
 (棕色),该反应可用于检验NO。
(棕色),该反应可用于检验NO。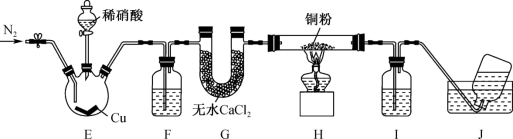
 ,目的是
,目的是(6)写出装置E中发生反应的离子方程式:
(7)若观察到装置H中红色粉末变黑,则NO与Cu发生反应,同时生成一种单质,写出该反应的化学方程式:
您最近一年使用:0次



