名校
1 . 已知短周期元素M、N、X、Y、Z分布在三个周期,N、X最外层电子数相同,Z原子序数大于X,其中Z的简单离子半径在同周期中最小,X单质极易与常见无色无味液态物质发生置换反应且做氧化剂,在短周期中Y的最高价氧化物对应水化物的碱性最强。回答下列问题:
(1)Y在周期表中的位置是_____ ;N的简单离子的核外电子排布示意图为_____ 。
(2)用电子式表示化合物YN的形成过程:_____ 。
(3)在YZO2与YX的混合液中,通入足量CO2,是工业制取Y3ZX6的一种方法,写出该反应的化学方程式:_____ 。
(4)镓(31Ga)的化合物氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。
①下列有关说法正确的是_____ (填字母)。
a.Ga位于元素周期表第四周期IVA族
b.Ga为门捷列夫预言的“类铝”
c.Ga的最高价氧化物对应水化物的碱性比Z元素最高价氧化物对应水化物的碱性强
②废弃的含GaAs的半导体材料可以用浓硝酸溶解,放出NO2气体,同时生成H3AsO4和Ga(NO3)3,写出该反应的化学方程式:_____ 。
(5)YZM4是有机合成的重要还原剂,其合成路线如图所示。
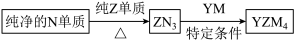
特定条件利用YZM4遇水反应生成的氢气的体积测定YZM4样品纯度。
①YZM4遇水反应的化学方程式为_____ 。
②现设计如图四种装置测定YZM4样品的纯度(假设杂质不参与反应)。

从简约性、准确性考虑,最适宜的方案是_____ (填编号)。
③取样品ag,若实验测得氢气的体积为VmL(标准状态),则YZM4样品纯度为_____ (用代数式表示)。
(1)Y在周期表中的位置是
(2)用电子式表示化合物YN的形成过程:
(3)在YZO2与YX的混合液中,通入足量CO2,是工业制取Y3ZX6的一种方法,写出该反应的化学方程式:
(4)镓(31Ga)的化合物氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。
①下列有关说法正确的是
a.Ga位于元素周期表第四周期IVA族
b.Ga为门捷列夫预言的“类铝”
c.Ga的最高价氧化物对应水化物的碱性比Z元素最高价氧化物对应水化物的碱性强
②废弃的含GaAs的半导体材料可以用浓硝酸溶解,放出NO2气体,同时生成H3AsO4和Ga(NO3)3,写出该反应的化学方程式:
(5)YZM4是有机合成的重要还原剂,其合成路线如图所示。

特定条件利用YZM4遇水反应生成的氢气的体积测定YZM4样品纯度。
①YZM4遇水反应的化学方程式为
②现设计如图四种装置测定YZM4样品的纯度(假设杂质不参与反应)。

从简约性、准确性考虑,最适宜的方案是
③取样品ag,若实验测得氢气的体积为VmL(标准状态),则YZM4样品纯度为
您最近一年使用:0次
名校
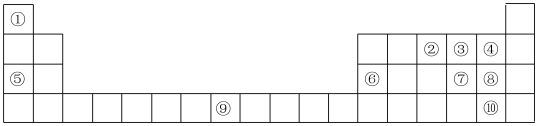
2 . (Ⅰ)如表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:_______ 。
(2)元素⑤和③的单质加热生成产物中含有的化学键类型为_______ 。
(3)元素⑨在周期表中的位置是_______ 。
(Ⅱ)L、M、N、Q、R、T分别代表上述十种元素之一,其原子半径及主要化合价关系如表:
(4)写出M最高价氧化物对应的水化物与N的最高价含氧酸反应的化学方程式:________ 。
(5)用一个离子方程式证明N和Q两元素的非金属性强弱:_______ 。
(6)R与T形成的简单氢化物的沸点较高的是:_______ (填化学式)。
(7)L、M、Q、R四种元素形成的简单离子半径从大到小的顺序为_______ (用相应的离子符号表示)。
(2)元素⑤和③的单质加热生成产物中含有的化学键类型为
(3)元素⑨在周期表中的位置是
(Ⅱ)L、M、N、Q、R、T分别代表上述十种元素之一,其原子半径及主要化合价关系如表:
| 元素代号 | L | M | N | Q | R | T |
| 原子半径/nm | 0.186 | 0.143 | 0.099 | 0.114 | 0.104 | 0.066 |
| 主要化合价 | +1 | +3 | +7、-1 | +7、-1 | +6、-2 | -2 |
(4)写出M最高价氧化物对应的水化物与N的最高价含氧酸反应的化学方程式:
(5)用一个离子方程式证明N和Q两元素的非金属性强弱:
(6)R与T形成的简单氢化物的沸点较高的是:
(7)L、M、Q、R四种元素形成的简单离子半径从大到小的顺序为
您最近一年使用:0次
2024-02-01更新
|
255次组卷
|
2卷引用:辽宁省沈阳市重点高中五校协作体2023-2024学年高一上学期1月期末化学试题
3 . 食品添加剂中可能存在的部分短周期元素的最高正化合价或最低负化合价与原子序数的关系如下图所示。已知:x为非金属元素,d元素的最外层电子数为内层电子数的3倍。
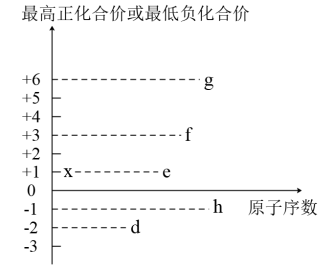
(1)x、e、d三种元素形成的离子化合物的电子式为___________ 。
(2)图中g元素所在元素周期表中的位置________ ,f元素形成的最高价氧化物与NaOH溶液反应的离子方程式为________ 。元素h的气态氢化物稳定性比元素g的气态氢化物稳定性_______ (填“强”或“弱”)。
(3)d、e、f、g元素的简单离子半径由大到小的顺序为___________ (用化学式表示)。
(4)x和d组成的化合物中,既含有极性共价键又含有非极性共价键的是___________ (填化学式)。
(5)一种麻醉剂的分子结构式如图所示。其中,X的原子核只有1个质子;元素Y、Z、W原子序数依次增大,且均位于X的下一周期;元素E的原子比W原子多8个电子,其中Z元素的化合价为___________ ,写出 分子的结构式
分子的结构式___________ 。
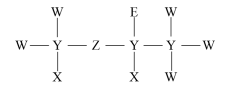

(1)x、e、d三种元素形成的离子化合物的电子式为
(2)图中g元素所在元素周期表中的位置
(3)d、e、f、g元素的简单离子半径由大到小的顺序为
(4)x和d组成的化合物中,既含有极性共价键又含有非极性共价键的是
(5)一种麻醉剂的分子结构式如图所示。其中,X的原子核只有1个质子;元素Y、Z、W原子序数依次增大,且均位于X的下一周期;元素E的原子比W原子多8个电子,其中Z元素的化合价为
 分子的结构式
分子的结构式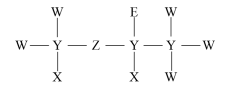
您最近一年使用:0次
4 . 氯元素形成的单质或化合物用途广泛。
(1)氯元素在周期表中的位置_____ 。
(2)工业上可用钢瓶储运液氯,在加注液氯前要对钢瓶进行充分干燥的原因是_____ (填合适的化学方程式)。
如图是氯的价类二维图:

其中C是一种新型净水剂,其合成路线如图:
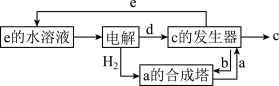
(3)C为______ (填化学式)。
(4)在氧化还原反应中,可将其拆成氧化半反应和还原半反应,比如:Zn+Cu2+=Zn2++Cu的氧化半反应可以表示为:Zn-2e-=Zn2+,电解时生成d的氧化半反应式为______ 。
(5)“a的合成塔”中发生反应的化学方程式为______ 。
(6)“c的发生器”中发生反应的离子方程式为_____ (写出正确的离子方程式并用单线桥法分析电子转移的情况)。
(7)实验测得等物质的量的f、O3、H2O2具有相同的漂白能力,原因是_____ 。
(1)氯元素在周期表中的位置
(2)工业上可用钢瓶储运液氯,在加注液氯前要对钢瓶进行充分干燥的原因是
如图是氯的价类二维图:

其中C是一种新型净水剂,其合成路线如图:

(3)C为
(4)在氧化还原反应中,可将其拆成氧化半反应和还原半反应,比如:Zn+Cu2+=Zn2++Cu的氧化半反应可以表示为:Zn-2e-=Zn2+,电解时生成d的氧化半反应式为
(5)“a的合成塔”中发生反应的化学方程式为
(6)“c的发生器”中发生反应的离子方程式为
(7)实验测得等物质的量的f、O3、H2O2具有相同的漂白能力,原因是
您最近一年使用:0次
解题方法
5 . W、X、Y、Z为原子序数依次增大的短周期主族元素,W2-与Ne原子的电子层结构相同,W、X、Y在元素周期表中的相对位置如图。下列有关叙述中正确的是
| W | |||
| X | Y |
| A.W、Y形成的化合物溶于水得到的一定是强酸 |
B.元素X、Y、Z形成的简单离子半径关系: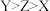 |
| C.含元素Z的化合物都具有漂白性 |
| D.W、X形成的化合物易溶于水 |
您最近一年使用:0次
解题方法
6 . A是一种重要的化工原料,A的产量可以用来衡量一个国家的石油化工水平,E是具有香味的无色透明油状液体。A、B、C、D在一定条件下存在如下转化关系(部分反应条件、产物被省略)。
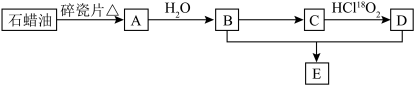
已知: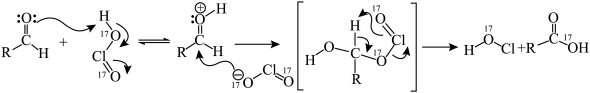
(1)回答下列问题。
① 的反应类型是
的反应类型是___________ ;
②A、D中官能团的名称分别是___________ 、___________ ;
③E的名称是___________ 。
(2)下列关于有机物A、B、C、D、E的说法正确的___________ 。
①通过煤的干馏可以得到A
②医疗上常用 (体积分数)的B溶液做消毒剂
(体积分数)的B溶液做消毒剂
③由C的官能团预测:C可能与新制的氢氧化铜反应,生成砖红色的氧化铜沉淀
④当温度低于D的熔点时,D可凝结成类似冰一样的晶体
⑤E的密度大于水
(3)根据已知信息,写出反应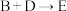 的化学方程式:
的化学方程式:___________ 。
(4)丁烷是由石蜡油获得A的过程中的中间产物之一,它的一氯代物同分异构体有___________ 种。写出其中含有三个甲基的有机物结构简式:___________ 。
(5)三名科学家因在有机合成的复分解反应研究方面做出重大贡献而获得诺贝尔化学奖。一种利用该类型反应生产乙烯的合成路线如下图所示。
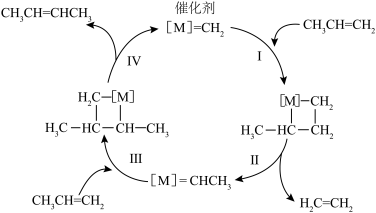
①步骤Ⅰ~Ⅳ中属于加成反应的是___________ (填序号)
②写出上述合成路线的总反应方程式:___________ 。

已知:

(1)回答下列问题。
①
 的反应类型是
的反应类型是②A、D中官能团的名称分别是
③E的名称是
(2)下列关于有机物A、B、C、D、E的说法正确的
①通过煤的干馏可以得到A
②医疗上常用
 (体积分数)的B溶液做消毒剂
(体积分数)的B溶液做消毒剂③由C的官能团预测:C可能与新制的氢氧化铜反应,生成砖红色的氧化铜沉淀
④当温度低于D的熔点时,D可凝结成类似冰一样的晶体
⑤E的密度大于水
(3)根据已知信息,写出反应
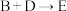 的化学方程式:
的化学方程式:(4)丁烷是由石蜡油获得A的过程中的中间产物之一,它的一氯代物同分异构体有
(5)三名科学家因在有机合成的复分解反应研究方面做出重大贡献而获得诺贝尔化学奖。一种利用该类型反应生产乙烯的合成路线如下图所示。

①步骤Ⅰ~Ⅳ中属于加成反应的是
②写出上述合成路线的总反应方程式:
您最近一年使用:0次
2023-07-13更新
|
247次组卷
|
2卷引用:辽宁省五校(大连二十四中、东北育才等)2022-2023学年高一下学期期末考试化学试题
解题方法
7 . 为了研究有机物A的组成与结构,某同学进行如下实验。
i.将9.0 g A在足量氧气中充分燃烧,并使其产物依次缓缓通过足量的浓硫酸和碱石灰,发现两者分别增重5.4 g和13.2 g。
ii.通过质谱法测得其相对分子质量为90。
iii.通过红外光谱法测得A中含有-OH和-COOH。
请回答下列问题。
(1)9.0 g A完全燃烧生成水的物质的量是____________ mol。
(2)A的分子式是____________ 。
(3)在一定条件下,若两个A分子可以反应得到一个六元环的分子,还能发生缩聚反应,写出A发生缩聚反应的方程式____________________________________ 。
(4)试写出由与A含有相同C原子数的烯烃为原料(无机试剂及催化剂任用)合成A的合成路线_________________________ 。(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
i.将9.0 g A在足量氧气中充分燃烧,并使其产物依次缓缓通过足量的浓硫酸和碱石灰,发现两者分别增重5.4 g和13.2 g。
ii.通过质谱法测得其相对分子质量为90。
iii.通过红外光谱法测得A中含有-OH和-COOH。
请回答下列问题。
(1)9.0 g A完全燃烧生成水的物质的量是
(2)A的分子式是
(3)在一定条件下,若两个A分子可以反应得到一个六元环的分子,还能发生缩聚反应,写出A发生缩聚反应的方程式
(4)试写出由与A含有相同C原子数的烯烃为原料(无机试剂及催化剂任用)合成A的合成路线
您最近一年使用:0次
8 . 吡唑类化合物是重要的医用中间体,下图是吡唑类物质 L 的合成路线
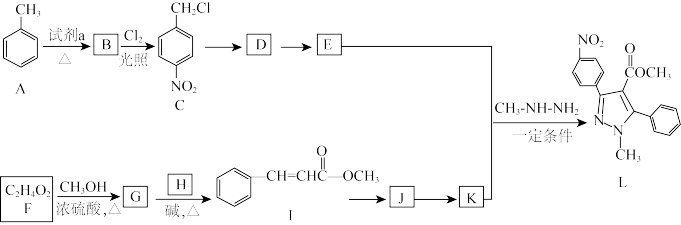
已知:R1-CHO+R2CH2-COOR3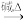
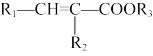
R1-CHO+R2NH2 R1-CH=N-R2
R1-CH=N-R2
(1)试剂 a 是_____
(2)C生成D的反应类型是_____
(3)D生成E的化学方程式是_____
(4)生成G的化学方程式是_____
(5)H的结构简式是_____
(6)写出符合下列条件的 I 的同分异构体的结构简式_____ (写出一种即可)
a.是反式结构 b. 能发生银镜反应和水解反应 c. 苯环上的一氯代物有 2 种
(7)K的分子式是C10H8O2,K 的结构简式是_____
(8)以 2-甲基丙烯和乙酸为原料,选用必要的无机试剂,合成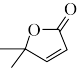 写出合成 路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
写出合成 路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)_____

已知:R1-CHO+R2CH2-COOR3
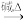
R1-CHO+R2NH2
 R1-CH=N-R2
R1-CH=N-R2(1)试剂 a 是
(2)C生成D的反应类型是
(3)D生成E的化学方程式是
(4)生成G的化学方程式是
(5)H的结构简式是
(6)写出符合下列条件的 I 的同分异构体的结构简式
a.是反式结构 b. 能发生银镜反应和水解反应 c. 苯环上的一氯代物有 2 种
(7)K的分子式是C10H8O2,K 的结构简式是
(8)以 2-甲基丙烯和乙酸为原料,选用必要的无机试剂,合成
 写出合成 路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
写出合成 路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
您最近一年使用:0次
名校
解题方法
9 . (1)下面是4种粒子的结构示意图:
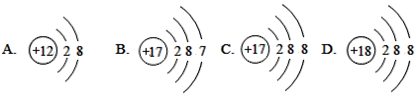
图中粒子共能表示_______ 种元素,图中表示的阳离子是____________ (用离子符号表示),图中A所表示的元素在元素周期表中的位置_____________________________ .
(2)在1-18号的短周期主族元素中,表中的字母代表一种元素,回答下列问题:
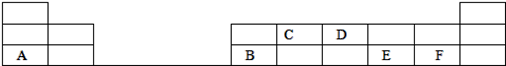
①写出D单质的电子式_____________________ ;
②写出C的最高价氧化物的结构式_____________________ ;
③E和F分别形成的气态氢化物中较稳定的是(填写氢化物的化学式)_____________________ ;
④A最高价氧化物的水化物所含化学键为___________________ ,其水溶液与B反应的离子方程式为___________________________ ;
(3)X、Y、Z、M、N、Q皆为短周期主族元素,其原子半径与主要化合价的关系如图所示.下列说法正确的是( )
A.金属性:N>Q
B.最高价氧化物对应水化物的酸性:M>Y
C.简单离子半径:Q>N>X
D.原子序数:Z>M>X>Y
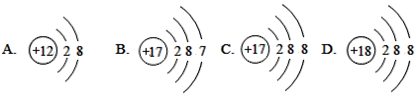
图中粒子共能表示
(2)在1-18号的短周期主族元素中,表中的字母代表一种元素,回答下列问题:

①写出D单质的电子式
②写出C的最高价氧化物的结构式
③E和F分别形成的气态氢化物中较稳定的是(填写氢化物的化学式)
④A最高价氧化物的水化物所含化学键为
(3)X、Y、Z、M、N、Q皆为短周期主族元素,其原子半径与主要化合价的关系如图所示.下列说法正确的是
A.金属性:N>Q
B.最高价氧化物对应水化物的酸性:M>Y
C.简单离子半径:Q>N>X
D.原子序数:Z>M>X>Y
您最近一年使用:0次
2017-07-17更新
|
588次组卷
|
5卷引用:辽宁省抚顺中学2017-2018学年高一上学期期末考试化学试题
名校
解题方法
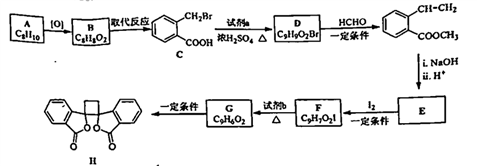
10 . 具有抗菌作用的白头翁素衍生物H的合成路线如下图所示:
已知:
ⅰ.
ⅱ.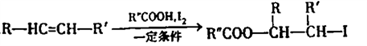
ⅲ.
(以上R、R′、R″代表氢、烷基或芳基等)
(1)A属于苯的同系物,其名称是___________________ 。
(2)B的结构简式是_______________ 。
(3)由C生成D的化学方程式是_________________ 。
(4)由E与I2在一定条件下反应生成F的化学方程式是_____________________ ,此反应同时生成另外一个有机副产物且与F互为同分异构体,此有机副产物的结构简式是______________ 。
(5)试剂b是____________ 。
(6)下列说法正确的是_____ (选填字母序号)。
a.G存在顺反异构体
b.由C生成H的反应是加成反应
c.1mol G最多可以与lmolH2发生加成反应
d.1molF或1molH与足量NaOH溶液反应,均消耗2molNaOH
(7)以乙烯为起始原料,结合已知信息选用必要的无机试剂合成 ,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)_____ 。

已知:
ⅰ.

ⅱ.

ⅲ.

(以上R、R′、R″代表氢、烷基或芳基等)
(1)A属于苯的同系物,其名称是
(2)B的结构简式是
(3)由C生成D的化学方程式是
(4)由E与I2在一定条件下反应生成F的化学方程式是
(5)试剂b是
(6)下列说法正确的是
a.G存在顺反异构体
b.由C生成H的反应是加成反应
c.1mol G最多可以与lmolH2发生加成反应
d.1molF或1molH与足量NaOH溶液反应,均消耗2molNaOH
(7)以乙烯为起始原料,结合已知信息选用必要的无机试剂合成
 ,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
您最近一年使用:0次
2017-11-11更新
|
283次组卷
|
2卷引用:辽宁师范大学附属中学2018届高三上学期期末考试化学试题



