名校
解题方法
1 . 下列反应的离子方程式正确的是( )
①小苏打溶液中加入少量的石灰水:Ca2++OH-+HCO-3=CaCO3↓+2H2O
②将金属钠加入水中:2Na+2H2O=2Na++2OH-+H2↑
③石灰石溶于醋酸:CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O
④氯气与水反应:Cl2+H2O=2H++Cl-+ClO-
⑤纯碱溶液中滴加少量盐酸:CO32-+H+=HCO-3
⑥次氯酸钙溶液中通入足量二氧化碳:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO
⑦氯化亚铁溶液中通入氯气:Fe2++Cl2=Fe3++2Cl-
⑧铜片插入三氯化铁溶液中:Cu+Fe3+=Cu2++Fe2+
⑨氯化铝溶液中滴加过量的氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH+4
①小苏打溶液中加入少量的石灰水:Ca2++OH-+HCO-3=CaCO3↓+2H2O
②将金属钠加入水中:2Na+2H2O=2Na++2OH-+H2↑
③石灰石溶于醋酸:CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O
④氯气与水反应:Cl2+H2O=2H++Cl-+ClO-
⑤纯碱溶液中滴加少量盐酸:CO32-+H+=HCO-3
⑥次氯酸钙溶液中通入足量二氧化碳:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO
⑦氯化亚铁溶液中通入氯气:Fe2++Cl2=Fe3++2Cl-
⑧铜片插入三氯化铁溶液中:Cu+Fe3+=Cu2++Fe2+
⑨氯化铝溶液中滴加过量的氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH+4
| A.①②⑤⑨ | B.②③⑤⑨ | C.④⑤⑥⑦ | D.②③⑧⑨ |
您最近一年使用:0次
名校
2 . 下列实验过程中产生的现象与对应图形相符合的是( )
A. 向盐酸中加入NaAlO2溶液 向盐酸中加入NaAlO2溶液 |
B. pH=1的醋酸和盐酸分别加等量水稀释 pH=1的醋酸和盐酸分别加等量水稀释 |
C.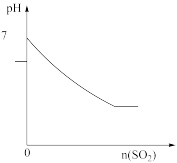 SO2气体通入溴水中 SO2气体通入溴水中 |
D. 氨气通入醋酸溶液中 氨气通入醋酸溶液中 |
您最近一年使用:0次
2020-03-06更新
|
97次组卷
|
2卷引用:山西省实验中学2020届高三化学复习针对性试题集(六)
名校
解题方法
3 . 下列叙述正确的是( )
| A.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数 |
| B.X、Y均为短周期元素,其简单离子mXa+与nYb-的电子层结构相同,则m+a=n-b。 |
| C.F、Cl、Br的最外层电子数都是7,次外层电子数都是8 |
| D.结合质子(H+)能力:OH->CH3COO->Cl- |
您最近一年使用:0次
名校
解题方法
4 . 下列说法不正确 的是 ( )
① C2H6分子中既含极性键又含非极性键
② 若R2—和M+的电子层结构相同,则原子序数:R>M
③ F2、Cl2、Br2、I2熔点随相对分子质量增大而升高
④ NCl3、PCl3、CO2、CS2分子中各原子均达到8e-稳定结构
⑤ 若X的质子数为a,中子数为b,则原子可表示为abX
⑥由于氨和水分子之间能形成氢键,NH3分子极易溶于水
⑦原子序数为34号的元素属于长周期的副族元素
① C2H6分子中既含极性键又含非极性键
② 若R2—和M+的电子层结构相同,则原子序数:R>M
③ F2、Cl2、Br2、I2熔点随相对分子质量增大而升高
④ NCl3、PCl3、CO2、CS2分子中各原子均达到8e-稳定结构
⑤ 若X的质子数为a,中子数为b,则原子可表示为abX
⑥由于氨和水分子之间能形成氢键,NH3分子极易溶于水
⑦原子序数为34号的元素属于长周期的副族元素
| A.②⑤⑦ | B.①③④⑤ | C.②④⑤⑥ | D.③⑤⑥⑦ |
您最近一年使用:0次
名校
解题方法
5 . 如图所示2套实验装置,分别回答下列问题。
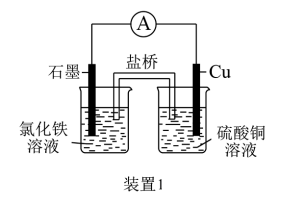
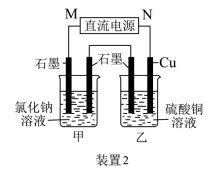
(1)装置1中的Cu是_________ 极(填“正”或“负”),该装置发生的总反应的离子方程式为___________ 。
(2)装置2中甲烧杯盛放100 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5 mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到右边石墨电极附近首先变红,左边石墨电极附近无明显现象。
① 电源的M端为_________ 极,甲烧杯右边石墨电极附近首先变红的原因是___________________ 。
② 乙烧杯中电解反应的离子方程式为____________ 。
③ 若装置甲阴、阳两极各产生112mL气体(标准状况),则装置乙所得溶液的pH为______ (忽略反应前后溶液的体积变化)。


(1)装置1中的Cu是
(2)装置2中甲烧杯盛放100 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5 mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到右边石墨电极附近首先变红,左边石墨电极附近无明显现象。
① 电源的M端为
② 乙烧杯中电解反应的离子方程式为
③ 若装置甲阴、阳两极各产生112mL气体(标准状况),则装置乙所得溶液的pH为
您最近一年使用:0次
名校
6 . 体积相同的盐酸和醋酸两种溶液,n(Cl-)=n(CH3COO-)=0.01mol,下列叙述错误的是
| A.它们分别与足量CaCO3反应时,放出的CO2一样多 |
| B.它们与NaOH完全中和时,醋酸溶液所消耗的NaOH多 |
| C.两种溶液的pH相同 |
| D.分别用水稀释相同倍数时,n(Cl-)<n(CH3COO-) |
您最近一年使用:0次
名校
7 . 元素周期表中同周期或同主族元素,随着原子序数的递增,下列说法正确的是
| A.ⅦA族元素的氢化物沸点逐渐升高 |
| B.ⅥA族元素的原子核外最外层电子数逐渐增多 |
| C.碱金属元素的最高价氧化物的水化物的碱性逐渐增强 |
| D.第二周期元素(除稀有气体元素)的最高化合价数值逐渐增大 |
您最近一年使用:0次
2020-03-06更新
|
226次组卷
|
3卷引用:山西省实验中学2020届高三化学复习针对性试题集(三)
山西省实验中学2020届高三化学复习针对性试题集(三)(已下线)专题16 元素周期律和元素周期表(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练上海市建平中学2020-2021学年高三上学期期中考试化学试题
名校
解题方法
8 . 某密闭容器中放入一定量的NO2,发生反应2NO2(g) N2O4(g) △H<0,在达平衡后,若分别单独改变下列条件,重新达到平衡后,
N2O4(g) △H<0,在达平衡后,若分别单独改变下列条件,重新达到平衡后,有可能 使平衡混合气体平均相对分子质量减小的是
 N2O4(g) △H<0,在达平衡后,若分别单独改变下列条件,重新达到平衡后,
N2O4(g) △H<0,在达平衡后,若分别单独改变下列条件,重新达到平衡后,| A.通入NO2 | B.通入N2O4 | C.通入N2 | D.降低温度 |
您最近一年使用:0次
名校
9 . 下列装置或操作能达到实验目的的是
①从碘水中分离出碘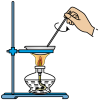 ②用铜和稀硝酸制取少量NO
②用铜和稀硝酸制取少量NO
③证明铁生锈空气参与反应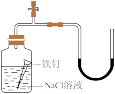 ④检验装置气密性
④检验装置气密性
①从碘水中分离出碘
 ②用铜和稀硝酸制取少量NO
②用铜和稀硝酸制取少量NO
③证明铁生锈空气参与反应
 ④检验装置气密性
④检验装置气密性
| A.①②③④ | B.③④ | C.②③④ | D.①② |
您最近一年使用:0次
10 . 常温下,下列离子能与H+、Cl—、Fe3+在同一溶液中大量共存的是
| A.Fe2+ | B.ClO— | C.I— | D.HCO3— |
您最近一年使用:0次



