名校
解题方法
1 . 中学化学中几种常见物质的转化关系如图所示(图中部分反应物或生成物及反应条件未列出)。已知:A、B、C、D、E是单质, X、Y、Z、M、N、W、H、K是化合物,其中B是短周期中原子半径最大的元素的单质、D和E为应用广泛的金属单质。请回答下列问题:

(1)组成C的元素的原子结构示意图是_____________ 。
(2)写出B在氧气中燃烧生成的产物与H2O反应的化学方程式___________ ;
(3)用惰性电极电解X的水溶液的阴极反应方程式________________________ ;
(4)写出实验室制备M的化学方程式_____________________________________ ;

(1)组成C的元素的原子结构示意图是
(2)写出B在氧气中燃烧生成的产物与H2O反应的化学方程式
(3)用惰性电极电解X的水溶液的阴极反应方程式
(4)写出实验室制备M的化学方程式
您最近一年使用:0次
名校
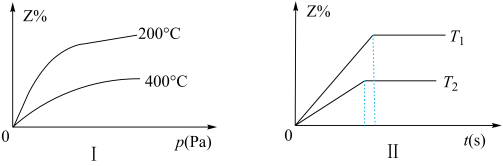
2 . 在一密闭容器中充入X和Y,在一定条件下进行如下反应:aX(g)+bY(g) cZ(g)+dW(s),如图I是不同温度下反应达到平衡时,反应混合物中Z的体积分数和压强关系的示意图,下列说法中正确的是
cZ(g)+dW(s),如图I是不同温度下反应达到平衡时,反应混合物中Z的体积分数和压强关系的示意图,下列说法中正确的是
 cZ(g)+dW(s),如图I是不同温度下反应达到平衡时,反应混合物中Z的体积分数和压强关系的示意图,下列说法中正确的是
cZ(g)+dW(s),如图I是不同温度下反应达到平衡时,反应混合物中Z的体积分数和压强关系的示意图,下列说法中正确的是
| A.由图I得K(200℃)>K(400℃),但a+b与c+d的大小无法比较 |
| B.若a=c,在保持Y浓度不变的前提下,使X和Z的浓度增大相同的倍数,平衡正向移动 |
| C.若反应在恒容容器中进行,达平衡后再充入气体Z,由于压强增大,平衡正向移动 |
| D.该反应在不同温度下(T2>T1),Z的体积分数与时间的关系图象可用图Ⅱ表示 |
您最近一年使用:0次
名校
3 . 以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工
(1)将水蒸气通过红热的碳即可产生水煤气。反应为:C(s)+H2O(g) CO(g)+H2(g) ΔH=+131.3 kJ•mol-1。
CO(g)+H2(g) ΔH=+131.3 kJ•mol-1。
①该反应在常温下____________ 自发进行(填“能”与“不能”);
②一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是______________ (填字母,下同)。
a.容器中的压强不变 b.1 mol H—H键断裂的同时断裂2 mol H—O键
c.c(CO)=c(H2) d.密闭容器的容积不再改变
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
①实验1中以v(CO2) 表示的反应速率为________________ 。(取小数二位,下同)
②该反应为_____ (填“吸”或“放”)热反应,实验2条件下平衡常数K=________ 。
③若实验3达平衡时与实验2平衡状态中各物质的质量分数分别相等,且t<3min,则a、b应满足的关系是________________________ (用含a、b的数学式表示)。
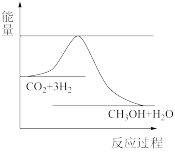
(3)目前工业上有一种方法是用CO2来生产甲醇。一定条件下发生反应: CO2(g)+3H2(g) CH3OH(g)+H2O(g) ,如图表示该反应进行过程中能量(单位为kJ•mol-1)的变化。在体积为1 L的恒容密闭容器中,充入1mol CO2和3mol H2,下列措施中能使c(CH3OH)增大的是
CH3OH(g)+H2O(g) ,如图表示该反应进行过程中能量(单位为kJ•mol-1)的变化。在体积为1 L的恒容密闭容器中,充入1mol CO2和3mol H2,下列措施中能使c(CH3OH)增大的是___________ 。
a.升高温度
b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离出来
d.再充入1mol CO2和3mol H2
(1)将水蒸气通过红热的碳即可产生水煤气。反应为:C(s)+H2O(g)
 CO(g)+H2(g) ΔH=+131.3 kJ•mol-1。
CO(g)+H2(g) ΔH=+131.3 kJ•mol-1。①该反应在常温下
②一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是
a.容器中的压强不变 b.1 mol H—H键断裂的同时断裂2 mol H—O键
c.c(CO)=c(H2) d.密闭容器的容积不再改变
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)
 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 6 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
①实验1中以v(CO2) 表示的反应速率为
②该反应为
③若实验3达平衡时与实验2平衡状态中各物质的质量分数分别相等,且t<3min,则a、b应满足的关系是
(3)目前工业上有一种方法是用CO2来生产甲醇。一定条件下发生反应: CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ,如图表示该反应进行过程中能量(单位为kJ•mol-1)的变化。在体积为1 L的恒容密闭容器中,充入1mol CO2和3mol H2,下列措施中能使c(CH3OH)增大的是
CH3OH(g)+H2O(g) ,如图表示该反应进行过程中能量(单位为kJ•mol-1)的变化。在体积为1 L的恒容密闭容器中,充入1mol CO2和3mol H2,下列措施中能使c(CH3OH)增大的是
a.升高温度
b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离出来
d.再充入1mol CO2和3mol H2
您最近一年使用:0次
名校
4 . 下列关于有机物的说法正确的是
A. 的同分异构体中,有醇、酚、酯类物质 的同分异构体中,有醇、酚、酯类物质 |
B.1 mol 最多能与4 mol NaOH反应 最多能与4 mol NaOH反应 |
| C.纯净物C4H8的核磁共振氢谱峰最多为4 |
| D.化学式为C8H8的有机物,一定能使酸性高锰酸钾溶液褪色 |
您最近一年使用:0次
名校
解题方法
5 . 下列离子方程式中正确的是
| A.在硫酸氢钾溶液中加入氢氧化钡溶液至pH =7:Ba2++OH—+H++SO42—=BaSO4↓+H2O |
| B.FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+=4Fe3++2H2O |
| C.甲醇、氧气和氢氧化钾溶液组成的燃料电池的负极反应:CH3OH+H2O-6e—=CO2↑+6H+ |
| D.NH4A1(SO4)2溶液中加入过量Ba(OH)2溶液:A13++2SO42—+2Ba2++4OH—=A1O2—+2BaSO4↓+2H2O |
您最近一年使用:0次
名校
解题方法
6 . 下列离子组可能大量共存的是
| A.甲基橙呈黄色的溶液中:I-、Cl-、NO3-、Na+ |
| B.石蕊呈蓝色的溶液中:Na+、AlO2-、NO3-、NH4+ |
| C.含大量Al3+的溶液中:K+、Na+、NO3-、HCO3- |
| D.含大量H+的溶液中:SO42-、Cl-、F-、K+ |
您最近一年使用:0次
7 . NA代表阿伏加 德罗常数,下列说法正确的是
| A.标准状况下,22.4LSO3中含有氧原子数目为3NA |
| B.在25℃、101kPa下,1 mol 硫和2 mol硫燃烧热相等 |
| C.18 g D2O中含有的质子数目为10NA |
| D.含0.5 mol H2SO4的稀溶液与含0.5mol Ba(OH)2 的晶体完全中和所放出的热量为中和热 |
您最近一年使用:0次
名校
解题方法
8 . 下列离子方程式正确的是
| A.氮化镁投入过量盐酸 Mg3N2+6H+=3Mg2++2NH3↑ |
| B.硫化亚铁固体投入过量稀硝酸 3FeS+8H++2NO3—=3Fe2++2NO↑+3S+4H2O |
| C.过量二氧化硫通入次氯酸钠溶液 SO2+ClO-+H2O=SO42-+Cl—+2H+ |
| D.偏铝酸钠溶液中通入足量二氧化碳 2AlO2—+CO2+2H2O=2Al(OH)3↓+CO32— |
您最近一年使用:0次
9 . 下列文字表述与对应的化学用语或名称关系正确的是
A.CS2的电子式为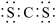 |
B.光气(COCl2)结构式为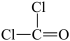 |
C.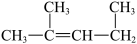 的名称为1,3-二甲基-2-丁烯 的名称为1,3-二甲基-2-丁烯 |
D.NaH中氢离子结构示意图为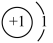 |
您最近一年使用:0次
名校
解题方法
10 . 四种短周期元素A、B、C、D原子序数依次增大。A、B、C三种元素原子核外电子层数之和是5。A、B两种元素原子最外层电子数之和等于C元素原子最外电子层上的电子数;B元素原子最外电子层上的电子数是它电子层数的2倍,A和C可以形成化合物CA3,B与D的原子序数之比为3∶4。请回答:
(1)化合物CA3的化学式是__________ 。
(2)写出A和C化合生成CA3反应的平衡常数表达式_________ 。在一定条件下要使该反应平衡向右移动,可采取的措施有________ 。
A 缩小反应容器容积 B 增大反应容器容积
C 使用合适的催化剂 D 及时分离出生成物
(3)由四种元素中的三种元素组成的物质甲属于盐类,其水溶液呈酸性,请用离子方程式表示其呈酸性的原因__________ ,若用pH试纸测定0.1 mol/L的甲溶液的pH,实验操作是__________
(4)乙和丙为含有上述四种元素的常见无机盐,二者均既可与盐酸又可与烧碱溶液反应。则乙和丙的化学式为乙:___________ ;丙__________ 。
(5)写出乙溶液与硫酸氢钠溶液反应的离子方程式_________ 。
(1)化合物CA3的化学式是
(2)写出A和C化合生成CA3反应的平衡常数表达式
A 缩小反应容器容积 B 增大反应容器容积
C 使用合适的催化剂 D 及时分离出生成物
(3)由四种元素中的三种元素组成的物质甲属于盐类,其水溶液呈酸性,请用离子方程式表示其呈酸性的原因
(4)乙和丙为含有上述四种元素的常见无机盐,二者均既可与盐酸又可与烧碱溶液反应。则乙和丙的化学式为乙:
(5)写出乙溶液与硫酸氢钠溶液反应的离子方程式
您最近一年使用:0次
2020-03-06更新
|
89次组卷
|
2卷引用:山西省实验中学2020届高三化学复习针对性试题集(二)



