名校
解题方法
1 . 铁是日常生活中最常见的金属,某班同学在学习铁的知识时,有下列问题:
问题1:铁为何称为黑色金属?
问题2:CuO在高温下可分解为Cu2O和O2,Fe2O3在高温下可分解为FeO和O2吗?
(1)对于问题1,同学们上网查找,有两种解释:
A.因为在铁表面上有黑色的铁的氧化物,所以叫黑色金属
B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属
①你认为正确的说法是__________ 。
②若有一黑色粉末,如何鉴别是铁粉,还是Fe3O4?______________________________________ 。
③若有一黑色粉末,为铁和四氧化三铁的混合物,如何证明其中有Fe3O4(只要求简述实验方法)?____________________________________ 。
(2)对于问题2,同学们准备实验探究,他们设想了两种方法:
A.将三氧化二铁高温灼烧,看灼烧前后颜色是否变化。
B.将三氧化二铁高温灼烧,看灼烧前后质量是否变化。
①实验中应将Fe2O3放在__________ (填仪器名称)中灼烧。
②方法A中,如果高温灼烧后颜色由__________ 变为__________ ,说明Fe2O3确实发生了变化。能说明生成的一定为FeO吗?__________ ,理由是________________________ 。
③方法B中,如果发生了预期的反应,固体高温灼烧前后质量比应为________ ,但是,实验结果固体灼烧前后质量比为30∶29,则高温灼烧后生成物是____________________ 。
④比较两种方法,你认为较好的方法是__________ 。
问题1:铁为何称为黑色金属?
问题2:CuO在高温下可分解为Cu2O和O2,Fe2O3在高温下可分解为FeO和O2吗?
(1)对于问题1,同学们上网查找,有两种解释:
A.因为在铁表面上有黑色的铁的氧化物,所以叫黑色金属
B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属
①你认为正确的说法是
②若有一黑色粉末,如何鉴别是铁粉,还是Fe3O4?
③若有一黑色粉末,为铁和四氧化三铁的混合物,如何证明其中有Fe3O4(只要求简述实验方法)?
(2)对于问题2,同学们准备实验探究,他们设想了两种方法:
A.将三氧化二铁高温灼烧,看灼烧前后颜色是否变化。
B.将三氧化二铁高温灼烧,看灼烧前后质量是否变化。
①实验中应将Fe2O3放在
②方法A中,如果高温灼烧后颜色由
③方法B中,如果发生了预期的反应,固体高温灼烧前后质量比应为
④比较两种方法,你认为较好的方法是
您最近一年使用:0次
名校
解题方法
2 . 已知某白色粉末只有K2SO4、NH4HCO3、KCl、NH4Cl、CuSO4五种物质中的两种,为检验该白色粉末的成分,请完成下列实验:
实验一:取适量该白色粉末于烧杯中,加蒸馏水溶解,得到无色透明溶液A。将溶液A分成两份,分别装于两支试管中,向其中一支试管里滴加稀硝酸,有无色气泡产生。
由此判断,该白色粉末中肯定含有__________ ,肯定不含有__________ 。
实验二:
实验三:
实验一:取适量该白色粉末于烧杯中,加蒸馏水溶解,得到无色透明溶液A。将溶液A分成两份,分别装于两支试管中,向其中一支试管里滴加稀硝酸,有无色气泡产生。
由此判断,该白色粉末中肯定含有
实验二:
| 待检验物质 | 实验操作 | 预期现象和结论 |
| K2SO4 | 向盛有溶液A的另一支试管中滴加 |
| 实验前提 | 实验操作 | 预期现象和结论 |
| 若白色 粉末中不 含K2SO4 | 取少量原固体混合物于试管中,用酒精灯充分加热 | 如果试管底部有固体残留,则混合物中含有 |
您最近一年使用:0次
名校
解题方法
3 . A、B、C、D、E、F六种常见的单质或化合物在一定条件下有如下图所示的相互转化关系,所有反应物和生成物均已给出。
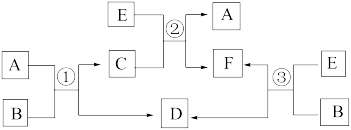
(1)若B在常温下为液态;C是一种有磁性的化合物;E是一种无色、无味的有毒气体。则反应③的化学方程式______________ 。
(2)若B由两种元素组成,其简单离子的电子层结构相同;绿色植物的光合作用和呼吸作用可实现自然界中D、E的循环。则B的电子式为_________________ ,11.6 g A和E组成的混合气体与足量的B固体反应,固体增重3.6 g,则A、E混合气中E 的体积分数为_________________________ 。
(3)若A和E都是第四周期常见的金属单质,其余都是常见的盐,反应①②③都在溶液中进行,则B、C、F氧化性由强到弱顺序为(用离子符号表示)____________ 。

(1)若B在常温下为液态;C是一种有磁性的化合物;E是一种无色、无味的有毒气体。则反应③的化学方程式
(2)若B由两种元素组成,其简单离子的电子层结构相同;绿色植物的光合作用和呼吸作用可实现自然界中D、E的循环。则B的电子式为
(3)若A和E都是第四周期常见的金属单质,其余都是常见的盐,反应①②③都在溶液中进行,则B、C、F氧化性由强到弱顺序为(用离子符号表示)
您最近一年使用:0次
名校
解题方法
4 . 物质A有如下图所示转化关系,其中乙为金属单质,常温下,它在G 的浓溶液中发生钝化, F 的溶液中只含有一种溶质(有的反应可能在水溶液中进行,有的反应的生成物未全部给出,反应条件也未注明)。请讨论以下两种情况 (注:两种情况下各字母代表的物质可能不同)
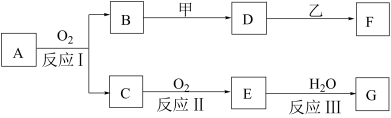
回答下列问题:
(1)第一种情况:用两根玻璃棒分别蘸取 A、G的浓溶液并使它们接近时,有大量白烟生成;甲为焰色反应呈黄色的金属单质; D 和 F 的溶液均呈碱性。则:①反应Ⅲ的化学方程式 为__________________________ 。
②D与乙反应的离子方程式 为_________________________________________
(2)第二种情况: 甲由两种单质直接化合得到;B 为红棕色固体; C为无色气体,是形成酸雨的大气污染物之一;D 的水溶液加入用硝酸酸化的AgNO3溶液有白色沉淀生成。则:
①工业上,反应 I的化学方程式为______________________________________ 生产设备名称为:__________
②D和乙反应的离子方程式 为______________________________________________
③ 请简述检验D溶液中阳离子的方法__________________________________ 。
④ 若A的相对分子质量为120,反应Ⅰ、Ⅱ、Ⅲ均为完全转化。现取m克含A及少量杂质的样品,按上述过程充分反应后(杂质不参与反应),得到密度为ρg/cm3,溶质质量分数为a% 的G溶液n mL。则该样品中A的质量分数=_____________ (列出计算式即可)。

回答下列问题:
(1)第一种情况:用两根玻璃棒分别蘸取 A、G的浓溶液并使它们接近时,有大量白烟生成;甲为焰色反应呈黄色的金属单质; D 和 F 的溶液均呈碱性。则:①反应Ⅲ的
②D与乙反应的
(2)第二种情况: 甲由两种单质直接化合得到;B 为红棕色固体; C为无色气体,是形成酸雨的大气污染物之一;D 的水溶液加入用硝酸酸化的AgNO3溶液有白色沉淀生成。则:
①工业上,反应 I的化学方程式为
②D和乙反应的
③ 请简述检验D溶液中阳离子的方法
④ 若A的相对分子质量为120,反应Ⅰ、Ⅱ、Ⅲ均为完全转化。现取m克含A及少量杂质的样品,按上述过程充分反应后(杂质不参与反应),得到密度为ρg/cm3,溶质质量分数为a% 的G溶液n mL。则该样品中A的质量分数=
您最近一年使用:0次
名校
5 . 质隐形眼镜材料W、树脂X的合成路线如下:

已知:
(1)A 中含有的官能团名称是___________ 。
(2)甲的结构简式是___________ 。
(3)B → C反应的化学方程式是___________ 。
(4)B有多种同分异构体。属于酯且含有碳碳双键的同分异构体共有__________ 种(不考虑顺反异构,下同),写出其中能发生银镜反应,且含有甲基的所有同分异构体的结构简式是__________ 。
(5)已知F的相对分子质量为110,分子中碳原子、氢原子数都是氧原子数的3倍,苯环上的氢原子化学环境都相同。则F还能发生的反应是(填序号)___________ 。
a 加成反应 b 氧化反应 c 加聚反应 d 分解反应
(6)写出树脂X可能的结构简式(写出一种即可)_________ 。
(7)E的分子式为C10H14O2,含三个甲基,苯环上的一溴代物有两种。生成E的化学方程式是_________ 。

已知:

(1)A 中含有的官能团名称是
(2)甲的结构简式是
(3)B → C反应的化学方程式是
(4)B有多种同分异构体。属于酯且含有碳碳双键的同分异构体共有
(5)已知F的相对分子质量为110,分子中碳原子、氢原子数都是氧原子数的3倍,苯环上的氢原子化学环境都相同。则F还能发生的反应是(填序号)
a 加成反应 b 氧化反应 c 加聚反应 d 分解反应
(6)写出树脂X可能的结构简式(写出一种即可)
(7)E的分子式为C10H14O2,含三个甲基,苯环上的一溴代物有两种。生成E的化学方程式是
您最近一年使用:0次
名校
解题方法
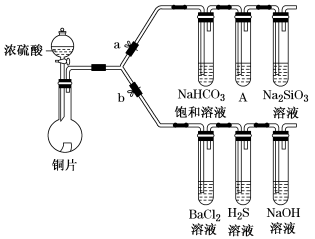
6 . 根据要求完成下列各小题实验目的。(a、b为弹簧夹,加热及固定装置已略去)
① 连接仪器、________ 、加药品后,打开a关闭b,然后滴入浓硫酸,加热。
② 铜与浓硫酸反应的化学方程式是_______ 。装置A中试剂是_______ 。
③ 能说明碳的非金属性比硅强的实验现象是_________ 。
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
① 在(1)①操作后打开b,关闭a。
② H2S溶液中有浅黄色浑浊出现,化学方程式是____ 。
③ BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
写出其中SO2显示还原性生成沉淀的离子方程式_________ 。
① 连接仪器、
② 铜与浓硫酸反应的化学方程式是
③ 能说明碳的非金属性比硅强的实验现象是
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
① 在(1)①操作后打开b,关闭a。
② H2S溶液中有浅黄色浑浊出现,化学方程式是
③ BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 |
您最近一年使用:0次
2020-03-06更新
|
148次组卷
|
6卷引用:山西省实验中学2020届高三化学复习针对性试题集(六)
名校
解题方法
7 . 如图所示2套实验装置,分别回答下列问题。
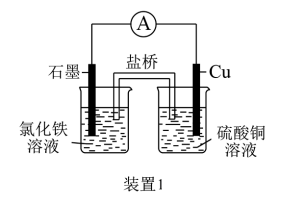
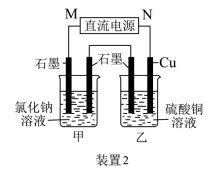
(1)装置1中的Cu是_________ 极(填“正”或“负”),该装置发生的总反应的离子方程式为___________ 。
(2)装置2中甲烧杯盛放100 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5 mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到右边石墨电极附近首先变红,左边石墨电极附近无明显现象。
① 电源的M端为_________ 极,甲烧杯右边石墨电极附近首先变红的原因是___________________ 。
② 乙烧杯中电解反应的离子方程式为____________ 。
③ 若装置甲阴、阳两极各产生112mL气体(标准状况),则装置乙所得溶液的pH为______ (忽略反应前后溶液的体积变化)。


(1)装置1中的Cu是
(2)装置2中甲烧杯盛放100 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5 mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到右边石墨电极附近首先变红,左边石墨电极附近无明显现象。
① 电源的M端为
② 乙烧杯中电解反应的离子方程式为
③ 若装置甲阴、阳两极各产生112mL气体(标准状况),则装置乙所得溶液的pH为
您最近一年使用:0次
名校
解题方法
8 . 四种短周期元素A、B、C、D原子序数依次增大。A、B、C三种元素原子核外电子层数之和是5。A、B两种元素原子最外层电子数之和等于C元素原子最外电子层上的电子数;B元素原子最外电子层上的电子数是它电子层数的2倍,A和C可以形成化合物CA3,B与D的原子序数之比为3∶4。请回答:
(1)化合物CA3的化学式是__________ 。
(2)写出A和C化合生成CA3反应的平衡常数表达式_________ 。在一定条件下要使该反应平衡向右移动,可采取的措施有________ 。
A 缩小反应容器容积 B 增大反应容器容积
C 使用合适的催化剂 D 及时分离出生成物
(3)由四种元素中的三种元素组成的物质甲属于盐类,其水溶液呈酸性,请用离子方程式表示其呈酸性的原因__________ ,若用pH试纸测定0.1 mol/L的甲溶液的pH,实验操作是__________
(4)乙和丙为含有上述四种元素的常见无机盐,二者均既可与盐酸又可与烧碱溶液反应。则乙和丙的化学式为乙:___________ ;丙__________ 。
(5)写出乙溶液与硫酸氢钠溶液反应的离子方程式_________ 。
(1)化合物CA3的化学式是
(2)写出A和C化合生成CA3反应的平衡常数表达式
A 缩小反应容器容积 B 增大反应容器容积
C 使用合适的催化剂 D 及时分离出生成物
(3)由四种元素中的三种元素组成的物质甲属于盐类,其水溶液呈酸性,请用离子方程式表示其呈酸性的原因
(4)乙和丙为含有上述四种元素的常见无机盐,二者均既可与盐酸又可与烧碱溶液反应。则乙和丙的化学式为乙:
(5)写出乙溶液与硫酸氢钠溶液反应的离子方程式
您最近一年使用:0次
2020-03-06更新
|
89次组卷
|
2卷引用:山西省实验中学2020届高三化学复习针对性试题集(二)
名校
9 . A、B、C、D、E是核电荷数依次增大的5种短周期主族元素;原子半径按D、E、B、C、A顺序依次减小,B和E是同主族元素。
(1)下列推断正确的是________ 。
a A、B、E不可能在同一主族
b A、B、C可能在同一周期
c C的最高价氧化物的水化物可能显碱性
d C和D的单质可能生成离子化合物
(2)若A与D同主族,B属非金属元素,它的一种单质是电的良导体,C原子的最外层电子数比A与B的最外层电子数总和还多1。则①A与C元素按原子个数比1:1形成的化合物F的电子式为______ ;F属于__________ 分子(填“极性”或“非极性”)
②由A、B、C、D四元素按原子个数比1:1:3:1形成的化合物为_________ ,它与A、C、D形成的化合物在水溶液中反应的离子方程式为_______ ;
③E在周期表中的位置______ C和E形成的化合物属于_____ 晶体
④由A、B、C元素中的两种或三种可以组成多种分子,其中含有18个电子的分子是____ (填化学式)。
⑤B、C、E氢化物的沸点由高到低为__________ ,试说明原因 _____ 。
(1)下列推断正确的是
a A、B、E不可能在同一主族
b A、B、C可能在同一周期
c C的最高价氧化物的水化物可能显碱性
d C和D的单质可能生成离子化合物
(2)若A与D同主族,B属非金属元素,它的一种单质是电的良导体,C原子的最外层电子数比A与B的最外层电子数总和还多1。则①A与C元素按原子个数比1:1形成的化合物F的电子式为
②由A、B、C、D四元素按原子个数比1:1:3:1形成的化合物为
③E在周期表中的位置
④由A、B、C元素中的两种或三种可以组成多种分子,其中含有18个电子的分子是
⑤B、C、E氢化物的沸点由高到低为
您最近一年使用:0次
名校
10 . W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。回答下列问题:
(1)W、X对应的两种最高价氧化物的水化物可以反应生成盐和水,该反应的离子方程式为______________________________________________________ 。
(2)X的硝酸盐水溶液显______ 性,用离子方程式解释原因______________________ 。
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为____________ 。
(4)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是: > > > 。(填写离子符号)_____________
(5)Z的最高价氧化物为无色液体,0.25mol该物质与一定量水混合得到一种稀溶液,并放出QkJ的热量。写出该反应的热化学方程式:___________________________ 。
(1)W、X对应的两种最高价氧化物的水化物可以反应生成盐和水,该反应的离子方程式为
(2)X的硝酸盐水溶液显
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为
(4)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是: > > > 。(填写离子符号)
(5)Z的最高价氧化物为无色液体,0.25mol该物质与一定量水混合得到一种稀溶液,并放出QkJ的热量。写出该反应的热化学方程式:
您最近一年使用:0次



