名校
1 . 根据实验操作和现象得出的结论不正确 的是
选项 | 实验操作和现象 | 结论 |
A | 红热的铁与水蒸气反应后的固体物质,用稀硫酸溶解,滴入几滴KSCN溶液,未显红色 | 固体物质中可能含有+3价铁元素 |
B | 钠在空气中加热,发生剧烈反应,得到淡黄色固体 | 固体物质中含有 |
C | 用硫酸酸化的 溶液滴入 溶液滴入 溶液中,溶液由绿变黄 溶液中,溶液由绿变黄 |  氧化性比 氧化性比 强 强 |
D | 某溶液中滴加 溶液,出现白色沉淀,再加足量稀 溶液,出现白色沉淀,再加足量稀 ,沉淀不溶解 ,沉淀不溶解 | 溶液中含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-31更新
|
201次组卷
|
2卷引用:浙江省绍兴市第一中学2023-2024学年高一下学期回头考试化学试题
名校
解题方法
2 . 下列实验仪器的名称不正确 的是
A.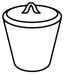 坩埚 坩埚 | B.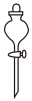 分液漏斗 分液漏斗 |
C.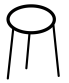 泥三角 泥三角 | D.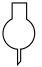 球形干燥管 球形干燥管 |
您最近一年使用:0次
2024-03-25更新
|
128次组卷
|
2卷引用:浙江省浙南名校2023-2024学年高一下学期开学化学试题
3 . 下列说法
| A.门捷列夫在前人研究的基础上,列出了第一张元素周期表 |
B.用激光笔照射 溶液,可产生丁达尔效应 溶液,可产生丁达尔效应 |
C.考古工作者利用 断代法,可对文物进行年代测定 断代法,可对文物进行年代测定 |
| D.回收废旧电池可减少对环境的污染并实现资源的再利用 |
您最近一年使用:0次
名校
4 . 化学能和电能的相互转化应用于各个领域。回答下列问题:
(1)硫酸是铅酸蓄电池的电解质,在铅酸蓄电池中负极的电极反应式是___________ 。
(2)“反应2”是2LiOH+6H2C2O4+2FePO4=2LiFePO4+7CO2↑+5CO↑+7H2O,其中体现氧化性和还原性的反应物的物质的量之比为___________ 。
(3)利用LiFePO4作电极的电池稳定、安全、对环境友好,放电时工作原理如图所示。
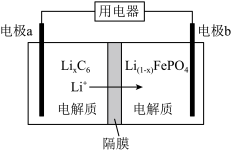
①电极a是该电池的___________ (填“正极”或“负极”),
②充电时电极a的电极反应式为___________ 。
③放电时电极b的电极反应式为___________ 。
(1)硫酸是铅酸蓄电池的电解质,在铅酸蓄电池中负极的电极反应式是
(2)“反应2”是2LiOH+6H2C2O4+2FePO4=2LiFePO4+7CO2↑+5CO↑+7H2O,其中体现氧化性和还原性的反应物的物质的量之比为
(3)利用LiFePO4作电极的电池稳定、安全、对环境友好,放电时工作原理如图所示。

①电极a是该电池的
②充电时电极a的电极反应式为
③放电时电极b的电极反应式为
您最近一年使用:0次
名校
5 . 类推的思维方法在化学学习中应用广泛,但类推出的结论需经过实践的检验才能确定其正确与否。下列几种类推结论错误的是
| A.Al(OH)3能与NaOH溶液反应,则Be(OH)2也能与NaOH溶液反应 |
| B.SO2是“V形”分子,则O3是“V形”分子 |
| C.第二周期元素氢化物稳定性:H2O>HF>NH3,则第三周期元素氢化物稳定性:H2S>HCl>PH3 |
| D.工业制Mg采用电解熔融MgCl2的方法,则工业制Al也可采用电解熔融AlCl3的方法 |
您最近一年使用:0次
名校
解题方法
6 . 下列有关物质的除杂所选试剂或方法不正确 的是
A.除去 固体中少量 固体中少量 :直接加热 :直接加热 |
B.除去 溶液中少量 溶液中少量 :过量铁粉,过滤 :过量铁粉,过滤 |
C.除去 气体中少量 气体中少量 :饱和食盐水、浓硫酸,洗气 :饱和食盐水、浓硫酸,洗气 |
D.除去 气体中少量 气体中少量 :过量 :过量 ,点燃 ,点燃 |
您最近一年使用:0次
2024-03-15更新
|
183次组卷
|
2卷引用:浙江省浙南名校2023-2024学年高一下学期开学化学试题
7 . 已知25℃时,醋酸、碳酸、氢氰酸的电离平衡常数如下表:
回答下列问题:
(1)25℃时,pH相等的三种溶液①CH3COONa溶液、②Na2CO3溶液、③NaCN溶液,浓度由大到小的顺序为___________ (填序号)。
(2)25℃时,向NaCN溶液中通入少量CO2,反应的离子方程式为___________ 。
(3)将浓度为0.02mol·L-1的HCN与0.01 mol·L-1NaOH溶液等体积混合,则混合溶液中c(H+ )___________ c(OH- )(填“>”、“<”或 “=”)。
(4)常温下,向浓度为0.1mol·L-1、体积为V L的氨水中逐滴加入 一定浓度的盐酸,用pH计测溶液的pH,变化曲线如图所示,d点两种溶液恰好完全反应。根据图中信息回答下列问题:
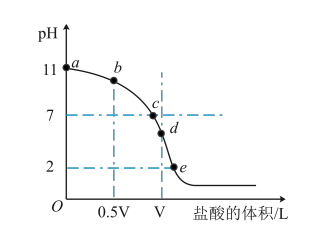
①该温度时NH3·H2O的电离常数Kb≈___________ ;
②b、c、d三点的溶液中,由水电离出的c(H+)由大到小的顺序为___________ ;
③根据以上滴定曲线判断点d所示溶液中:c(Cl-)= c(NH3·H2O)+___________ 。
| 化学式 | CH3COOH | H2CO3 | HCN |
| 电离平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=6.2×10-10 |
(1)25℃时,pH相等的三种溶液①CH3COONa溶液、②Na2CO3溶液、③NaCN溶液,浓度由大到小的顺序为
(2)25℃时,向NaCN溶液中通入少量CO2,反应的离子方程式为
(3)将浓度为0.02mol·L-1的HCN与0.01 mol·L-1NaOH溶液等体积混合,则混合溶液中c(H+ )
(4)常温下,向浓度为0.1mol·L-1、体积为V L的氨水中逐滴加入 一定浓度的盐酸,用pH计测溶液的pH,变化曲线如图所示,d点两种溶液恰好完全反应。根据图中信息回答下列问题:

①该温度时NH3·H2O的电离常数Kb≈
②b、c、d三点的溶液中,由水电离出的c(H+)由大到小的顺序为
③根据以上滴定曲线判断点d所示溶液中:c(Cl-)= c(NH3·H2O)+
您最近一年使用:0次
名校
8 . CH4还原CO2是实现“双碳”经济的有效途径之一,相关的主要反应有:
I.CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH1=+247 kJ·mol-1,
2CO(g)+2H2(g) ΔH1=+247 kJ·mol-1,
Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=+41 kJ·mol-1,
CO(g)+H2O(g) ΔH2=+41 kJ·mol-1,
Ⅲ.CO2(g)+H2(g) HCOOH(g) ΔH3<0
HCOOH(g) ΔH3<0
请回答:
(1)仅考虑反应I、Ⅱ,有利于提高CO2平衡转化率的条件是___________。
(2)反应CH4(g)+3CO2(g) 4CO(g)+2H2O(g)的ΔH=
4CO(g)+2H2O(g)的ΔH=___________ kJ·mol-1;
(3)在某恒温、恒容的密闭容器中仅发生反应Ⅲ,CO2和H2的投料浓度均为1.0 mol·L−1,平衡常数K=2.4×10−8,则CO2的平衡转化率为___________ 。
(4)用氨水吸收HCOOH,得到1.00 mol·L−1氨水和0.18 mol·L−1甲酸铵的混合溶液,298 K时该混合溶液的pH=___________ 。 [已知:298 K时,电离常数 Kb(NH3·H2O)=1.8×10−5、 Ka(HCOOH)=1.8×10−4 ]
(5)在3.0MPa,有催化剂的条件下,向密闭容器中充入1molCO2和3molH2,发生反应Ⅱ、Ⅲ,CO2的平衡转化率与HCOOH、CO的选择性随温度的变化如图所示。
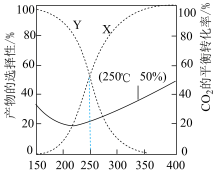
①图中Y曲线代表___________ (填化学式)的选择性。
②CO2的平衡转化率在250℃以后随温度升高而变大的原因:___________ 。
I.CH4(g)+CO2(g)
 2CO(g)+2H2(g) ΔH1=+247 kJ·mol-1,
2CO(g)+2H2(g) ΔH1=+247 kJ·mol-1,Ⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2=+41 kJ·mol-1,
CO(g)+H2O(g) ΔH2=+41 kJ·mol-1, Ⅲ.CO2(g)+H2(g)
 HCOOH(g) ΔH3<0
HCOOH(g) ΔH3<0请回答:
(1)仅考虑反应I、Ⅱ,有利于提高CO2平衡转化率的条件是___________。
| A.低温低压 | B.低温高压 | C.高温低压 | D.高温高压 |
(2)反应CH4(g)+3CO2(g)
 4CO(g)+2H2O(g)的ΔH=
4CO(g)+2H2O(g)的ΔH=(3)在某恒温、恒容的密闭容器中仅发生反应Ⅲ,CO2和H2的投料浓度均为1.0 mol·L−1,平衡常数K=2.4×10−8,则CO2的平衡转化率为
(4)用氨水吸收HCOOH,得到1.00 mol·L−1氨水和0.18 mol·L−1甲酸铵的混合溶液,298 K时该混合溶液的pH=
(5)在3.0MPa,有催化剂的条件下,向密闭容器中充入1molCO2和3molH2,发生反应Ⅱ、Ⅲ,CO2的平衡转化率与HCOOH、CO的选择性随温度的变化如图所示。

①图中Y曲线代表
②CO2的平衡转化率在250℃以后随温度升高而变大的原因:
您最近一年使用:0次
名校
解题方法
9 . 糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是
| A.脱氧过程是吸热反应,可降低温度,延长糕点保质期 |
| B.脱氧过程中铁的电极反应为:Fe - 3e- = Fe3+ |
| C.脱氧过程中碳做原电池负极 |
| D.含有0.1 mol铁粉的脱氧剂,理论上最多能吸收氧气0.075 mol |
您最近一年使用:0次
名校
10 . CH3COOH与CH3COONa等物质的量混合配制成的稀溶液,pH=4.7,下列说法或离子浓度关系正确的是
| A.CH3COONa的水解程度大于CH3COOH的电离程度 |
| B.CH3COONa的存在抑制了CH3COOH的电离 |
| C.c(CH3COO-)>c(Na+)>c(OH-)> c(H+) |
| D.c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+) |
您最近一年使用:0次



