2025高三·全国·专题练习
解题方法
1 . 根据信息书写方程式或描述反应过程。
(1)BMO(Bi2MoO6)是一种高效光催化剂,可用于光催化降解苯酚,弱酸性条件下降解苯酚的反应原理如下图所示。___________ 。
②写出 与苯酚反应的离子方程式:
与苯酚反应的离子方程式:___________ 。
(2)氯化银可以溶于氨水中,写出该反应的离子方程式:___________ 。
(1)BMO(Bi2MoO6)是一种高效光催化剂,可用于光催化降解苯酚,弱酸性条件下降解苯酚的反应原理如下图所示。
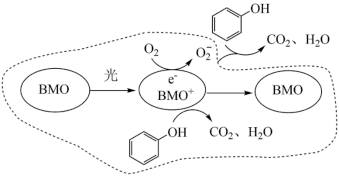
②写出
 与苯酚反应的离子方程式:
与苯酚反应的离子方程式:(2)氯化银可以溶于氨水中,写出该反应的离子方程式:
您最近一年使用:0次
2025高三·全国·专题练习
解题方法
2 .  有较强的配位能力,许多金属离子都可以与
有较强的配位能力,许多金属离子都可以与 形成稳定的配合。反应
形成稳定的配合。反应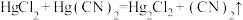 用于制备
用于制备 。
。
(1)上述反应的氧化剂是___________ 。
(2)写出 的结构简式
的结构简式___________ , 的空间构型是
的空间构型是___________ ;1mol 分子中
分子中 键为
键为___________ mol。
(3) 被称为拟卤素,性质与卤素相似,写出
被称为拟卤素,性质与卤素相似,写出 与氢氧化钠溶液反应的离子方程式
与氢氧化钠溶液反应的离子方程式___________ 。
(4)基态N价层电子排布式为___________ 。
 有较强的配位能力,许多金属离子都可以与
有较强的配位能力,许多金属离子都可以与 形成稳定的配合。反应
形成稳定的配合。反应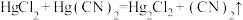 用于制备
用于制备 。
。(1)上述反应的氧化剂是
(2)写出
 的结构简式
的结构简式 的空间构型是
的空间构型是 分子中
分子中 键为
键为(3)
 被称为拟卤素,性质与卤素相似,写出
被称为拟卤素,性质与卤素相似,写出 与氢氧化钠溶液反应的离子方程式
与氢氧化钠溶液反应的离子方程式(4)基态N价层电子排布式为
您最近一年使用:0次
2025高三·全国·专题练习
3 . 回答下列问题。
(1)某氯原子的质量是a g,12C原子的质量是b g,用NA表示阿伏加德罗常数的值。
①该氯原子的相对原子质量为___________ ;
②该氯原子的摩尔质量是___________ ;
③m g该氯原子的物质的量为___________ ;
④n g该氯原子所含的电子数为___________ 。
(2)12.4 g Na2R含Na+ 0.4 mol,则Na2R的摩尔质量为___________ ,R的相对原子质量为___________ 。含R的质量为1.6 g的Na2R,其物质的量为___________ 。
(1)某氯原子的质量是a g,12C原子的质量是b g,用NA表示阿伏加德罗常数的值。
①该氯原子的相对原子质量为
②该氯原子的摩尔质量是
③m g该氯原子的物质的量为
④n g该氯原子所含的电子数为
(2)12.4 g Na2R含Na+ 0.4 mol,则Na2R的摩尔质量为
您最近一年使用:0次
2025高三上·全国·专题练习
4 . 一块表面已被氧化为氧化钠的钠块17.0 g,投入50 g水中,最多能产生0.2 g气体,则:
(1)涉及的化学方程式为_______ ,_______ 。
(2)钠块中钠的质量是_______ g。
(3)钠块中氧化钠的质量是_______ g。
(4)原来钠块中被氧化的钠的质量是_______ g。
(5)设所得溶液的体积为50 mL,求所得溶液溶质物质的量浓度是_______ 。
(1)涉及的化学方程式为
(2)钠块中钠的质量是
(3)钠块中氧化钠的质量是
(4)原来钠块中被氧化的钠的质量是
(5)设所得溶液的体积为50 mL,求所得溶液溶质物质的量浓度是
您最近一年使用:0次
2025高三上·全国·专题练习
5 . 某消毒小组人员用18.4mol•L-1的浓硫酸配制500mL0.1mol•L-1的稀硫酸用于84消毒液消毒能力的实验探究,在配制过程中,下列操作中能使所配溶液的浓度偏低的有___________ (填代号)。
①用量筒量取98%的硫酸时俯视
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④转移过程中,有少量液体溅出
⑤定容时,加蒸馏水超过标线,又用胶头滴管吸出
①用量筒量取98%的硫酸时俯视
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④转移过程中,有少量液体溅出
⑤定容时,加蒸馏水超过标线,又用胶头滴管吸出
您最近一年使用:0次
2025高三·全国·专题练习
解题方法
6 . 请回答下列问题:
(1)重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeO·Cr2O3,还含有硅、铝等杂质:
铬铁矿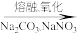 熔块
熔块
该步骤的主要反应为FeO·Cr2O3+Na2CO3+NaNO3 Na2CrO4+Fe2O3+CO2↑+NaNO2。上述反应配平后FeO·Cr2O3与NaNO3的化学计量数比为
Na2CrO4+Fe2O3+CO2↑+NaNO2。上述反应配平后FeO·Cr2O3与NaNO3的化学计量数比为___________ 。
(2)酸性条件下,MnO(OH)2将I-氧化为I2:MnO(OH)2+I-+H+→Mn2++I2+H2O(未配平)。配平该反应的方程式,其化学计量数依次为___________ 。
(1)重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeO·Cr2O3,还含有硅、铝等杂质:
铬铁矿
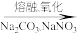 熔块
熔块该步骤的主要反应为FeO·Cr2O3+Na2CO3+NaNO3
 Na2CrO4+Fe2O3+CO2↑+NaNO2。上述反应配平后FeO·Cr2O3与NaNO3的化学计量数比为
Na2CrO4+Fe2O3+CO2↑+NaNO2。上述反应配平后FeO·Cr2O3与NaNO3的化学计量数比为(2)酸性条件下,MnO(OH)2将I-氧化为I2:MnO(OH)2+I-+H+→Mn2++I2+H2O(未配平)。配平该反应的方程式,其化学计量数依次为
您最近一年使用:0次
23-24高一下·全国·期末
7 . 回答下列问题:
(1)用20% H2SO4浸取软锰矿(主要成分为MnO2、SiO2等)制备高纯MnO2,酸浸时,通常加入FeSO4作催化剂加快反应速率。为提高酸浸速率,还可以采取的措施有______________ (写一种)。
(2)工业上用稀硫酸浸取碳酸锰矿(主要成分为MnCO3,另含FeO、Fe2O3、CaO等杂质)生产锰酸锂(LiMn2O4),为了提高碳酸锰矿浸出的速率,在“酸浸”时可采取的措施有:①适当升高温度;②搅拌;③_______________ 等。
(3)用NaOH熔盐高钛渣(主要成分为Ti3O5,含少量SiO2、FeO、Fe2O3)制备白色颜料TiO2,为加快反应速率,在维持反应物颗粒大小、反应温度一定的条件下,可采取的措施是________________ 。
(1)用20% H2SO4浸取软锰矿(主要成分为MnO2、SiO2等)制备高纯MnO2,酸浸时,通常加入FeSO4作催化剂加快反应速率。为提高酸浸速率,还可以采取的措施有
(2)工业上用稀硫酸浸取碳酸锰矿(主要成分为MnCO3,另含FeO、Fe2O3、CaO等杂质)生产锰酸锂(LiMn2O4),为了提高碳酸锰矿浸出的速率,在“酸浸”时可采取的措施有:①适当升高温度;②搅拌;③
(3)用NaOH熔盐高钛渣(主要成分为Ti3O5,含少量SiO2、FeO、Fe2O3)制备白色颜料TiO2,为加快反应速率,在维持反应物颗粒大小、反应温度一定的条件下,可采取的措施是
您最近一年使用:0次
8 . 物质的结构决定物质的性质。请回答下列涉及物质结构和性质的问题:
(1)第三周期元素I1变化规律如图所示,第三周期元素中I1处于Al与P之间的元素符号是___________ 。___________ 。
(3)已知固态HF、H2O、NH3的氢键键能和结构如下:
___________ 个水分子包围形成___________ 构型。
(4)碳化硅的结构与金刚石类似(如图所示),其硬度仅次于金刚石,具有较强的耐磨性能。碳化硅晶胞结构中每个碳原子周围与其距离最近的硅原子有___________ 个。
(1)第三周期元素I1变化规律如图所示,第三周期元素中I1处于Al与P之间的元素符号是

(3)已知固态HF、H2O、NH3的氢键键能和结构如下:
| 物质 | 氢键X-H···Y | 氢键键能kJ·mol-1 |
| (HF)n | F-H···F | 28.1 |
| 冰 | O-H···O | 18.8 |
| (NH3)n | N-H···N | 5.4 |

(4)碳化硅的结构与金刚石类似(如图所示),其硬度仅次于金刚石,具有较强的耐磨性能。碳化硅晶胞结构中每个碳原子周围与其距离最近的硅原子有

您最近一年使用:0次
23-24高二下·全国·期末
解题方法
9 . 已知某些共价键的键能、键长数据如表所示:
(1)下列推断正确的是___________(填字母,下同)。
(2)在HX(X=F、Cl、Br、I)分子中,键长最短的是___________ ,最长的是___________ ;O—O的键长___________ (填“大于”“小于”或“等于”)O=O的键长。
| 共价键 | Cl—Cl | Br—Br | I—I | H—F | H—Cl | H—Br | H—I | H—O |
| 键能/(kJ·mol-1) | 242.7 | 193.7 | 152.7 | 568 | 431.8 | 366 | 298.7 | 462.8 |
| 键长/pm | 198 | 228 | 267 | 96 | ||||
| 共价键 | C—C | C=C | C≡C | C—H | N—H | N=O | O—O | O=O |
| 键能/(kJ·mol-1) | 347.7 | 615 | 812 | 413.4 | 390.8 | 607 | 142 | 497.3 |
| 键长/pm | 154 | 133 | 120 | 109 | 101 |
| A.热稳定性:HF>HCl>HBr>HI |
| B.氧化性:I2>Br2>Cl2 |
| C.沸点:H2O>NH3 |
| D.还原性:HI>HBr>HCl>HF |
您最近一年使用:0次
23-24高一下·全国·课前预习
解题方法
10 . “乙醇燃料电池”的工作原理为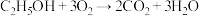 ,装置如图所示。
,装置如图所示。 的移动方向为由
的移动方向为由_______ (填“A到B”或“B到A”)。写出A电极的电极反应式:_____________ 。
②若标况下有11.2L 参与反应,理论上通过质子交换膜的
参与反应,理论上通过质子交换膜的 数目为
数目为_______ 。
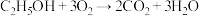 ,装置如图所示。
,装置如图所示。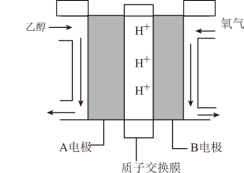
 的移动方向为由
的移动方向为由②若标况下有11.2L
 参与反应,理论上通过质子交换膜的
参与反应,理论上通过质子交换膜的 数目为
数目为
您最近一年使用:0次



