名校
1 . 根据原电池原理,人们研制出了性能各异的化学电池。
(1)某兴趣小组同学用大小相同的铜片和锌片作电极研究水果电池,如图所示:__________ 。负极材料是__________ ,负极反应式为____________________ 。
②该电池工作时,下列说法错误的是__________ (填字母)。
A.锌片的质量减小
B.电流由铜片经LED灯流向锌片
C.化学能全部转化为电能
D.发生了氧化还原反应
③若将锌片和铜片从柠檬中拿出,用蒸馏水洗净干燥后相互接触,LED灯__________ (填“会”或“不会”)亮,原因是____________________________________________________________ 。
(2)某锂-空气电池的总反应为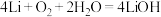 ,其工作原理示意图如图所示:
,其工作原理示意图如图所示: 发生
发生__________ (填“氧化”或“还原”)反应。
②锂离子向电池__________ (填“正”或“负”)极移动。
③石墨电极__________ (填“参与”或“不参与”)电极反应。
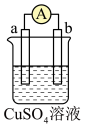
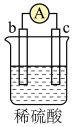
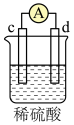
(3)现有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下表所示:
由上表可判断a、b、c、d四种金属的活动性由大到小排列为__________ (填字母)。
(1)某兴趣小组同学用大小相同的铜片和锌片作电极研究水果电池,如图所示:

②该电池工作时,下列说法错误的是
A.锌片的质量减小
B.电流由铜片经LED灯流向锌片
C.化学能全部转化为电能
D.发生了氧化还原反应
③若将锌片和铜片从柠檬中拿出,用蒸馏水洗净干燥后相互接触,LED灯
(2)某锂-空气电池的总反应为
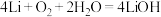 ,其工作原理示意图如图所示:
,其工作原理示意图如图所示:
 发生
发生②锂离子向电池
③石墨电极
(3)现有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下表所示:
实验装置 |
|
|
|
|
部分实验现象 | b极质量增大 | 外电路电流 从a流向d | c极上有气泡产生 | d极溶解 |
您最近一年使用:0次
2 . 回答下列问题。
I.含铁元素的物质在人类的生产和生活中有着重要应用。有下列4种含铁化合物:
A.Fe(OH)2 B.Fe2O3 C.FeSO4 D. Fe3O4
(1)可用作红色颜料的是_______ (填字母代号,下同);
(2)具有磁性的黑色晶体是_______ ;
(3)在空气中迅速变为灰绿色,最后变为红褐色的是_______ ;
(4)可用于治疗缺铁性贫血的是_______ 。
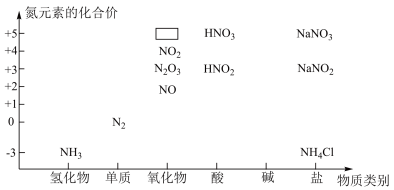
II.物质类别和元素价态是学习元素及其化合物性质的重要认识视角。下图是氮及其化合物的“价一类”二维图:
(5)图中所示变化中,涉及氮的固定的是_______ (填数字序号)。
(6)图中物质为红棕色气体的是_______ (填名称或化学式)。
(7)图中所示变化中,属于非氧化还原反应的是_______ (填数字序号)。
(8)图中气体A遇到氯化氢出现白烟,反应的化学方程式为_______ 。
I.含铁元素的物质在人类的生产和生活中有着重要应用。有下列4种含铁化合物:
A.Fe(OH)2 B.Fe2O3 C.FeSO4 D. Fe3O4
(1)可用作红色颜料的是
(2)具有磁性的黑色晶体是
(3)在空气中迅速变为灰绿色,最后变为红褐色的是
(4)可用于治疗缺铁性贫血的是
II.物质类别和元素价态是学习元素及其化合物性质的重要认识视角。下图是氮及其化合物的“价一类”二维图:
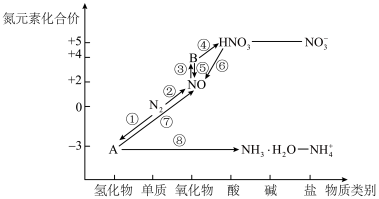
(5)图中所示变化中,涉及氮的固定的是
(6)图中物质为红棕色气体的是
(7)图中所示变化中,属于非氧化还原反应的是
(8)图中气体A遇到氯化氢出现白烟,反应的化学方程式为
您最近一年使用:0次
3 . 按要求回答下列问题:
(1)写出下列有机物的系统命名或结构简式______ 。
④2,5—二甲基—4—乙基庚烷______ 。
(2)写出下列有关反应的化学方程式
①丙烯一定条件下可制得2—丙醇:____________ 。
②由甲苯制TNT炸药:______ 。
③异戊二烯一定条件下可制得聚异戊二烯橡胶:______ 。
④甲苯光照条件下与氯气生成一氯代物:______ 。
(1)写出下列有机物的系统命名或结构简式
①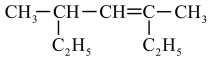
②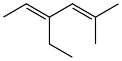
④2,5—二甲基—4—乙基庚烷
(2)写出下列有关反应的化学方程式
①丙烯一定条件下可制得2—丙醇:
②由甲苯制TNT炸药:
③异戊二烯一定条件下可制得聚异戊二烯橡胶:
④甲苯光照条件下与氯气生成一氯代物:
您最近一年使用:0次
解题方法
4 . 中国高铁对实现“一带一路”的倡议有重要的作用。
(1)高铁上的信息传输系统使用了光导纤维,其主要成分是______ ;乘务员使用的无线通话机的芯片材料是______ 。
(2)SiO2是一种酸性氧化物,能与强碱溶液反应。例如,SiO2与NaOH反应可生成 。
。 的水溶液俗称水玻璃,具有黏结力强、耐高温等特性,可以用作黏合剂和防火剂。请写出相关反应的化学方程式
的水溶液俗称水玻璃,具有黏结力强、耐高温等特性,可以用作黏合剂和防火剂。请写出相关反应的化学方程式______ 。
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与玻璃中的二氧化硅反应的化学方程式为______ 。
(4)氮化硅(Si3N4)可由石英与焦炭在高温的氮气流中通过以下反应制备: 。
。
①以及以上反应中的氧化剂______ ,还原剂 ______ 。
②若该反应生成67.2L一氧化碳(标准状况),则生成氮化硅的质量_______ g。
(1)高铁上的信息传输系统使用了光导纤维,其主要成分是
(2)SiO2是一种酸性氧化物,能与强碱溶液反应。例如,SiO2与NaOH反应可生成
 。
。 的水溶液俗称水玻璃,具有黏结力强、耐高温等特性,可以用作黏合剂和防火剂。请写出相关反应的化学方程式
的水溶液俗称水玻璃,具有黏结力强、耐高温等特性,可以用作黏合剂和防火剂。请写出相关反应的化学方程式(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与玻璃中的二氧化硅反应的化学方程式为
(4)氮化硅(Si3N4)可由石英与焦炭在高温的氮气流中通过以下反应制备:
 。
。①以及以上反应中的氧化剂
②若该反应生成67.2L一氧化碳(标准状况),则生成氮化硅的质量
您最近一年使用:0次
解题方法
5 . 下图是氮的化合物的“价类二维图”。______ ,该物质的电子式_____ 。
(2)写出实验室制取氨气的化学方程式:______ 。
(3)实验室中硝酸通常保存在棕色瓶中,硝酸保存在棕色瓶中的原因:____ (请用方程式解释。)
(4)使用浓硝酸进行实验:反应剧烈进行,铜丝逐渐变细,溶液变绿,试管上方出现红棕色气体。铜与浓硝酸反应的化学方程式为_____ ;以上反应中酸性与氧化性硝酸的物质的量之比_____ 。
(5)工业生产中为了盛装大量浓硝酸,可选择_____ 作为罐体材料。
a.铜 b.铝 c.铂 d.镁
(2)写出实验室制取氨气的化学方程式:
(3)实验室中硝酸通常保存在棕色瓶中,硝酸保存在棕色瓶中的原因:
(4)使用浓硝酸进行实验:反应剧烈进行,铜丝逐渐变细,溶液变绿,试管上方出现红棕色气体。铜与浓硝酸反应的化学方程式为
(5)工业生产中为了盛装大量浓硝酸,可选择
a.铜 b.铝 c.铂 d.镁
您最近一年使用:0次
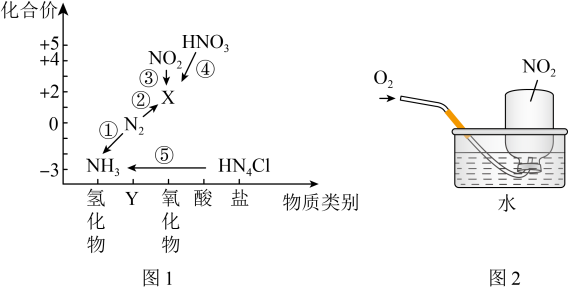
6 . 氮元素是高中化学学习的一种重要非金属元素,其价类二维图如图1所示。________ ,反应①~⑤中不属于氧化还原反应的是________ (填序号)。
(2)反应①中每消耗1mol氢气,转移电子________ mol。
(3)除去X中混有的少量 的方法是
的方法是________ 。
(4)工业以氨气为原料制备硝酸的第一步反应为氨的催化氧化,写出该反应的化学方程式________ 。
(5)用集气瓶收集 气体并倒置在水槽中,然后缓慢通入适量
气体并倒置在水槽中,然后缓慢通入适量 ,如图2所示。一段时间后,集气瓶中充满溶液。
,如图2所示。一段时间后,集气瓶中充满溶液。
①写出该过程总反应的化学方程式________ 。该实验对工业上生产硝酸的启示是________ 。
②假设该实验条件下,气体摩尔体积为 ,瓶内液体不扩散,则集气瓶中溶液的物质的量浓度为
,瓶内液体不扩散,则集气瓶中溶液的物质的量浓度为________ mol/L。
(2)反应①中每消耗1mol氢气,转移电子
(3)除去X中混有的少量
 的方法是
的方法是(4)工业以氨气为原料制备硝酸的第一步反应为氨的催化氧化,写出该反应的化学方程式
(5)用集气瓶收集
 气体并倒置在水槽中,然后缓慢通入适量
气体并倒置在水槽中,然后缓慢通入适量 ,如图2所示。一段时间后,集气瓶中充满溶液。
,如图2所示。一段时间后,集气瓶中充满溶液。①写出该过程总反应的化学方程式
②假设该实验条件下,气体摩尔体积为
 ,瓶内液体不扩散,则集气瓶中溶液的物质的量浓度为
,瓶内液体不扩散,则集气瓶中溶液的物质的量浓度为
您最近一年使用:0次
解题方法
7 . 世界卫生组织将 定为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有广泛应用。
定为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有广泛应用。
(1) 的摩尔质量为
的摩尔质量为__________________ 。
(2)制备 的一种反应为:
的一种反应为: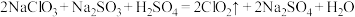 ,用单线桥法标出其电子转移的方向和数目
,用单线桥法标出其电子转移的方向和数目__________________________________ 。
(3) 可将废水中的
可将废水中的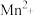 转化为
转化为 而除去,本身被还原为
而除去,本身被还原为 ,该反应中氧化产物和还原产物的物质的量之比是
,该反应中氧化产物和还原产物的物质的量之比是________________ 。
(4)一种“二氧化氧泡腾片”有效成分为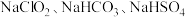 ,该泡腾片能快速溶击水产生大量
,该泡腾片能快速溶击水产生大量 ,同时
,同时 在酸性条件下发生自身氧化还原反应,得到
在酸性条件下发生自身氧化还原反应,得到 溶液。
溶液。
①上述过程中产生大量 的离子方程式为
的离子方程式为__________________ 。
②上述过程生成 离子方程式为
离子方程式为___________________ 。
③消毒效率是用单位质量的消毒剂得电子数来表示的, 作消毒剂时和氯气一样,还原产物均为
作消毒剂时和氯气一样,还原产物均为 ,计
,计 的消毒效率是氯气的
的消毒效率是氯气的_______ 倍(结果保留两位小数)。
 定为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有广泛应用。
定为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有广泛应用。(1)
 的摩尔质量为
的摩尔质量为(2)制备
 的一种反应为:
的一种反应为: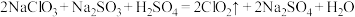 ,用单线桥法标出其电子转移的方向和数目
,用单线桥法标出其电子转移的方向和数目(3)
 可将废水中的
可将废水中的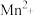 转化为
转化为 而除去,本身被还原为
而除去,本身被还原为 ,该反应中氧化产物和还原产物的物质的量之比是
,该反应中氧化产物和还原产物的物质的量之比是(4)一种“二氧化氧泡腾片”有效成分为
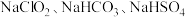 ,该泡腾片能快速溶击水产生大量
,该泡腾片能快速溶击水产生大量 ,同时
,同时 在酸性条件下发生自身氧化还原反应,得到
在酸性条件下发生自身氧化还原反应,得到 溶液。
溶液。①上述过程中产生大量
 的离子方程式为
的离子方程式为②上述过程生成
 离子方程式为
离子方程式为③消毒效率是用单位质量的消毒剂得电子数来表示的,
 作消毒剂时和氯气一样,还原产物均为
作消毒剂时和氯气一样,还原产物均为 ,计
,计 的消毒效率是氯气的
的消毒效率是氯气的
您最近一年使用:0次
解题方法
8 . 电化学原理在污染治理方面有着重要的作用。回答下列问题:
I.煤在直接燃烧前要进行脱硫处理。采用电解法脱硫的基本原理如图所示:
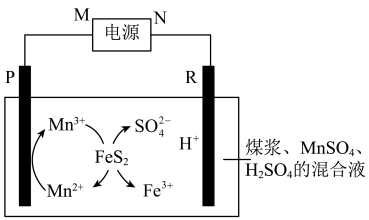
已知:两电极为完全相同的惰性电极。
(1)M为电源的___________ 极。
(2)电解池工作时,观察到R电极上有无色气体产生,写出电极反应式___________ 。
(3)电解池工作时,混合液中 的物质的量
的物质的量___________ (填“变大”、“变小”或“不变”)。
(4)电解过程中,混合溶液中的pH将___________ (填“变大”、“变小”或“不变”),理由是___________ 。
II.电解还原法处理酸性含铬废水:以铁板做阴、阳极,电解含铬废水,示意如图:
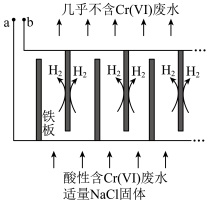
(5)酸性废水中的 在该电池中发生的离子反应方程式为
在该电池中发生的离子反应方程式为___________ 。
(6)为了使 和
和 转化为
转化为 和
和 沉淀,向反应后的溶液中加入一定量的烧碱,若溶液中
沉淀,向反应后的溶液中加入一定量的烧碱,若溶液中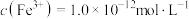 ,则溶液中
,则溶液中
___________  。{已知
。{已知 ,
,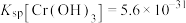 }
}
(7)随着电解的进行,阳极铁板会发生钝化,表面形成 的钝化膜,使电解池不能正常工作。将阴极铁板与阳极铁板交换使用,一段时间后,钝化膜消失,结合有关反应,解释钝化膜消失的原因:
的钝化膜,使电解池不能正常工作。将阴极铁板与阳极铁板交换使用,一段时间后,钝化膜消失,结合有关反应,解释钝化膜消失的原因:___________ 。
I.煤在直接燃烧前要进行脱硫处理。采用电解法脱硫的基本原理如图所示:

已知:两电极为完全相同的惰性电极。
(1)M为电源的
(2)电解池工作时,观察到R电极上有无色气体产生,写出电极反应式
(3)电解池工作时,混合液中
 的物质的量
的物质的量(4)电解过程中,混合溶液中的pH将
II.电解还原法处理酸性含铬废水:以铁板做阴、阳极,电解含铬废水,示意如图:

(5)酸性废水中的
 在该电池中发生的离子反应方程式为
在该电池中发生的离子反应方程式为(6)为了使
 和
和 转化为
转化为 和
和 沉淀,向反应后的溶液中加入一定量的烧碱,若溶液中
沉淀,向反应后的溶液中加入一定量的烧碱,若溶液中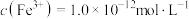 ,则溶液中
,则溶液中
 。{已知
。{已知 ,
,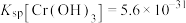 }
}(7)随着电解的进行,阳极铁板会发生钝化,表面形成
 的钝化膜,使电解池不能正常工作。将阴极铁板与阳极铁板交换使用,一段时间后,钝化膜消失,结合有关反应,解释钝化膜消失的原因:
的钝化膜,使电解池不能正常工作。将阴极铁板与阳极铁板交换使用,一段时间后,钝化膜消失,结合有关反应,解释钝化膜消失的原因:
您最近一年使用:0次
9 . 按要求完成下题。
(1)写出H2S的电离方程式:______ 。
(2)0.1mol/LNa2CO3溶液中各离子浓度大小顺序为______ 。
(3)pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,所得溶液显______ 性。
(4)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是______ 。
(5)常温下,NaCN溶液的pH>7,原因是______ (离子反应方程式)。
(6)常温下,pH=10的CH3COONa溶液中,由水电离出的c(OH-)=______ mol/L。
(7)常温下,0.05mol/LH2SO4溶液的pH=______ 。
(1)写出H2S的电离方程式:
(2)0.1mol/LNa2CO3溶液中各离子浓度大小顺序为
(3)pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,所得溶液显
(4)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是
(5)常温下,NaCN溶液的pH>7,原因是
(6)常温下,pH=10的CH3COONa溶液中,由水电离出的c(OH-)=
(7)常温下,0.05mol/LH2SO4溶液的pH=
您最近一年使用:0次
解题方法
10 . 回答下列问题:
(1)实验室配制FeSO4溶液,溶解时先要加入少量的稀硫酸,其原因是
(2)下列盐溶液中能发生水解,
①Na2CO3
②(NH4)2SO4
③泡沫灭火器里盛有Al2(SO4)3溶液和NaHCO3溶液,当灭火时,这两种溶液混合立即喷出大量泡沫,写出水解离子方程式
(3)物质的量浓度均为0.1mol/L的下列溶液:①KNO3、②K2CO3、③KHCO3、④H2SO4、⑤CH3COOH、⑥NaOH、⑦Ba(OH)2,pH由大到小的顺序为:
(4)写出NH4Cl溶液中各
您最近一年使用:0次