名校
1 . 正极材料为LiCoO2的锂离子电池已被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。
(1)橄榄石型LiFePO4是一种潜在的锂离子电池正极材料,它可以通过(NH4)2Fe(SO4)2、H3PO4与LiOH溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得。
①共沉淀反应除了得到LiFePO4外,还有另外一种酸式盐产物,请写出共沉淀的化学方程式为_______ 。
②高温成型前,常向LiFePO4中加入少量活性炭黑,其作用除了可以改善诚信后的LiFePO4的导电性能外,还能_______ 。
(2)废旧锂离子电池的正极材料试样(主要含有LiCoO2及少量Al、Fe等)可通过下列实验方法回收钴、锂。

①在上述溶解过程中,S2O 被氧化成SO
被氧化成SO ,LiCoO2在溶解过程中反应的化学方程式为
,LiCoO2在溶解过程中反应的化学方程式为_______ 。
②已知Co的氧化物与Fe的氧化物类似。Co(OH)2在空气中加热时,固体残留率随温度的变化如图所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体的成分为_______ (填化学式),在350~400℃范围内,剩余固体的成分为_______ (填化学式)。

(1)橄榄石型LiFePO4是一种潜在的锂离子电池正极材料,它可以通过(NH4)2Fe(SO4)2、H3PO4与LiOH溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得。
①共沉淀反应除了得到LiFePO4外,还有另外一种酸式盐产物,请写出共沉淀的化学方程式为
②高温成型前,常向LiFePO4中加入少量活性炭黑,其作用除了可以改善诚信后的LiFePO4的导电性能外,还能
(2)废旧锂离子电池的正极材料试样(主要含有LiCoO2及少量Al、Fe等)可通过下列实验方法回收钴、锂。

①在上述溶解过程中,S2O
 被氧化成SO
被氧化成SO ,LiCoO2在溶解过程中反应的化学方程式为
,LiCoO2在溶解过程中反应的化学方程式为②已知Co的氧化物与Fe的氧化物类似。Co(OH)2在空气中加热时,固体残留率随温度的变化如图所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体的成分为

您最近一年使用:0次
2023-04-26更新
|
179次组卷
|
2卷引用:北京市中国人民大学附属中学2020届高三化学质检试题
名校
2 . 向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:
(1)写出并配平CCl4层由紫色变成无色的化学反应方程式_______ (如果系数是1,不用填写):

(2)整个过程中的还原剂是_______ 。
(3)把KI换成KBr,则CCl4层变为_______ 色,继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是_______ 。
(4)加碘盐中含碘量为20mg~50mg/kg。制取加碘盐(含KIO3的食盐)500kg,若用KI与Cl2反应制KIO3,至少需要消耗Cl2_______ L(标准状况,保留2位小数)。
(1)写出并配平CCl4层由紫色变成无色的化学反应方程式

(2)整个过程中的还原剂是
(3)把KI换成KBr,则CCl4层变为
(4)加碘盐中含碘量为20mg~50mg/kg。制取加碘盐(含KIO3的食盐)500kg,若用KI与Cl2反应制KIO3,至少需要消耗Cl2
您最近一年使用:0次
2023-04-26更新
|
297次组卷
|
3卷引用:北京市中国人民大学附属中学2020届高三化学质检试题
名校
3 . 制取纳米Al2O3需要纯净的硫酸铝。现有0.05mol•L-1硫酸铝酸性溶液,经检验,含有Fe2+、Fe3+。可按下述操作提纯:往溶液中加足量H2O2充分反应,再用试剂X调节溶液pH=3.5(温室下,0.1 mol•L-1的Fe2+、Al3+开始沉淀的pH分别为7.0和3.7,Fe3+完全沉淀的pH=3.2)
(1)纳米氧化铝分散在分散剂中将形成胶体。则纳米氧化铝的直径约为_______ 。
(2)往溶液中加入H2O2的作用是_______ (用离子方程式表示)。
(3)加入的X试剂(填选项编号)是_______ 。
A.CuO B.Al(OH)3 C.NaOH D.NaHCO3
若调节后溶液的pH偏离3.5,可能带来的后果是_______ 。
(1)纳米氧化铝分散在分散剂中将形成胶体。则纳米氧化铝的直径约为
(2)往溶液中加入H2O2的作用是
(3)加入的X试剂(填选项编号)是
A.CuO B.Al(OH)3 C.NaOH D.NaHCO3
若调节后溶液的pH偏离3.5,可能带来的后果是
您最近一年使用:0次
4 . 以下是有关胶体性质的实验探究,回答相关的问题。
Fe(OH)3胶体的制备:
(1)实验室制取Fe(OH)3胶体的方法是_______ ;该反应的离子方程式是:_______ 。制备Fe(OH)3胶体用到的FeCl3溶解在盐酸溶液中制备得到,需要用盐酸溶液的理由是:_______ 。
(2)制备得到的Fe(OH)3胶体体系具有的性质是_______ (填写序号字母)。
a.光束通过该液体的形成光亮的“通路”
b.静止一段时间后,该红褐色液体仍然澄清透明
c.向该液体中加入硝酸银溶液,无沉淀产生
d.将该液体加热、蒸干、灼烧后,有氧化物生成
(3)在分离和提纯Fe(OH)3胶体时用到的方法是:_______ (填分离操作的名称)。
Fe(OH)3胶体的制备:
(1)实验室制取Fe(OH)3胶体的方法是
(2)制备得到的Fe(OH)3胶体体系具有的性质是
a.光束通过该液体的形成光亮的“通路”
b.静止一段时间后,该红褐色液体仍然澄清透明
c.向该液体中加入硝酸银溶液,无沉淀产生
d.将该液体加热、蒸干、灼烧后,有氧化物生成
(3)在分离和提纯Fe(OH)3胶体时用到的方法是:
您最近一年使用:0次
14-15高二上·湖北荆州·期末
名校
解题方法
5 . NH4Al(SO4)2常作食品加工中的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其原理是_______ (用离子方程式说明)。
(2)相同条件下,0.1mol∙L-1NH4Al(SO4)2溶液中的c( )
)_______ (填“等于”“大于”或“小于”)0.1mol∙L-1NH4HSO4溶液中的c( )。
)。
(3)几种均为0.1mol∙L-1的电解质溶液的pH随温度变化的曲线如图所示。
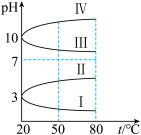
①其中符合0.1mol∙L-1NH4Al(SO4)2溶液的pH随温度变化的曲线是_______ (填罗马数字),导致NH4Al(SO4)2溶液的pH随温度变化的原因是_______ 。
②20℃时,0.1mol∙L-1NH4Al(SO4)2溶液中2c c
c 3cAl3=
3cAl3=_______ molL1。
(4)室温时,向100mL0.1mol∙L-1NH4HSO4溶液中滴加0.1mol∙L-1NaOH溶液,溶液pH与加入NaOH溶液体积的关系曲线如图乙所示。

试分析图中a、b、c、d四个点,水的电离程度最大的是_______ 点;在b点,溶液中各离子浓度由大到小的排列顺序是_______ 。
(1)NH4Al(SO4)2可作净水剂,其原理是
(2)相同条件下,0.1mol∙L-1NH4Al(SO4)2溶液中的c(
 )
) )。
)。(3)几种均为0.1mol∙L-1的电解质溶液的pH随温度变化的曲线如图所示。

①其中符合0.1mol∙L-1NH4Al(SO4)2溶液的pH随温度变化的曲线是
②20℃时,0.1mol∙L-1NH4Al(SO4)2溶液中2c
 c
c 3cAl3=
3cAl3=(4)室温时,向100mL0.1mol∙L-1NH4HSO4溶液中滴加0.1mol∙L-1NaOH溶液,溶液pH与加入NaOH溶液体积的关系曲线如图乙所示。

试分析图中a、b、c、d四个点,水的电离程度最大的是
您最近一年使用:0次
2022-12-01更新
|
1393次组卷
|
57卷引用:2013-2014学年湖北省荆州市部分县市高二上学期期末考试化学试卷
(已下线)2013-2014学年湖北省荆州市部分县市高二上学期期末考试化学试卷(已下线)2014届山西省山大附中高三下学期第一次月考化学试卷2016-2017学年内蒙古包头九中高二上10月月考化学卷2016-2017学年四川省成都七中高二上11月考试化学卷2015—2016学年河南省郑州一中高二上学期期末考试化学试卷湖南省临武一中、嘉禾一中2017-2018学年高二12月联考化学试题河北省永年县第二中学2017-2018学年高二12月月考化学试题宁夏育才中学2017-2018学年高二上学期期末考试化学试题湖北省宜昌市第一中学2017-2018学年高二上学期期末考试化学试题高二人教版选修4 期末学业测评(一)山东省济宁市实验中学2018-2019学年高二上学期第二次月考化学试题(已下线)2019年1月5日 《每日一题》人教选修4-周末培优吉林省松原市扶余市第一中学2018-2019学年高二上学期期末考试化学试题【全国百强校】江苏省扬州中学2018-2019学年高二第二学期五月检测化学试题(已下线)2019年10月13日《每日一题》2020年高考一轮复习——每周一测四川省武胜烈面中学校2019-2020学年高二上学期期中考试化学试题苏教版选修四化学反应原理专题3第三单元 盐类的水解 同步检测试卷(已下线)考点14 化学基本理论——《备战2020年高考精选考点专项突破题集》(已下线)2019年12月30日 《每日一题》人教版(选修4)——盐类水解的影响因素河北省沧州市泊头市第一中学2019-2020学年高二上学期第三次月考化学试题山东省淄博市2019-2020学年高二上学期期中考试化学试题四川省成都市射洪县2018-2019学年高二下学期期末能力素质监测理综化学试题(英才班)山西省晋中市祁县中学校2019-2020学年高二11月月考化学试题鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第2节 弱电解质的电离 盐类的水解 课时3 水解平衡的移动和水解原理的应用河南省南阳市第一中学2021届高三上学期第二次月考(9月)化学试题高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第三节 盐类的水解 课时2 盐类水解的影响因素及应用(已下线)第3章 章末检测-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)浙江省苍南县金乡卫城中学2020-2021学年高二上学期第一次月考化学试题(已下线)3.3.2 影响盐类水解的主要因素和盐类水解的应用(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)江苏省南通市海门实验学校2020-2021学年高二上学期期中考试化学试题安徽省皖南八校2022届高三上学期摸底联考化学试题湖北省黄石市有色第一中学2020-2021学年高二上学期期末考试化学试题福建省莆田锦江中学2020-2021学年高二上学期期末考试化学试题(已下线)第25讲 盐类水解(精练)-2022年高考化学一轮复习讲练测选择性必修1 专题3 第三单元 课时2 盐类水解的影响因素及应用(已下线)3.3.1 盐类的水解-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)第23讲 盐类水解(练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)章末培优3 专题3 水溶液中的离子反应-2021-2022学年高二化学课后培优练(苏教教版2019选择性必修1)(已下线)3.3.3 盐类水解的应用-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)3.3.2 影响盐类水解的主要因素-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)第15练 反应原理综合-2022年【寒假分层作业】高二化学(人教版2019选择性必修2)辽宁省渤海大学附属高级中学2021-2022学年高二上学期期中考试化学试题四川省资阳中学2021-2022学年高二下学期3月月考化学试题山西省运城市教育发展联盟2021-2022学年高二上学期11月期中检测化学试题(已下线)3.3.2 影响盐类的水解的主要因素-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)(已下线)第20讲 盐类水解的影响因素及应用(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)上海市卢湾高级中学2022-2023学年高三上学期期中考试化学试题上海市卢湾高级中学2022-2023学年高三上学期期中考试化学试题(已下线)专题十三水溶液中的离子平衡四川省成都市树德中学2022-2023学年高二上学期期末考试化学试题四川省宜宾市第四中学校2022-2023学年高二下学期开学考试化学试题(已下线)第八章 水溶液中的离子反应与平衡 第49练 盐类的水解(已下线)专题突破卷09 水溶液中的离子反应与平衡 ?-2024年高考化学一轮复习考点通关卷(新教材新高考)广东省广州市华南师范大学附属中学2022-2023学年高二上学期12月月考化学试题(已下线)盐类的水解黑龙江省大庆铁人中学2023-2024学年高二上学期期中考试化学试题山西省朔州市怀仁县阳高一中2023-2024学年高二上学期11月化学试卷
6 . H2O2在Fe2+、Cu2+的存在下生成具有强氧化性的·OH(羟基自由基),·OH可将有机物氧化降解。
(1)Cu2+-H2O2体系中存在下列反应:
Cu2+(aq)+H2O2(aq)= CuOOH+(aq)+H+(aq) ΔH1=a kJ·mol-1
CuOOH+(aq)=Cu+(aq)+·OH(aq)+ O2(g) ΔH2=b kJ·mol-1
O2(g) ΔH2=b kJ·mol-1
2CuOOH+(aq)=2Cu+(aq)+H2O2(aq)+O2(g) ΔH3=c kJ·mol-1
则H2O2(aq)=2·OH(aq) ΔH=________ kJ·mol-1。
(2)为探究Fe2+-Cu2+-H2O2能够协同催化氧化降解甲基橙,某研究小组的实验结果如图1所示。得出“Fe2+-Cu2+-H2O2催化氧化降解甲基橙效果优于单独加入Fe2+或Cu2+”结论的证据为_______ 。
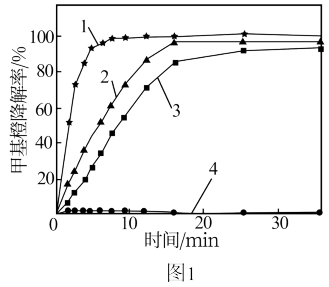
实验条件:200 mL甲基橙模拟废水(1.5 g·L-1,pH=3.0),温度60 ℃、V(H2O2)=2.0 mL
1—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0.02∶0.4
2—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0.02∶0
3—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0∶0.4
4—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0∶0
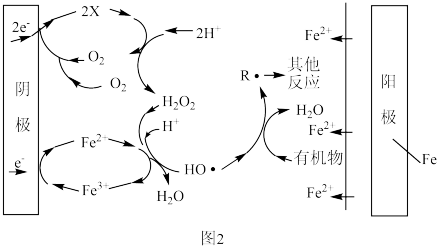
(3)EFH2O2FeOx法可用于水体中有机污染物降解,其反应机理如图2所示。阳极的电极反应式为______ ,X微粒的化学式为________ ,阴极附近Fe2+参与反应的离子方程式为_______ 。
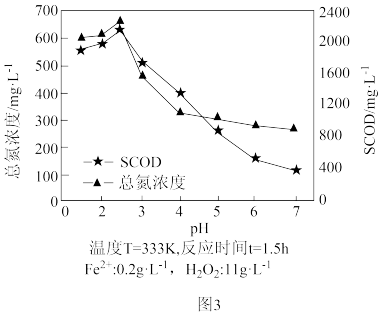
(4)SCOD是指溶解性化学需氧量,是衡量水中有机物质含量多少的指标。水体SCOD越大,说明其有机物含量越高。用Fe2+-H2O2法氧化破解啤酒工业污泥中的微生物,释放出有机物和氮等。测得不同初始pH下污泥经氧化破解后上层清液中的SCOD及总氮浓度如图3所示。当pH>2.5时,总氮浓度、SCOD均降低,其原因可能是__________ 。
(1)Cu2+-H2O2体系中存在下列反应:
Cu2+(aq)+H2O2(aq)= CuOOH+(aq)+H+(aq) ΔH1=a kJ·mol-1
CuOOH+(aq)=Cu+(aq)+·OH(aq)+
 O2(g) ΔH2=b kJ·mol-1
O2(g) ΔH2=b kJ·mol-12CuOOH+(aq)=2Cu+(aq)+H2O2(aq)+O2(g) ΔH3=c kJ·mol-1
则H2O2(aq)=2·OH(aq) ΔH=
(2)为探究Fe2+-Cu2+-H2O2能够协同催化氧化降解甲基橙,某研究小组的实验结果如图1所示。得出“Fe2+-Cu2+-H2O2催化氧化降解甲基橙效果优于单独加入Fe2+或Cu2+”结论的证据为

实验条件:200 mL甲基橙模拟废水(1.5 g·L-1,pH=3.0),温度60 ℃、V(H2O2)=2.0 mL
1—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0.02∶0.4
2—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0.02∶0
3—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0∶0.4
4—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0∶0
(3)EFH2O2FeOx法可用于水体中有机污染物降解,其反应机理如图2所示。阳极的电极反应式为

(4)SCOD是指溶解性化学需氧量,是衡量水中有机物质含量多少的指标。水体SCOD越大,说明其有机物含量越高。用Fe2+-H2O2法氧化破解啤酒工业污泥中的微生物,释放出有机物和氮等。测得不同初始pH下污泥经氧化破解后上层清液中的SCOD及总氮浓度如图3所示。当pH>2.5时,总氮浓度、SCOD均降低,其原因可能是

您最近一年使用:0次
名校
解题方法
7 . 乙烯A主要由石油炼制而获得,其产量可以用来衡量一个国家的石油化工发展水平,乙烯A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型。根据图回答下列问题:
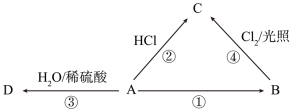
(1)写出A、B、C、D的结构简式:A_______ ,B_______ ,C_______ ,D_______ 。
(2)写出②、④两步反应的化学方程式,并注明反应类型:
②_______ ,反应类型_______ 。
④_______ ,反应类型_______ 。

(1)写出A、B、C、D的结构简式:A
(2)写出②、④两步反应的化学方程式,并注明反应类型:
②
④
您最近一年使用:0次
2022-05-09更新
|
613次组卷
|
9卷引用:2016届浙江省杭州市五校联盟高三第二次诊断考试理综化学试卷
2016届浙江省杭州市五校联盟高三第二次诊断考试理综化学试卷2015-2016学年河北省沧州市黄骅中学高一下期中化学试卷黑龙江省青冈县一中2018-2019学年高二上学期开学考试化学试题湖北省汉川市第二中学2018-2019学年高一下学期5月月考化学试题吉林省长春市九台区第四中学2018-2019学年高一下学期期中考试化学试题吉林省白城市第一中学2019-2020学年高一下学期期末考试化学试题课后-7.2.1 乙烯-人教2019必修第二册(已下线)7.2.2 不饱和烃-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)(已下线)专题05 饱和烃与不饱和烃(知识串讲+专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(沪科版2020必修第二册)
解题方法
8 . 丙烯酰胺是一种重要的有机合成的中间体。它的球棍模型如图所示(图中“棍”代表单键或双键,不同颜色的球表示不同原子):

(1)丙烯酰胺的分子式为___________ ,结构简式为___________ 。
(2)有关丙烯酰胺的说法正确的是___________。
(3)工业上生产丙烯酰胺可以用下面的反应(反应均在一定条件下进行):CH≡CH CH2=CHCN
CH2=CHCN 丙烯酰胺,假设反应I和反应II都是原子利用率为100%的反应,反应I所需另一反应物的分子式为
丙烯酰胺,假设反应I和反应II都是原子利用率为100%的反应,反应I所需另一反应物的分子式为___________ ,反应II的化学方程式为___________ 。
(4)聚丙烯酰胺(PAM)是一种合成有机高分子絮凝剂,写出由丙烯酰胺合成聚丙烯酰胺的化学方程式:___________ 。

(1)丙烯酰胺的分子式为
(2)有关丙烯酰胺的说法正确的是___________。
| A.丙烯酰胺分子内所有原子不可能在同一平面内 |
| B.丙烯酰胺属于烃的衍生物 |
| C.丙烯酰胺能使酸性高锰酸钾溶液褪色 |
| D.丙烯酰胺能使溴的四氯化碳溶液褪色 |
 CH2=CHCN
CH2=CHCN 丙烯酰胺,假设反应I和反应II都是原子利用率为100%的反应,反应I所需另一反应物的分子式为
丙烯酰胺,假设反应I和反应II都是原子利用率为100%的反应,反应I所需另一反应物的分子式为(4)聚丙烯酰胺(PAM)是一种合成有机高分子絮凝剂,写出由丙烯酰胺合成聚丙烯酰胺的化学方程式:
您最近一年使用:0次
2022-02-07更新
|
261次组卷
|
4卷引用:广东省深圳市2020届高三二模热身试题化学试题
广东省深圳市2020届高三二模热身试题化学试题陕西省榆林市清源中学2020-2021学年高二下学期第一次月考化学试题(已下线)3.4.3 油脂与酰胺-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修3)(已下线)第19讲 油脂 酰胺(word讲义)-【帮课堂】2021-2022学年高二化学同步精品讲义(人教2019选择性必修3)
9 . 常温下,部分酸的电离平衡常数如下:
(1) 相同的三种酸,则
相同的三种酸,则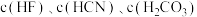 的浓度从大到小为
的浓度从大到小为___________ 。
(2)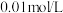 的
的 溶液中,
溶液中, 为
为_____  ,使此溶液中
,使此溶液中 的电离程度增大且
的电离程度增大且 也增大的方法是
也增大的方法是_______ 。
(3)中和等量的 ,消耗等
,消耗等 的氢氟酸和硫酸的体积分别为
的氢氟酸和硫酸的体积分别为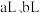 ,则a
,则a______ b(填“大于”、“小于”或“等于”,下同)。中和等浓度、等体积的氢氟酸和硫酸需要 的物质的量为
的物质的量为 ,则
,则
___________  。
。
(4)向 中通入少量的
中通入少量的 ,发生的离子方程式为
,发生的离子方程式为___________ 。
(5)设计实验证明氢氟酸比盐酸的酸性弱___________ 。
化学式 |
|
|
|
电离常数 |
|
|
|
 相同的三种酸,则
相同的三种酸,则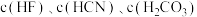 的浓度从大到小为
的浓度从大到小为(2)
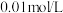 的
的 溶液中,
溶液中, 为
为 ,使此溶液中
,使此溶液中 的电离程度增大且
的电离程度增大且 也增大的方法是
也增大的方法是(3)中和等量的
 ,消耗等
,消耗等 的氢氟酸和硫酸的体积分别为
的氢氟酸和硫酸的体积分别为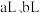 ,则a
,则a 的物质的量为
的物质的量为 ,则
,则
 。
。(4)向
 中通入少量的
中通入少量的 ,发生的离子方程式为
,发生的离子方程式为(5)设计实验证明氢氟酸比盐酸的酸性弱
您最近一年使用:0次
2022-01-13更新
|
483次组卷
|
4卷引用:山东省临沂市临沭第一中学2018届高三10月学情调研测试化学试题
山东省临沂市临沭第一中学2018届高三10月学情调研测试化学试题山西省太原市山西省实验中学2019-2020学年高二上学期12月月考化学试题重庆市万州第二高级中学2021-2022学年高二上学期期中考试化学试题(已下线)微专题37 强弱电解质的判断与比较-备战2023年高考化学一轮复习考点微专题
10 . 请回答下列问题:
(1) 是一种酸根离子,
是一种酸根离子, 中铁元素的化合价为
中铁元素的化合价为___________ 。 属于
属于___________ (填“酸”“碱”、“盐”或“氧化物”)。
(2)新型纳米材料氧缺位铁酸盐(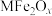 ,
,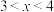 ,
, 、Zn、Ni,且均为
、Zn、Ni,且均为 价,下同)是由铁酸盐
价,下同)是由铁酸盐 经过高温反应得到的。将纳米材料氧缺位铁酸盐分散在蒸馏水中,所形成的分散系属于
经过高温反应得到的。将纳米材料氧缺位铁酸盐分散在蒸馏水中,所形成的分散系属于___________ ;铁酸盐 经过高温反应得到
经过高温反应得到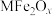 的反应属于
的反应属于___________ (填“氧化还原”或“非氧化还原”)反应。
(3)在酸性条件下, 容易转化为
容易转化为 ,某反应体系中共存在下列6种粒子:
,某反应体系中共存在下列6种粒子: 、
、 、
、 、
、 、
、 、
、 ,则该反应中的氧化剂是
,则该反应中的氧化剂是___________ ,还原剂是___________ 。
(4) 是重要的化工原料,从氧化还原反应的角度分析,下列制备
是重要的化工原料,从氧化还原反应的角度分析,下列制备 的方案理论上可行的是
的方案理论上可行的是___________ (填字母)。
a. b.
b. c.
c. d.
d.
(5)已知 能被
能被 氧化为
氧化为 ,则
,则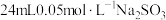 溶液与
溶液与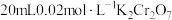 溶液恰好反应时,Cr元素在还原产物中的化合价为
溶液恰好反应时,Cr元素在还原产物中的化合价为___________ 。
(1)
 是一种酸根离子,
是一种酸根离子, 中铁元素的化合价为
中铁元素的化合价为 属于
属于(2)新型纳米材料氧缺位铁酸盐(
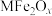 ,
,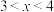 ,
, 、Zn、Ni,且均为
、Zn、Ni,且均为 价,下同)是由铁酸盐
价,下同)是由铁酸盐 经过高温反应得到的。将纳米材料氧缺位铁酸盐分散在蒸馏水中,所形成的分散系属于
经过高温反应得到的。将纳米材料氧缺位铁酸盐分散在蒸馏水中,所形成的分散系属于 经过高温反应得到
经过高温反应得到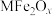 的反应属于
的反应属于(3)在酸性条件下,
 容易转化为
容易转化为 ,某反应体系中共存在下列6种粒子:
,某反应体系中共存在下列6种粒子: 、
、 、
、 、
、 、
、 、
、 ,则该反应中的氧化剂是
,则该反应中的氧化剂是(4)
 是重要的化工原料,从氧化还原反应的角度分析,下列制备
是重要的化工原料,从氧化还原反应的角度分析,下列制备 的方案理论上可行的是
的方案理论上可行的是a.
 b.
b. c.
c. d.
d.
(5)已知
 能被
能被 氧化为
氧化为 ,则
,则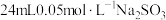 溶液与
溶液与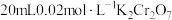 溶液恰好反应时,Cr元素在还原产物中的化合价为
溶液恰好反应时,Cr元素在还原产物中的化合价为
您最近一年使用:0次
2021-12-08更新
|
366次组卷
|
3卷引用:安徽省安庆市宿松县程集中学2021届高三上学期9月月考化学试题