解题方法
1 . NaCN属于剧毒化学品,应与酸类、氧化剂、食用化学品分开存放。其阴离子 中各原子均满足8电子稳定结构,NaCN的电子式为
中各原子均满足8电子稳定结构,NaCN的电子式为_______ ;强氧化剂NaClO会将 氧化,生成
氧化,生成 、
、 和
和 等无毒无害物质,可用该反应处理含氰废水(破氰),该反应的离子方程式为
等无毒无害物质,可用该反应处理含氰废水(破氰),该反应的离子方程式为_______ 。
 中各原子均满足8电子稳定结构,NaCN的电子式为
中各原子均满足8电子稳定结构,NaCN的电子式为 氧化,生成
氧化,生成 、
、 和
和 等无毒无害物质,可用该反应处理含氰废水(破氰),该反应的离子方程式为
等无毒无害物质,可用该反应处理含氰废水(破氰),该反应的离子方程式为
您最近一年使用:0次
14-15高二上·湖北荆州·期末
名校
解题方法
2 . NH4Al(SO4)2常作食品加工中的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其原理是_______ (用离子方程式说明)。
(2)相同条件下,0.1mol∙L-1NH4Al(SO4)2溶液中的c( )
)_______ (填“等于”“大于”或“小于”)0.1mol∙L-1NH4HSO4溶液中的c( )。
)。
(3)几种均为0.1mol∙L-1的电解质溶液的pH随温度变化的曲线如图所示。
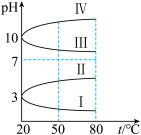
①其中符合0.1mol∙L-1NH4Al(SO4)2溶液的pH随温度变化的曲线是_______ (填罗马数字),导致NH4Al(SO4)2溶液的pH随温度变化的原因是_______ 。
②20℃时,0.1mol∙L-1NH4Al(SO4)2溶液中2c c
c 3cAl3=
3cAl3=_______ molL1。
(4)室温时,向100mL0.1mol∙L-1NH4HSO4溶液中滴加0.1mol∙L-1NaOH溶液,溶液pH与加入NaOH溶液体积的关系曲线如图乙所示。

试分析图中a、b、c、d四个点,水的电离程度最大的是_______ 点;在b点,溶液中各离子浓度由大到小的排列顺序是_______ 。
(1)NH4Al(SO4)2可作净水剂,其原理是
(2)相同条件下,0.1mol∙L-1NH4Al(SO4)2溶液中的c(
 )
) )。
)。(3)几种均为0.1mol∙L-1的电解质溶液的pH随温度变化的曲线如图所示。

①其中符合0.1mol∙L-1NH4Al(SO4)2溶液的pH随温度变化的曲线是
②20℃时,0.1mol∙L-1NH4Al(SO4)2溶液中2c
 c
c 3cAl3=
3cAl3=(4)室温时,向100mL0.1mol∙L-1NH4HSO4溶液中滴加0.1mol∙L-1NaOH溶液,溶液pH与加入NaOH溶液体积的关系曲线如图乙所示。

试分析图中a、b、c、d四个点,水的电离程度最大的是
您最近一年使用:0次
2022-12-01更新
|
1394次组卷
|
57卷引用:安徽省皖南八校2022届高三上学期摸底联考化学试题
安徽省皖南八校2022届高三上学期摸底联考化学试题湖北省黄石市有色第一中学2020-2021学年高二上学期期末考试化学试题福建省莆田锦江中学2020-2021学年高二上学期期末考试化学试题(已下线)第25讲 盐类水解(精练)-2022年高考化学一轮复习讲练测选择性必修1 专题3 第三单元 课时2 盐类水解的影响因素及应用(已下线)3.3.1 盐类的水解-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)第23讲 盐类水解(练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)章末培优3 专题3 水溶液中的离子反应-2021-2022学年高二化学课后培优练(苏教教版2019选择性必修1)(已下线)3.3.3 盐类水解的应用-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)3.3.2 影响盐类水解的主要因素-2021-2022学年高二化学课后培优练(人教版选修4)辽宁省渤海大学附属高级中学2021-2022学年高二上学期期中考试化学试题山西省运城市教育发展联盟2021-2022学年高二上学期11月期中检测化学试题(已下线)2013-2014学年湖北省荆州市部分县市高二上学期期末考试化学试卷(已下线)2014届山西省山大附中高三下学期第一次月考化学试卷2016-2017学年内蒙古包头九中高二上10月月考化学卷2016-2017学年四川省成都七中高二上11月考试化学卷2015—2016学年河南省郑州一中高二上学期期末考试化学试卷湖南省临武一中、嘉禾一中2017-2018学年高二12月联考化学试题河北省永年县第二中学2017-2018学年高二12月月考化学试题宁夏育才中学2017-2018学年高二上学期期末考试化学试题湖北省宜昌市第一中学2017-2018学年高二上学期期末考试化学试题高二人教版选修4 期末学业测评(一)山东省济宁市实验中学2018-2019学年高二上学期第二次月考化学试题(已下线)2019年1月5日 《每日一题》人教选修4-周末培优吉林省松原市扶余市第一中学2018-2019学年高二上学期期末考试化学试题【全国百强校】江苏省扬州中学2018-2019学年高二第二学期五月检测化学试题(已下线)2019年10月13日《每日一题》2020年高考一轮复习——每周一测四川省武胜烈面中学校2019-2020学年高二上学期期中考试化学试题苏教版选修四化学反应原理专题3第三单元 盐类的水解 同步检测试卷(已下线)考点14 化学基本理论——《备战2020年高考精选考点专项突破题集》(已下线)2019年12月30日 《每日一题》人教版(选修4)——盐类水解的影响因素河北省沧州市泊头市第一中学2019-2020学年高二上学期第三次月考化学试题山东省淄博市2019-2020学年高二上学期期中考试化学试题四川省成都市射洪县2018-2019学年高二下学期期末能力素质监测理综化学试题(英才班)山西省晋中市祁县中学校2019-2020学年高二11月月考化学试题鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第2节 弱电解质的电离 盐类的水解 课时3 水解平衡的移动和水解原理的应用河南省南阳市第一中学2021届高三上学期第二次月考(9月)化学试题高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第三节 盐类的水解 课时2 盐类水解的影响因素及应用(已下线)第3章 章末检测-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)浙江省苍南县金乡卫城中学2020-2021学年高二上学期第一次月考化学试题(已下线)3.3.2 影响盐类水解的主要因素和盐类水解的应用(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)江苏省南通市海门实验学校2020-2021学年高二上学期期中考试化学试题(已下线)第15练 反应原理综合-2022年【寒假分层作业】高二化学(人教版2019选择性必修2)四川省资阳中学2021-2022学年高二下学期3月月考化学试题(已下线)3.3.2 影响盐类的水解的主要因素-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)(已下线)第20讲 盐类水解的影响因素及应用(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)上海市卢湾高级中学2022-2023学年高三上学期期中考试化学试题上海市卢湾高级中学2022-2023学年高三上学期期中考试化学试题(已下线)专题十三水溶液中的离子平衡四川省成都市树德中学2022-2023学年高二上学期期末考试化学试题四川省宜宾市第四中学校2022-2023学年高二下学期开学考试化学试题(已下线)第八章 水溶液中的离子反应与平衡 第49练 盐类的水解(已下线)专题突破卷09 水溶液中的离子反应与平衡 ?-2024年高考化学一轮复习考点通关卷(新教材新高考)广东省广州市华南师范大学附属中学2022-2023学年高二上学期12月月考化学试题(已下线)盐类的水解黑龙江省大庆铁人中学2023-2024学年高二上学期期中考试化学试题山西省朔州市怀仁县阳高一中2023-2024学年高二上学期11月化学试卷
3 . 已知A为烃,B为烃的含氧衍生物,由等物质的量的A、B组成的混合物0.05mol在0.125mol的氧气中恰好完全燃烧,生成0.1mol的CO2和0.1molH2O,且A与B具有相同的碳原子数。
(1)A、B可能的分子组成(任写两种组合)___________ 、___________ 。
(2)请写出简要的推断过程___________ 。
(1)A、B可能的分子组成(任写两种组合)
(2)请写出简要的推断过程
您最近一年使用:0次
解题方法
4 . 填空。
(1)化合物A、B、C的熔点如下表:
化合物C的熔点明显高于A的原因是___________ 。
(2)20%的NaCl溶液中滴加乙醇会有白色固体析出,原因是___________ 。
(1)化合物A、B、C的熔点如下表:
| A | B | C | |
| 化学式 | CH3CH2Cl | CH3CH2CH2Cl | CH3NH3Cl |
| 熔点/℃ | -139 | -123 | 230 |
(2)20%的NaCl溶液中滴加乙醇会有白色固体析出,原因是
您最近一年使用:0次
5 . 乙烯产量是衡量一个国家石油化工水平的重要标志。回答下列问题:
(1)实验室可用乙醇与浓硫酸共热制取乙烯,乙醇所含官能团的名称为_______ 。
(2)乙醇制乙烯过程中会产生 和
和 等杂质。
等杂质。
①检验产物中 的方法是
的方法是_______ , 的电子式为
的电子式为_______ 。
② 也能使酸性
也能使酸性 溶液褪色,写出反应的离子方程式
溶液褪色,写出反应的离子方程式_______ 。
③ 和
和 均能与
均能与 溶液反应,写出
溶液反应,写出 与
与 溶液反应的化学方程式
溶液反应的化学方程式_______ 。(已知常温下,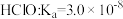 ,
,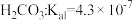 ,
,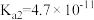 )
)
(3)一种由乙烯制备聚丙烯酸甲酯的合成路线如图:

① 的反应类型是
的反应类型是_______ 。
②D的结构简式为_______ ,与E具有相同官能团的同分异构体还有_______ 种。
③出由E合成聚丙烯酸甲酯的化学方程式_______ 。
(1)实验室可用乙醇与浓硫酸共热制取乙烯,乙醇所含官能团的名称为
(2)乙醇制乙烯过程中会产生
 和
和 等杂质。
等杂质。①检验产物中
 的方法是
的方法是 的电子式为
的电子式为②
 也能使酸性
也能使酸性 溶液褪色,写出反应的离子方程式
溶液褪色,写出反应的离子方程式③
 和
和 均能与
均能与 溶液反应,写出
溶液反应,写出 与
与 溶液反应的化学方程式
溶液反应的化学方程式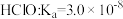 ,
,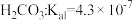 ,
,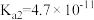 )
)(3)一种由乙烯制备聚丙烯酸甲酯的合成路线如图:

①
 的反应类型是
的反应类型是②D的结构简式为
③出由E合成聚丙烯酸甲酯的化学方程式
您最近一年使用:0次
名校
解题方法
6 .  与
与 在高温下发生反应:
在高温下发生反应: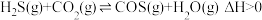 。在
。在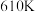 时,将
时,将 与
与 充入
充入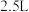 的空钢瓶中,经过
的空钢瓶中,经过 反应达到平衡,平衡时水蒸气的物质的量分数为0.125。
反应达到平衡,平衡时水蒸气的物质的量分数为0.125。
(1)用 的浓度变化表示的反应速率
的浓度变化表示的反应速率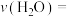
________ 。 的平衡转化率
的平衡转化率
_______  。
。
(2) 时该反应的平衡常数
时该反应的平衡常数 ,在此温度下按相同投料在相同容器中重复上述反应,经过
,在此温度下按相同投料在相同容器中重复上述反应,经过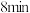 ,测得水蒸气的物质的量为
,测得水蒸气的物质的量为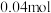 。判断此时该反应是否达到平衡
。判断此时该反应是否达到平衡___________ (填“是”“否”或“无法确定”)。
(3) 时,在体积一定的密闭容器中按原料初始组成
时,在体积一定的密闭容器中按原料初始组成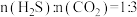 进行该反应,能判断反应达到化学平衡状态的依据是___________。
进行该反应,能判断反应达到化学平衡状态的依据是___________。
(4)要增大该反应的平衡常数K值,可采取的措施有___________。
 与
与 在高温下发生反应:
在高温下发生反应: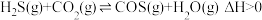 。在
。在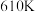 时,将
时,将 与
与 充入
充入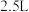 的空钢瓶中,经过
的空钢瓶中,经过 反应达到平衡,平衡时水蒸气的物质的量分数为0.125。
反应达到平衡,平衡时水蒸气的物质的量分数为0.125。(1)用
 的浓度变化表示的反应速率
的浓度变化表示的反应速率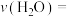
 的平衡转化率
的平衡转化率
 。
。(2)
 时该反应的平衡常数
时该反应的平衡常数 ,在此温度下按相同投料在相同容器中重复上述反应,经过
,在此温度下按相同投料在相同容器中重复上述反应,经过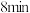 ,测得水蒸气的物质的量为
,测得水蒸气的物质的量为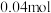 。判断此时该反应是否达到平衡
。判断此时该反应是否达到平衡(3)
 时,在体积一定的密闭容器中按原料初始组成
时,在体积一定的密闭容器中按原料初始组成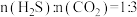 进行该反应,能判断反应达到化学平衡状态的依据是___________。
进行该反应,能判断反应达到化学平衡状态的依据是___________。| A.容器中压强不再改变 |
B.容器中 的物质的量分数不再改变 的物质的量分数不再改变 |
C. |
| D.容器中混合气体的密度不再改变 |
A.增大 的起始浓度 的起始浓度 | B.增大反应体系压强 |
| C.使用高效催化剂 | D.升高温度 |
您最近一年使用:0次
2022-01-15更新
|
522次组卷
|
3卷引用:新疆维吾尔自治区乌鲁木齐市2021-2022学年高三上学期第一次诊断性测试化学试题
新疆维吾尔自治区乌鲁木齐市2021-2022学年高三上学期第一次诊断性测试化学试题(已下线)第22讲 化学平衡常数及转化率的计算(练)-2023年高考化学一轮复习讲练测(全国通用)黑龙江省七台河市勃利县高级中学2022-2023学年高二上学期期中考试化学试题
7 . 化学与生产、生活、科学技术息息相关。
(1)生活中常用的“84”消毒液与洁厕灵(主要成分是盐酸)混合时会产生大量的有毒气体,写出该反应的离子方程式:___________ 。
(2)中国古代著作中有“银针验毒”的记录,其原理类似为: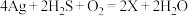 ,则X的化学式是
,则X的化学式是___________ ,其中 在该反应中
在该反应中___________ (填字母序号)。
A.是氧化剂 B.是还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(3)酯可用作饮料、化妆品中的香料。写出实验室制备乙酸乙酯的化学反应方程式:______ 。
(4) 和
和 都是大气污染物,汽车发动机工作时产生的
都是大气污染物,汽车发动机工作时产生的 和CO可通过催化转化器转化为两种无污染的气体,该反应的化学方程式是
和CO可通过催化转化器转化为两种无污染的气体,该反应的化学方程式是______ 。
(1)生活中常用的“84”消毒液与洁厕灵(主要成分是盐酸)混合时会产生大量的有毒气体,写出该反应的离子方程式:
(2)中国古代著作中有“银针验毒”的记录,其原理类似为:
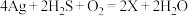 ,则X的化学式是
,则X的化学式是 在该反应中
在该反应中A.是氧化剂 B.是还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(3)酯可用作饮料、化妆品中的香料。写出实验室制备乙酸乙酯的化学反应方程式:
(4)
 和
和 都是大气污染物,汽车发动机工作时产生的
都是大气污染物,汽车发动机工作时产生的 和CO可通过催化转化器转化为两种无污染的气体,该反应的化学方程式是
和CO可通过催化转化器转化为两种无污染的气体,该反应的化学方程式是
您最近一年使用:0次
8 . 氮及其化合物在工农业生产和生命活动中起着重要的作用。回答下列问题:
(1)“中国制造2025”是中国政府实施制造强国战略第一 个十年行动纲领。氮化铬在现代工业中发挥更重要的作用,请写出Cr3+的价电子轨道表示式___________ ;基态铬、氮原子的未成对电子数之比为___________ 。
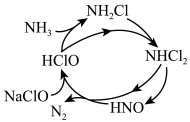
(2)NH3也是造成水体富营养化的重要原因之一,用NaClO溶液氧化可除去氨气。其反应机理如图所示(其中H2O和NaCl 略去)。NaClO 氧化NH3的总反应化学程式为___________ 。
(3)改变 对溶液中NaClO去除氨气效果与余氯(溶液中+1价氯元素的含量)的影响如图所示,则除氨气过程中最佳的
对溶液中NaClO去除氨气效果与余氯(溶液中+1价氯元素的含量)的影响如图所示,则除氨气过程中最佳的 值约为
值约为___________ 。

(4)室温下,用水稀释0.1mol·L-1氨水,溶液中随着水量的增加而减小的是___________。
(5)25°C时,将amol NH4NO3溶于水,向该溶液中滴加bL氨水后溶液呈中性,滴加氨水的过程中水的电离平衡将___________ (填 “正向”、“逆向”或“不”)移动。
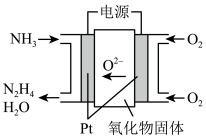
(6)工业上利用NH3制备联氨(N2H4)装置如下图,其阳极电极反应式为___________ 。
(1)“中国制造2025”是中国政府实施制造强国战略第一 个十年行动纲领。氮化铬在现代工业中发挥更重要的作用,请写出Cr3+的价电子轨道表示式
(2)NH3也是造成水体富营养化的重要原因之一,用NaClO溶液氧化可除去氨气。其反应机理如图所示(其中H2O和NaCl 略去)。NaClO 氧化NH3的总反应化学程式为

(3)改变
 对溶液中NaClO去除氨气效果与余氯(溶液中+1价氯元素的含量)的影响如图所示,则除氨气过程中最佳的
对溶液中NaClO去除氨气效果与余氯(溶液中+1价氯元素的含量)的影响如图所示,则除氨气过程中最佳的 值约为
值约为
(4)室温下,用水稀释0.1mol·L-1氨水,溶液中随着水量的增加而减小的是___________。
A.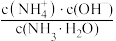 ) ) | B.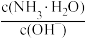 |
| C.c(H+) | D.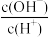 |
(6)工业上利用NH3制备联氨(N2H4)装置如下图,其阳极电极反应式为

您最近一年使用:0次
名校
9 . 某固体化合物X由5种元素组成。某学习小组进行了如图实验:

已知气体B能使湿润红色石蕊试纸变蓝。请回答:
(1)X中含有的元素有___ ,气体B的电子式___ 。
(2)X的化学式__ 。
(3)X的水溶液可以与纤维素作用,工业上利用此性质得到产物名称__ 。
(4)写出X隔绝空气强热生成A、D、E的化学方程式___ 。

已知气体B能使湿润红色石蕊试纸变蓝。请回答:
(1)X中含有的元素有
(2)X的化学式
(3)X的水溶液可以与纤维素作用,工业上利用此性质得到产物名称
(4)写出X隔绝空气强热生成A、D、E的化学方程式
您最近一年使用:0次
名校
10 . 请回答以下问题:
(1)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),而与其原子总数相等的等电子体CH3CH3相比,NH3BH3熔点比CH3CH3高,其原因是__ 。
(2)已知高温下,冰晶石密度为2.1g/cm3,铝单质的密度为2.3g/cm3,工业上电解法制单质铝的过程中,冰晶石起到哪些作用__ 。
(1)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),而与其原子总数相等的等电子体CH3CH3相比,NH3BH3熔点比CH3CH3高,其原因是
(2)已知高温下,冰晶石密度为2.1g/cm3,铝单质的密度为2.3g/cm3,工业上电解法制单质铝的过程中,冰晶石起到哪些作用
您最近一年使用:0次



