名校
解题方法
1 . 将12.6g无水亚硫酸钠固体加入100mL 8mol·L-1的硫酸中以制取SO2气体,反应完全后,若溶液中含+4价硫元素的物质的总浓度为0.2mol·L-1,假定溶液体积不变,忽略容器及导管中的气体体积,求:
(1)溶液中硫元素的质量_________ 。
(2)收集到SO2气体_________ 毫升(标准状况下)?
(1)溶液中硫元素的质量
(2)收集到SO2气体
您最近一年使用:0次
名校
2 . 将容积为50mL的量筒内充满NO2和O2的混合气体,倒置量筒在盛满水的水槽里,足够时间后,量筒里剩余气体体积为5mL。则混合气体中NO2和O2体积比可能是________ 。
您最近一年使用:0次
名校
解题方法
3 . 某100 mL的CuCl2溶液中,已知溶液中的Cl-的浓度为0.2 mol·L-1。现将一定量的铁粉投入到该溶液中,若反应后溶液体积不变,回答下列问题:
(1)原溶液中Cu2+的浓度为___________ ;
(2)反应后测得Cl-的浓度为___________ ;
(3)反应中氧化剂是___________ ,反应后测得溶液中Fe2+的浓度为0.05 mol/L,则反应生成铜单质的质量为___________ g,转移电子___________ 个;
(4)剩余的Cu2+的物质的量浓度为___________ 。
(1)原溶液中Cu2+的浓度为
(2)反应后测得Cl-的浓度为
(3)反应中氧化剂是
(4)剩余的Cu2+的物质的量浓度为
您最近一年使用:0次
名校
4 . 在2 L密闭容器中进行反应:mX(g)+nY(g) pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:
pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:
已知2 min内v(Q)=0.075 mol·L-1·min-1, =0.5
=0.5
(1)试确定以下物质的相关量:起始时n(Y)=___________ ,n(Q)=___________ ;
(2)方程式中m=___________ ,n=___________ ,p=___________ ,q=___________ ;
(3)用Z表示2 min内的反应速率___________ 。
 pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:
pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:| 物质 时间 | X | Y | Z | Q |
| 起始/mol | 0.7 | 1 | ||
| 2 min末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
| 3 min末/mol | 0.8 |
 =0.5
=0.5(1)试确定以下物质的相关量:起始时n(Y)=
(2)方程式中m=
(3)用Z表示2 min内的反应速率
您最近一年使用:0次
5 . 计算填空:
(1)实验室要配制360 g 10%的盐酸,需要36%的浓盐酸的质量是_______ 。
(2)配制溶质质量分数20%的稀硫酸溶液100 g,需要98%的浓硫酸(密度为1.84 g·mL-1)的体积是_______ 。
(3)配制溶质质量分数为20%的硫酸溶液1000g,需要98%的浓硫酸的质量是_______ ,需要10%的稀硫酸的质量是_______ 。
(1)实验室要配制360 g 10%的盐酸,需要36%的浓盐酸的质量是
(2)配制溶质质量分数20%的稀硫酸溶液100 g,需要98%的浓硫酸(密度为1.84 g·mL-1)的体积是
(3)配制溶质质量分数为20%的硫酸溶液1000g,需要98%的浓硫酸的质量是
您最近一年使用:0次
6 . 化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与化学键形成时放出的能量不同引起的,如图是N2和O2反应生成NO过程中的能量变化

请回答下列有关问题:
(1)反应物断键吸收的总能量为___________ 。
(2)生成物成键放出的总能量为___________ 。
(3)判断反应N2+O2=2NO是___________ (填“吸收”或“放出”)能量。
(4)反应物的总能量___________ (填“>”,“=”或“<”)生成物的总能量。

请回答下列有关问题:
(1)反应物断键吸收的总能量为
(2)生成物成键放出的总能量为
(3)判断反应N2+O2=2NO是
(4)反应物的总能量
您最近一年使用:0次
2021-06-11更新
|
586次组卷
|
2卷引用:海南省儋州川绵中学2021-2022学年高一下学期期中考试(等级考)化学试题
解题方法
7 . 根据晶胞结构示意图,计算晶胞的体积或密度。
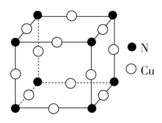
(1)N和Cu元素形成的化合物的晶胞结构如图所示,则该化合物的化学式为____ 。该化合物的相对分子质量为M,NA为阿伏加德罗常数的值。若该晶胞的边长为a cm,则该晶体的密度是______ g·cm-3。
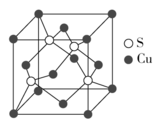
(2)S与Cu形成化合物晶体的晶胞如图所示。已知该晶体的密度为a g·cm-3,则该晶胞中硫原子的个数为______ 的体积为______ cm3(NA表示阿伏加德罗常数的值)。
(1)N和Cu元素形成的化合物的晶胞结构如图所示,则该化合物的化学式为

(2)S与Cu形成化合物晶体的晶胞如图所示。已知该晶体的密度为a g·cm-3,则该晶胞中硫原子的个数为

您最近一年使用:0次
8 . 回答下列问题
(1)0.5 mol的H2O所含有的氢原子个数为___ 个,所具有的质量为___ g。
(2)标准状况下,44.8 L的氧气的质量为___ g,氧气分子个数___ 个。
(3)1 L 0.1 mol/L的Na2SO4溶液中,Na+数目为___ 个,所含硫酸钠溶质的质量为___ g。
(1)0.5 mol的H2O所含有的氢原子个数为
(2)标准状况下,44.8 L的氧气的质量为
(3)1 L 0.1 mol/L的Na2SO4溶液中,Na+数目为
您最近一年使用:0次
9 . 化学平衡常数只与温度有关,与反应物或生成物的浓度无关。
已知可逆反应:M(g)+N(g) P(g)+Q(g),△H>0
P(g)+Q(g),△H>0
请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为:c(M)=1mol·L-1,c(N)=2.4mol·L-1;达到平衡后,M的转化率为60%,此时N的转化率为___ ;
(2)若反应温度升高,M的转化率___ (填“增大”“减小”或“不变”;)
(3)若反应温度不变,反应物的起始浓度分别为:c(M)=4mol·L-1,c(N)=amol·L-1;达到平衡后,c(P)=2mol·L-1,a=___ ;
(4)若反应温度不变,反应物的起始浓度为:c(M)=c(N)=1mol•L-1,达到平衡后,M的转化率为___ 。
已知可逆反应:M(g)+N(g)
 P(g)+Q(g),△H>0
P(g)+Q(g),△H>0请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为:c(M)=1mol·L-1,c(N)=2.4mol·L-1;达到平衡后,M的转化率为60%,此时N的转化率为
(2)若反应温度升高,M的转化率
(3)若反应温度不变,反应物的起始浓度分别为:c(M)=4mol·L-1,c(N)=amol·L-1;达到平衡后,c(P)=2mol·L-1,a=
(4)若反应温度不变,反应物的起始浓度为:c(M)=c(N)=1mol•L-1,达到平衡后,M的转化率为
您最近一年使用:0次
10 . 某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示,据此回答:

(1)该反应的化学方程式为______ 。
(2)从开始至2min,X的平均反应速率为______ mol/(L·min)、Z的平均反应速率为______ mol/(L·min)。
(3)改变下列条件,可以加快化学反应速率的有______ 。
A.升高温度
B.减小物质X的物质的量
C.增加物质Z的物质的量
D.减小压强

(1)该反应的化学方程式为
(2)从开始至2min,X的平均反应速率为
(3)改变下列条件,可以加快化学反应速率的有
A.升高温度
B.减小物质X的物质的量
C.增加物质Z的物质的量
D.减小压强
您最近一年使用:0次



