解题方法
1 . 以石英砂(主要成分为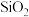 )为原料,经三步反应制得高纯硅,其中第一步反应的化学方程式如下。
)为原料,经三步反应制得高纯硅,其中第一步反应的化学方程式如下。
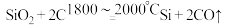
(1)作还原剂的物质是_______ ,碳元素的化合价_______ (填“升高”或“降低”)。
(2)若反应中消耗了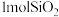 ,则生成
,则生成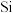 的物质的量为
的物质的量为_______  ,转移电子的物质的量为
,转移电子的物质的量为_______  。
。
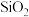 )为原料,经三步反应制得高纯硅,其中第一步反应的化学方程式如下。
)为原料,经三步反应制得高纯硅,其中第一步反应的化学方程式如下。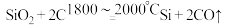
(1)作还原剂的物质是
(2)若反应中消耗了
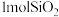 ,则生成
,则生成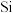 的物质的量为
的物质的量为 ,转移电子的物质的量为
,转移电子的物质的量为 。
。
您最近一年使用:0次
名校
解题方法
2 . 回答下列问题。
(1)依据物质的性质分析:CaO、Na2O、Fe2O3、CuO均属于______ (填“酸性氧化物”、“碱性氧化物”或“两性氧化物”),下列物质均能与它们发生反应的是______ (填字母)。
a.水 b.盐酸 c.氢氧化钠溶液
(2)木炭与浓硫酸发生反应: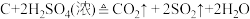 。作还原剂的物质是
。作还原剂的物质是______ ,硫元素的化合价______ (填“升高”或“降低”)。
(3)某反应中反应物与生成物的Fe3+、Mn2+、H+、 、H2O和一种未知离子X
、H2O和一种未知离子X
①已知 在反应中得到电子,则X是
在反应中得到电子,则X是______ 。
②该反应的离子方程式是______ 。
(1)依据物质的性质分析:CaO、Na2O、Fe2O3、CuO均属于
a.水 b.盐酸 c.氢氧化钠溶液
(2)木炭与浓硫酸发生反应:
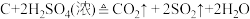 。作还原剂的物质是
。作还原剂的物质是(3)某反应中反应物与生成物的Fe3+、Mn2+、H+、
 、H2O和一种未知离子X
、H2O和一种未知离子X①已知
 在反应中得到电子,则X是
在反应中得到电子,则X是②该反应的离子方程式是
您最近一年使用:0次
解题方法
3 . 煤的气化是煤炭综合利用的重要途径之一,主要反应为C+H2O(g)  CO+H2。
CO+H2。
(1)该反应中,化合价升高的元素是___________ (填元素符号),氧化剂是___________ (填化学式),氧化产物是___________ (填化学式)。
(2)若消耗了1 mol C,则生成CO的体积约是___________ L(标准状况),转移电子的物质的量为___________ mol。
 CO+H2。
CO+H2。(1)该反应中,化合价升高的元素是
(2)若消耗了1 mol C,则生成CO的体积约是
您最近一年使用:0次
名校
4 . 生命体中,各种物质的结构和功能都与基础化学密切相关。磷脂和蛋白质就是其中的重要代表。
磷脂双层膜是由两亲性的磷脂分子以“尾部朝里,头朝外”的方式组成的双层膜结构,它起到对细胞进行包裹保护以及对物质进行选择性传递的作用。构成该双层膜结构的磷脂分子和磷脂双层膜结构的示意图以及其相关的脂质体如图所示。
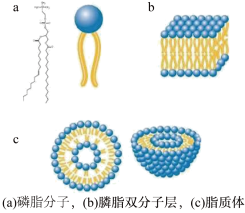
称取786.1mg磷脂分子(式量786.1),制备成1.000mL脂质体水溶液。取10.00μL该溶液,测得其中含有m个脂质体颗粒,直径为100nm。假设所有磷脂分子都形成了脂质体,计算脂质体外表面磷脂分子的排布密度______ (单位:个·m-2)。提示:1μL=10-3mL;球表面积公式S=4πr2(r为脂质体半径)
磷脂双层膜是由两亲性的磷脂分子以“尾部朝里,头朝外”的方式组成的双层膜结构,它起到对细胞进行包裹保护以及对物质进行选择性传递的作用。构成该双层膜结构的磷脂分子和磷脂双层膜结构的示意图以及其相关的脂质体如图所示。

称取786.1mg磷脂分子(式量786.1),制备成1.000mL脂质体水溶液。取10.00μL该溶液,测得其中含有m个脂质体颗粒,直径为100nm。假设所有磷脂分子都形成了脂质体,计算脂质体外表面磷脂分子的排布密度
您最近一年使用:0次
名校
5 . CO、C2H6均为常见的可燃性气体。
(1)等体积的CO和C2H6在相同条件下分别完全燃烧,转移的电子数之比是______ 。
(2)120℃、101kPa下,amL由CO、C2H6组成的混合气体在bmLO2中完全燃烧后,产物为CO2和H2O,恢复到原温度和压强。
①若混合气体与O2恰好完全反应,产生bmLCO2,则混合气体中C2H6的体积分数为______ 。
②若将燃烧后气体冷却至室温,反应后气体体积缩小了cmL,混合气体中C2H6体积是______ mL。(忽略温度下降,气体摩尔体积的变化)
(1)等体积的CO和C2H6在相同条件下分别完全燃烧,转移的电子数之比是
(2)120℃、101kPa下,amL由CO、C2H6组成的混合气体在bmLO2中完全燃烧后,产物为CO2和H2O,恢复到原温度和压强。
①若混合气体与O2恰好完全反应,产生bmLCO2,则混合气体中C2H6的体积分数为
②若将燃烧后气体冷却至室温,反应后气体体积缩小了cmL,混合气体中C2H6体积是
您最近一年使用:0次
名校
6 . Ⅰ.工业上常用电解 溶液制备
溶液制备 ,反应方程式如下:
,反应方程式如下: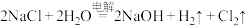 。回答下列问题:
。回答下列问题:
(1)用 的
的 溶液进行电解制备
溶液进行电解制备 。
。
①该 溶液中
溶液中 的物质的量是
的物质的量是_______  ;
;
②标准状况下,理论上最多能产生
_______ L;
③该反应中两种气体产物的质量比是_______ ;
④当 恰好完全反应时,停止电解,把所得溶液稀释到
恰好完全反应时,停止电解,把所得溶液稀释到 ,则所得
,则所得 溶液的物质的量浓度为
溶液的物质的量浓度为_______  。
。
(2)写出该反应的离子方程式_______ 。
Ⅱ.我国科学家用 人工合成淀粉时,第一步需要将
人工合成淀粉时,第一步需要将 转化为甲醇,反应的化学方程式为:
转化为甲醇,反应的化学方程式为: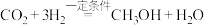 。
。
(3)做还原剂的物质是_______ ;
(4)反应中每生成 ,消耗
,消耗 的物质的量是
的物质的量是_______  ,转移电子的物质的量是
,转移电子的物质的量是_______  。
。
(5)对于反应: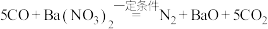 。
。
①发生还原反应的物质为_______ ;
②若有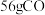 参与反应,则反应中转移的电子的物质的量为
参与反应,则反应中转移的电子的物质的量为_______  。
。
 溶液制备
溶液制备 ,反应方程式如下:
,反应方程式如下: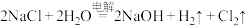 。回答下列问题:
。回答下列问题:(1)用
 的
的 溶液进行电解制备
溶液进行电解制备 。
。①该
 溶液中
溶液中 的物质的量是
的物质的量是 ;
;②标准状况下,理论上最多能产生

③该反应中两种气体产物的质量比是
④当
 恰好完全反应时,停止电解,把所得溶液稀释到
恰好完全反应时,停止电解,把所得溶液稀释到 ,则所得
,则所得 溶液的物质的量浓度为
溶液的物质的量浓度为 。
。(2)写出该反应的离子方程式
Ⅱ.我国科学家用
 人工合成淀粉时,第一步需要将
人工合成淀粉时,第一步需要将 转化为甲醇,反应的化学方程式为:
转化为甲醇,反应的化学方程式为: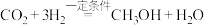 。
。(3)做还原剂的物质是
(4)反应中每生成
 ,消耗
,消耗 的物质的量是
的物质的量是 ,转移电子的物质的量是
,转移电子的物质的量是 。
。(5)对于反应:
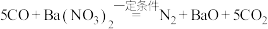 。
。①发生还原反应的物质为
②若有
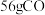 参与反应,则反应中转移的电子的物质的量为
参与反应,则反应中转移的电子的物质的量为 。
。
您最近一年使用:0次
7 . 请回答下列问题:
(1)8g CH4的物质的量是___________ mol,含有___________ 个甲烷分子,___________ 个电子;
(2)标准状况下,___________ g O2和2mol CO2占有相同的体积,均为___________ L;
(3)相同条件下,等质量的CH4和O2所含的原子个数之比为___________ ,密度之比为___________ 。
(4)向2.84g Na2SO4中加水至100mL,所得Na2SO4溶液的物质的量浓度为___________ ,取出20mL,所含Na+的物质的量浓度为___________ , 的数量为
的数量为___________ 。
(1)8g CH4的物质的量是
(2)标准状况下,
(3)相同条件下,等质量的CH4和O2所含的原子个数之比为
(4)向2.84g Na2SO4中加水至100mL,所得Na2SO4溶液的物质的量浓度为
 的数量为
的数量为
您最近一年使用:0次
名校
解题方法
8 . 书写下列化学方程式
(1)下图是1mol 和1molCO反应生成
和1molCO反应生成 和NO过程中能量变化示意图,请写出
和NO过程中能量变化示意图,请写出 和CO反应的热化学方程式
和CO反应的热化学方程式_______ 。

(2)已知拆开1mol H-H键、1mol 和1mol N-H键分别需要的能量是436kJ、948kJ、391kJ,则
和1mol N-H键分别需要的能量是436kJ、948kJ、391kJ,则 、
、 合成
合成 的热化学方程式为:
的热化学方程式为:_______ 。
(3)氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。甲烷水蒸气催化重整是制高纯氢的方法之一,已知存在如下反应:
ⅰ.

ⅱ.

ⅲ.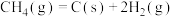

……
ⅲ为积炭反应,利用 和
和 计算
计算 时,还需要利用
时,还需要利用_______ 反应的△H。
(1)下图是1mol
 和1molCO反应生成
和1molCO反应生成 和NO过程中能量变化示意图,请写出
和NO过程中能量变化示意图,请写出 和CO反应的热化学方程式
和CO反应的热化学方程式
(2)已知拆开1mol H-H键、1mol
 和1mol N-H键分别需要的能量是436kJ、948kJ、391kJ,则
和1mol N-H键分别需要的能量是436kJ、948kJ、391kJ,则 、
、 合成
合成 的热化学方程式为:
的热化学方程式为:(3)氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。甲烷水蒸气催化重整是制高纯氢的方法之一,已知存在如下反应:
ⅰ.


ⅱ.


ⅲ.
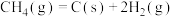

……
ⅲ为积炭反应,利用
 和
和 计算
计算 时,还需要利用
时,还需要利用
您最近一年使用:0次
名校
解题方法
9 . 某磁黄铁矿的主要成分是FexS(S为=-2价),磁黄铁矿中既含有二价铁又含有三价铁。将一定量的该磁黄铁矿与盐酸完全反应(注:矿石中其他成分不与盐酸反应),生成1.6g硫单质、0.45molFeCl2和一定量H2S气体,且溶液中滴加KSCN溶液不变血红色。请计算并回答下列问题:
(1)该磁黄铁矿FexS中,Fe2+(二价铁)与Fe3+(三价铁)的物质的量之比为_______ 。
(2)该磁黄铁矿FexS中,x=_______ 。
(1)该磁黄铁矿FexS中,Fe2+(二价铁)与Fe3+(三价铁)的物质的量之比为
(2)该磁黄铁矿FexS中,x=
您最近一年使用:0次
22-23高二上·北京西城·期中
名校
解题方法
10 . 弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属化学平衡。
I.填空。
(1)向NaCN溶液中通入少量的CO2,发生反应的离子方程式为_______ 。(已知 )
)
(2)某温度下,水的离子积常数KW=1×10-12。将此温度下pH=11的NaOH溶液aL与pH=1的bLH2SO4溶液混合,若所得混合液pH=2,则a:b=_______
II.已知H2A在水中存在以下平衡:H2A=H++HA-,HA- A2-+H+。
A2-+H+。
(3)常温下 溶液的pH
溶液的pH_______ (填序号),仅用化学用语解释原因_______ 。
A.大于7 B.小于7 C.等于7 D.无法确定
(4)已知常温下H2A的钙盐(CaA)的饱和溶液中存在以下平衡: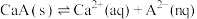
 。若要使该溶液中Ca2+浓度变小,可采取的措施有_______。
。若要使该溶液中Ca2+浓度变小,可采取的措施有_______。
III.
(5)某工业废水中主要含有Fe3+与Cr3+,毒性较大,若使用调节溶液pH的方法处理后的废水中残留的c(Fe3+)=2.0×10-13mol∙L-1,则残留的Cr3+的浓度为_______ (已知:Ksp[Fe(OH)3]= 4.0×10-38,Ksp[Cr(OH)3]= 6.0×10-31)。
I.填空。
(1)向NaCN溶液中通入少量的CO2,发生反应的离子方程式为
 )
)(2)某温度下,水的离子积常数KW=1×10-12。将此温度下pH=11的NaOH溶液aL与pH=1的bLH2SO4溶液混合,若所得混合液pH=2,则a:b=
II.已知H2A在水中存在以下平衡:H2A=H++HA-,HA-
 A2-+H+。
A2-+H+。(3)常温下
 溶液的pH
溶液的pHA.大于7 B.小于7 C.等于7 D.无法确定
(4)已知常温下H2A的钙盐(CaA)的饱和溶液中存在以下平衡:
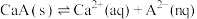
 。若要使该溶液中Ca2+浓度变小,可采取的措施有_______。
。若要使该溶液中Ca2+浓度变小,可采取的措施有_______。| A.升高温度 | B.降低温度 | C.加入NH4Cl晶体 | D.加入Na2A固体 |
III.
(5)某工业废水中主要含有Fe3+与Cr3+,毒性较大,若使用调节溶液pH的方法处理后的废水中残留的c(Fe3+)=2.0×10-13mol∙L-1,则残留的Cr3+的浓度为
您最近一年使用:0次



