1 . 亚硝酸钠( )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____ ___
___ ___=___
___=___ ___
___ ___
___ ___
___ ___
___ 。
。
(1)请完成该离子方程式并配平___________ 。
(2)从物质分类角度来看, 是
是___________ (填字母代号)。
a.酸 b.酸式盐 c.碱 d.非电解质 e.电解质 f.钠盐
(3)用上述反应来处理 开不是最佳方法,其原因是
开不是最佳方法,其原因是___________ 。从环保角度来讲,要将 转化为氮气,所用物质的
转化为氮气,所用物质的___________ 填“氧化性”或“还原性”)应该比KI更___________ (填“强”或“弱”)。
(4)下列方法不能用来区分固体 和NaCl的是___________(填序号)
和NaCl的是___________(填序号)
(5)误食 会导致人体血红蛋白中的
会导致人体血红蛋白中的 车转化为
车转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列:
表现出的性质与下列:___________ (填序号)反应中 表现出的性质相同。
表现出的性质相同。
A.
B.
C.
(6) 可以与
可以与 反应制备
反应制备 纳米颗粒。若
纳米颗粒。若 与
与 的系数之比为1∶2,配平该反应的离子方程式:
的系数之比为1∶2,配平该反应的离子方程式:___________ 。
____ _____
_____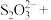 _____
_____ ____
____ ____
____ ______
______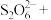 _____
_____
 )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____ ___
___ ___=___
___=___ ___
___ ___
___ ___
___ ___
___ 。
。(1)请完成该离子方程式并配平
(2)从物质分类角度来看,
 是
是a.酸 b.酸式盐 c.碱 d.非电解质 e.电解质 f.钠盐
(3)用上述反应来处理
 开不是最佳方法,其原因是
开不是最佳方法,其原因是 转化为氮气,所用物质的
转化为氮气,所用物质的(4)下列方法不能用来区分固体
 和NaCl的是___________(填序号)
和NaCl的是___________(填序号)| A.分别溶于水,滴加酚酞试液 | B.分别溶于水并滴加 酸化的 酸化的 溶液 溶液 |
| C.分别加强热并收集气体检验 | D.用筷子分别蘸取固体品尝味道 |
 会导致人体血红蛋白中的
会导致人体血红蛋白中的 车转化为
车转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列:
表现出的性质与下列: 表现出的性质相同。
表现出的性质相同。A.

B.

C.

(6)
 可以与
可以与 反应制备
反应制备 纳米颗粒。若
纳米颗粒。若 与
与 的系数之比为1∶2,配平该反应的离子方程式:
的系数之比为1∶2,配平该反应的离子方程式:____
 _____
_____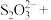 _____
_____ ____
____ ____
____ ______
______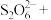 _____
_____
您最近一年使用:0次
名校
2 . (1)3.01×1023个OH-的物质的量为_______ ,含有电子的物质的量为_______ ,这些OH-和_______ g的Na+含有的电子数相同。
(2)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、 ,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c(
,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c( )=
)=_______ 。
(3)实验室可用KMnO4和浓盐酸反应制取氯气。其变化可表述为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
①请将上述化学方程式改写为离子方程式_______ 。
②浓盐酸在反应中显示出来的性质是_______ (填字母)。
a.只有还原性 b.还原性和酸性 c.只有氧化性 d.氧化性和酸性
③此反应中氧化产物是_______ (填化学式),还原性Cl-______ Mn2+(填>、<或=)。
④用双线桥法表示该反应电子转移的方向和数目:_______ 。
(2)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、
 ,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c(
,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c( )=
)=(3)实验室可用KMnO4和浓盐酸反应制取氯气。其变化可表述为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
①请将上述化学方程式改写为离子方程式
②浓盐酸在反应中显示出来的性质是
a.只有还原性 b.还原性和酸性 c.只有氧化性 d.氧化性和酸性
③此反应中氧化产物是
④用双线桥法表示该反应电子转移的方向和数目:
您最近一年使用:0次
3 . 近来,《饮用天然矿泉水》新标准引起热议,其中备受争议的溴酸盐是一种致癌物,新标准中溴酸盐极值为0.01mg/L。已知在酸性条件下有以下反应:
①2 +I2===2
+I2===2 +Br2
+Br2
②2 +10Br-+12H+===I2+5Br2+6H2O
+10Br-+12H+===I2+5Br2+6H2O
③5Br-+ +6H+===3Br2+3H2O
+6H+===3Br2+3H2O
请回答下列问题:
(1)有同学根据反应①得出氧化性:I2>Br2的结论,请说明该结论错误的理由是:_________ 。
(2)反应②中: →l2发生的是
→l2发生的是__________ 反应(氧化、还原)。
现向含6mol的KI的硫酸溶液中逐滴滴加KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量有如图的关系:
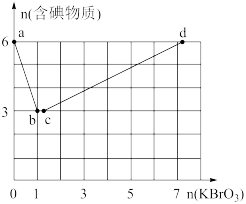
(3)完成a→b阶段的反应方程式,并标出电子转移的方向和数目:I-+BrO3-+H+→ ,________ 。
(4)b→c阶段只有一种元素化合价发生了改变,反应中氧化产物和还原产物的物质的量之比为______ 。
(5)a→b、b→c、c→d阶段的还原剂分别是______ 、_______ 、______ ,依次发生的这些反应,说明有关物质(l2、Br2、I-、Br-)还原性由强到弱的顺序是________ 。
①2
 +I2===2
+I2===2 +Br2
+Br2②2
 +10Br-+12H+===I2+5Br2+6H2O
+10Br-+12H+===I2+5Br2+6H2O③5Br-+
 +6H+===3Br2+3H2O
+6H+===3Br2+3H2O请回答下列问题:
(1)有同学根据反应①得出氧化性:I2>Br2的结论,请说明该结论错误的理由是:
(2)反应②中:
 →l2发生的是
→l2发生的是现向含6mol的KI的硫酸溶液中逐滴滴加KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量有如图的关系:

(3)完成a→b阶段的反应方程式,并标出电子转移的方向和数目:I-+BrO3-+H+→ ,
(4)b→c阶段只有一种元素化合价发生了改变,反应中氧化产物和还原产物的物质的量之比为
(5)a→b、b→c、c→d阶段的还原剂分别是
您最近一年使用:0次
19-20高三·浙江·阶段练习
4 . 工业次氯酸钠溶液中含有氯酸钠,测定次氯酸钠样品中的氯酸钠含量的方法如下:取10.00 mL碱性NaClO溶液试样,加入过量H2O2,将次氯酸钠完全还原为氯化钠(ClO 在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性)。加热煮沸,冷却至室温,加入硫酸至酸性,再加入0.1000 mol/L硫酸亚铁标准溶液30.00 mL,充分反应后,用0.01000 mol/L酸性K2Cr2O7溶液滴定至终点,消耗该溶液20.00 mL。已知:
在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性)。加热煮沸,冷却至室温,加入硫酸至酸性,再加入0.1000 mol/L硫酸亚铁标准溶液30.00 mL,充分反应后,用0.01000 mol/L酸性K2Cr2O7溶液滴定至终点,消耗该溶液20.00 mL。已知: +6Fe2++6H+=Cl-+6Fe3++3H2O;
+6Fe2++6H+=Cl-+6Fe3++3H2O; +6Fe2++14H+=2Cr3++6Fe3++7H2O
+6Fe2++14H+=2Cr3++6Fe3++7H2O
(1)与K2Cr2O7反应的硫酸亚铁的物质的量为_______ mol。
(2)计算样品中NaClO3的含量为_______ g/L,写出计算过程。
 在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性)。加热煮沸,冷却至室温,加入硫酸至酸性,再加入0.1000 mol/L硫酸亚铁标准溶液30.00 mL,充分反应后,用0.01000 mol/L酸性K2Cr2O7溶液滴定至终点,消耗该溶液20.00 mL。已知:
在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性)。加热煮沸,冷却至室温,加入硫酸至酸性,再加入0.1000 mol/L硫酸亚铁标准溶液30.00 mL,充分反应后,用0.01000 mol/L酸性K2Cr2O7溶液滴定至终点,消耗该溶液20.00 mL。已知: +6Fe2++6H+=Cl-+6Fe3++3H2O;
+6Fe2++6H+=Cl-+6Fe3++3H2O; +6Fe2++14H+=2Cr3++6Fe3++7H2O
+6Fe2++14H+=2Cr3++6Fe3++7H2O(1)与K2Cr2O7反应的硫酸亚铁的物质的量为
(2)计算样品中NaClO3的含量为
您最近一年使用:0次
5 . 请回答下列问题:
(1)已知实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为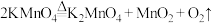 ,氧化产物是
,氧化产物是___________ (填化学式)。
(2)查阅资料可知,铜和浓 共热,发生反应
共热,发生反应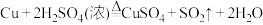 ,该反应中还原剂与氧化剂的物质的量之比为
,该反应中还原剂与氧化剂的物质的量之比为___________ ,其中 在反应中表现的性质为
在反应中表现的性质为___________ 。
(3)已知反应
① ;
;
②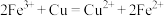 ;
;
③ ;
;
④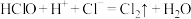 。
。
微粒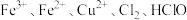 氧化性由强到弱的顺序为
氧化性由强到弱的顺序为___________
(4)请配平下列反应方程式:___________
___________ ___________
___________ (浓)=___________
(浓)=___________ ___________
___________ ___________
___________ ___________
___________
若反应中发生氧化反应的 物质的量为
物质的量为 ,则反应中转移的电子数为
,则反应中转移的电子数为___________ 。
(1)已知实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为
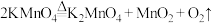 ,氧化产物是
,氧化产物是(2)查阅资料可知,铜和浓
 共热,发生反应
共热,发生反应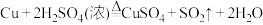 ,该反应中还原剂与氧化剂的物质的量之比为
,该反应中还原剂与氧化剂的物质的量之比为 在反应中表现的性质为
在反应中表现的性质为(3)已知反应
①
 ;
;②
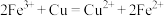 ;
;③
 ;
;④
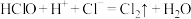 。
。微粒
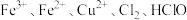 氧化性由强到弱的顺序为
氧化性由强到弱的顺序为(4)请配平下列反应方程式:
___________
 ___________
___________ (浓)=___________
(浓)=___________ ___________
___________ ___________
___________ ___________
___________
若反应中发生氧化反应的
 物质的量为
物质的量为 ,则反应中转移的电子数为
,则反应中转移的电子数为
您最近一年使用:0次
解题方法
6 . 大多数植物不能从空气中摄取氮,农作物生长需要通过合成氨,进行人工固氮。合成氨的某种催化剂P,主要成分为二价铁和三价铁的氧化物按一定比例形成的混合物。
(1)铁、氧的物质的量之比为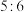 的由
的由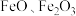 组成的混合物中,
组成的混合物中, 与
与 的物质的量之比为
的物质的量之比为_______ 。
(2)兴趣小组查阅相关资料,发现该合成氨催化剂活性最高时,催化剂P中 与
与 的物质的量之比为
的物质的量之比为 ,则此时该铁的氧化物混合物的平均摩尔质量为
,则此时该铁的氧化物混合物的平均摩尔质量为_______ ,其中氧元素的质量分数为_______ (保留2位有效数字)。
(3)兴趣小组发现以 为原料制备此催化剂的化学方程式为
为原料制备此催化剂的化学方程式为 。为制得这种活性最高的催化剂,理论上应向
。为制得这种活性最高的催化剂,理论上应向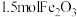 粉末中加入炭粉的质量为
粉末中加入炭粉的质量为_______ ,完全反应时生成 的体积为
的体积为_______ (折算成标准状况下)。
(4) 为剧毒物质,处理含有
为剧毒物质,处理含有 的废水常用的方法为在碱性条件下用
的废水常用的方法为在碱性条件下用 溶液将
溶液将 氧化为
氧化为 和一种单质气体,则该反应的离子方程式为
和一种单质气体,则该反应的离子方程式为_______ 。
(1)铁、氧的物质的量之比为
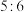 的由
的由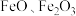 组成的混合物中,
组成的混合物中, 与
与 的物质的量之比为
的物质的量之比为(2)兴趣小组查阅相关资料,发现该合成氨催化剂活性最高时,催化剂P中
 与
与 的物质的量之比为
的物质的量之比为 ,则此时该铁的氧化物混合物的平均摩尔质量为
,则此时该铁的氧化物混合物的平均摩尔质量为(3)兴趣小组发现以
 为原料制备此催化剂的化学方程式为
为原料制备此催化剂的化学方程式为 。为制得这种活性最高的催化剂,理论上应向
。为制得这种活性最高的催化剂,理论上应向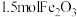 粉末中加入炭粉的质量为
粉末中加入炭粉的质量为 的体积为
的体积为(4)
 为剧毒物质,处理含有
为剧毒物质,处理含有 的废水常用的方法为在碱性条件下用
的废水常用的方法为在碱性条件下用 溶液将
溶液将 氧化为
氧化为 和一种单质气体,则该反应的离子方程式为
和一种单质气体,则该反应的离子方程式为
您最近一年使用:0次
名校
解题方法
7 . 根据所学知识完成下列问题
(1)铁钉浸入CuSO4溶液后,表面会附有铜,铜丝浸入AgNO3溶液后,表面会附有银。则Cu、Fe、Ag中,___________ 的还原性最强,Cu2+、Fe2+、Ag+中,___________ 的氧化性最强。
(2)火药是中国的四大发明之一,永远值得中华儿女骄傲。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。其中氧化产物是___________ 。(填化学式)
(3)在K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O中,还原剂是___________ ,氧化剂与还原剂的物质的量之比为___________ 。
(1)铁钉浸入CuSO4溶液后,表面会附有铜,铜丝浸入AgNO3溶液后,表面会附有银。则Cu、Fe、Ag中,
(2)火药是中国的四大发明之一,永远值得中华儿女骄傲。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。其中氧化产物是
(3)在K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O中,还原剂是
您最近一年使用:0次
名校
解题方法
8 . 移取20.00 两种一元弱酸
两种一元弱酸 和
和 的混合溶液,滴加0.1
的混合溶液,滴加0.1 的
的 至反应终点,消耗25
至反应终点,消耗25 。再取相同的上述溶液,加入50
。再取相同的上述溶液,加入50 ,0.02
,0.02
 的强碱性溶液,待其反应完成后,将溶液酸化,加入30
的强碱性溶液,待其反应完成后,将溶液酸化,加入30 0.2
0.2
 溶液,将剩余的
溶液,将剩余的 和
和 歧化生成的
歧化生成的 和
和 全部还原至
全部还原至 ,剩余的
,剩余的 溶液用上述
溶液用上述 溶液在酸性条件下反应至终点消耗18.5
溶液在酸性条件下反应至终点消耗18.5 。
。
已知:
① 在强碱性条件下还原产物为
在强碱性条件下还原产物为 ;
; 在酸性条件发生歧化反应;
在酸性条件发生歧化反应;
② 具有还原性,酸性条件下被氧化为
具有还原性,酸性条件下被氧化为 ,
, 不能被酸性高锰酸钾氧化
不能被酸性高锰酸钾氧化
(1)加入 的强碱性溶液发生的有电子转移的离子反应方程式为
的强碱性溶液发生的有电子转移的离子反应方程式为_______ 。
(2)酸化后 歧化发生离子反应方程式为
歧化发生离子反应方程式为_______ 。
(3)加入 溶液后发生反应的离子方程式为
溶液后发生反应的离子方程式为_______ 。
(4)则溶液中的 的浓度为
的浓度为_______ ; 的浓度为
的浓度为_______ 。
(5)若溶液酸化后将 过滤除掉,其它操作不变,则测得的
过滤除掉,其它操作不变,则测得的 浓度将
浓度将_______ (填“偏大”、“偏小”或“不变”)。
 两种一元弱酸
两种一元弱酸 和
和 的混合溶液,滴加0.1
的混合溶液,滴加0.1 的
的 至反应终点,消耗25
至反应终点,消耗25 。再取相同的上述溶液,加入50
。再取相同的上述溶液,加入50 ,0.02
,0.02
 的强碱性溶液,待其反应完成后,将溶液酸化,加入30
的强碱性溶液,待其反应完成后,将溶液酸化,加入30 0.2
0.2
 溶液,将剩余的
溶液,将剩余的 和
和 歧化生成的
歧化生成的 和
和 全部还原至
全部还原至 ,剩余的
,剩余的 溶液用上述
溶液用上述 溶液在酸性条件下反应至终点消耗18.5
溶液在酸性条件下反应至终点消耗18.5 。
。已知:
①
 在强碱性条件下还原产物为
在强碱性条件下还原产物为 ;
; 在酸性条件发生歧化反应;
在酸性条件发生歧化反应;②
 具有还原性,酸性条件下被氧化为
具有还原性,酸性条件下被氧化为 ,
, 不能被酸性高锰酸钾氧化
不能被酸性高锰酸钾氧化(1)加入
 的强碱性溶液发生的有电子转移的离子反应方程式为
的强碱性溶液发生的有电子转移的离子反应方程式为(2)酸化后
 歧化发生离子反应方程式为
歧化发生离子反应方程式为(3)加入
 溶液后发生反应的离子方程式为
溶液后发生反应的离子方程式为(4)则溶液中的
 的浓度为
的浓度为 的浓度为
的浓度为(5)若溶液酸化后将
 过滤除掉,其它操作不变,则测得的
过滤除掉,其它操作不变,则测得的 浓度将
浓度将
您最近一年使用:0次
解题方法
9 . 3.84 g Fe和Fe2O3的混合物溶于100 mL某浓度的盐酸中,恰好使混合物溶解,生成0.03 mol H2,向反应后的溶液中加入KSCN检验,溶液无明显现象,设HCl无挥发,反应后溶液的体积不变。(已知:氧化性Fe3+>H+,还原性Fe>Cl-)
(1)求标准状况下生成氢气的体积______ ?
(2)求反应后Cl-的物质的量浓度_______ ?
(1)求标准状况下生成氢气的体积
(2)求反应后Cl-的物质的量浓度
您最近一年使用:0次
名校
解题方法
10 . 重铬酸钾(K2Cr2O7)具有强氧化性,在实验室和工业中都有很广泛的应用。其主要应用之一是配制铬酸洗液(重铬酸钾、水和浓硫酸按照一定比例配制成的溶液)。根据所学知识,回答下列问题:
(1) K2Cr2O7中Cr的化合价为_______ 价,属于_______ (填“酸”、“碱”或“盐”)。
(2)当铬酸洗液变绿[溶液中K2Cr2O7转化成Cr2(SO4)3]失效时,将失效的铬酸洗液进行加热浓缩,冷却后加入KMnO4粉末氧化,滤去MnO2后可实现铬酸洗液的再生,其中加入KMnO4粉末氧化时发生反应的离子方程式为_______ (用单线桥法标明电子转移的方向和数目);滤去MnO2时,可采用过滤操作,过滤需要用到的玻璃仪器有_______ 。
(3)当铬酸洗液变黑失效时,可在酸性条件下加入铁屑将残留的K2Cr2O7转化成Cr2(SO4)3,铁屑自身转化成Fe3+,再用石灰石将铬元素转化成Cr(OH)3沉淀,其中铁屑将 转化成Cr3+的离子方程式为
转化成Cr3+的离子方程式为_______ ;若黑色铬酸洗液中 ,则处理1L该黑色铬酸洗液时,所需的铁屑的质量为
,则处理1L该黑色铬酸洗液时,所需的铁屑的质量为_______ g。
(4)酸性 K2Cr2O7溶液还可以用来测定铁矿石中铁(以+2价形式存在,铁的含量为x%)的含量,称取铁矿石试样(含Fe2+,设其他物质不与K2Cr2O7反应)0.4g,若加入的酸性K2Cr2O7溶液的体积为x mL,则K2Cr2O7的浓度为_______ g∙L-1。
(1) K2Cr2O7中Cr的化合价为
(2)当铬酸洗液变绿[溶液中K2Cr2O7转化成Cr2(SO4)3]失效时,将失效的铬酸洗液进行加热浓缩,冷却后加入KMnO4粉末氧化,滤去MnO2后可实现铬酸洗液的再生,其中加入KMnO4粉末氧化时发生反应的离子方程式为
(3)当铬酸洗液变黑失效时,可在酸性条件下加入铁屑将残留的K2Cr2O7转化成Cr2(SO4)3,铁屑自身转化成Fe3+,再用石灰石将铬元素转化成Cr(OH)3沉淀,其中铁屑将
 转化成Cr3+的离子方程式为
转化成Cr3+的离子方程式为 ,则处理1L该黑色铬酸洗液时,所需的铁屑的质量为
,则处理1L该黑色铬酸洗液时,所需的铁屑的质量为(4)酸性 K2Cr2O7溶液还可以用来测定铁矿石中铁(以+2价形式存在,铁的含量为x%)的含量,称取铁矿石试样(含Fe2+,设其他物质不与K2Cr2O7反应)0.4g,若加入的酸性K2Cr2O7溶液的体积为x mL,则K2Cr2O7的浓度为
您最近一年使用:0次
2022-11-11更新
|
377次组卷
|
2卷引用:湖南省金太阳联考2022-2023学年高一上学期期中考试化学试题



