名校
解题方法
1 . 硼元素有两种同位素: (相对原子质量10.0129,丰度19.78%)和
(相对原子质量10.0129,丰度19.78%)和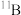 (相对原子质量11.00931,丰度80.22%)。请列式计算硼元素的相对原子质量(计算结果保留至小数点后两位)
(相对原子质量11.00931,丰度80.22%)。请列式计算硼元素的相对原子质量(计算结果保留至小数点后两位)___________ 。
 (相对原子质量10.0129,丰度19.78%)和
(相对原子质量10.0129,丰度19.78%)和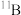 (相对原子质量11.00931,丰度80.22%)。请列式计算硼元素的相对原子质量(计算结果保留至小数点后两位)
(相对原子质量11.00931,丰度80.22%)。请列式计算硼元素的相对原子质量(计算结果保留至小数点后两位)
您最近一年使用:0次
名校
解题方法
2 . 用氨水吸收 ,得到
,得到 氨水和
氨水和 甲酸铵的混合溶液,
甲酸铵的混合溶液, 时该混合溶液的
时该混合溶液的
___________ 。(已知: 时,电离常数
时,电离常数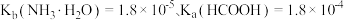 )
)
 ,得到
,得到 氨水和
氨水和 甲酸铵的混合溶液,
甲酸铵的混合溶液, 时该混合溶液的
时该混合溶液的
 时,电离常数
时,电离常数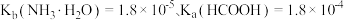 )
)
您最近一年使用:0次
3 . 常温时,用石墨电极电解500mLNaCl和CuSO4混合溶液,当电路中通过2mol电子时,两极均产生标准状况下16.8L气体,其中阳极产生的O2在标准状况下是5.6L(假定产生的气体全部放出,电解前后溶液体积变化忽略不计),求:
(1)原溶液中c(NaCl)=___________ ,c(CuSO4)=___________ 。
(2)电解后溶液的c(OH-)=___________ 。
(1)原溶液中c(NaCl)=
(2)电解后溶液的c(OH-)=
您最近一年使用:0次
名校
4 . 已知水在100℃时,Kw=10-12。
(1)在100℃下,某溶液中由水电离产生的c(H+)=1×10-9,则该溶液的pH=_______ 。
(2)100℃时,某BaCl2溶液中c(Cl-)=2×10-2 mol·L-1,取该溶液1mL加水稀释至100mL,则稀释后溶液中c(Ba2+)∶c(H+)=____ 。
(3)100℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是_____ 。
(4)100℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=6,则NaOH溶液与H2SO4溶液的体积比为_____ 。
(5)常温下,将0.02mol·L-1的Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合,所得混合液的pH=_____ 。
(6)已知HA的Ka=1×10-5,常温下,取V1 L pH=3的HA溶液与V2 L pH=11的NaOH溶液混合,若混合后溶液pH=7,则大小关系:V1____ V2(填“大于”“小于”或“等于”)。
(7)常温下,将a mol·L-1NaOH溶液和b mol·L-1醋酸溶液等体积混合,反应后溶液恰好显中性,醋酸的电离平衡常数为______ (用a、b表示)。
(8)常温下,甲、乙两烧杯中分别有等体积pH=2和pH=3的HA溶液,加入等浓度的NaOH溶液,恰好完全反应时,消耗的NaOH溶液的体积:V甲____ 10V乙(填“大于”“小于”或“等于”)。
(1)在100℃下,某溶液中由水电离产生的c(H+)=1×10-9,则该溶液的pH=
(2)100℃时,某BaCl2溶液中c(Cl-)=2×10-2 mol·L-1,取该溶液1mL加水稀释至100mL,则稀释后溶液中c(Ba2+)∶c(H+)=
(3)100℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是
(4)100℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=6,则NaOH溶液与H2SO4溶液的体积比为
(5)常温下,将0.02mol·L-1的Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合,所得混合液的pH=
(6)已知HA的Ka=1×10-5,常温下,取V1 L pH=3的HA溶液与V2 L pH=11的NaOH溶液混合,若混合后溶液pH=7,则大小关系:V1
(7)常温下,将a mol·L-1NaOH溶液和b mol·L-1醋酸溶液等体积混合,反应后溶液恰好显中性,醋酸的电离平衡常数为
(8)常温下,甲、乙两烧杯中分别有等体积pH=2和pH=3的HA溶液,加入等浓度的NaOH溶液,恰好完全反应时,消耗的NaOH溶液的体积:V甲
您最近一年使用:0次
解题方法
5 . 已知几种含碳物质间的转化及能量变化关系如图所示。

(1)写出表示 燃烧热的热化学方程式:
燃烧热的热化学方程式:___________ ,若有672mL(标准状况下) 完全燃烧,会放出
完全燃烧,会放出___________ kJ能量。
(2)反应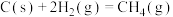
 =
=___________ kJ⋅mol-1,该反应中反应物的总键能___________ (填“大于”、“小于”或“等于”)生成物的总键能;若18gC(s)与 反应,完全转化成
反应,完全转化成 ,需要
,需要___________ (填“吸收”或“放出”)___________ kJ能量。
(3)在25℃、101kPa下,30g由 和
和 组成的混合气体完全燃烧生成
组成的混合气体完全燃烧生成 和液态水,放出热量1031.8kJ,则混合气体中
和液态水,放出热量1031.8kJ,则混合气体中 和
和 的物质的量分别为
的物质的量分别为___________ mol、___________ mol。

(1)写出表示
 燃烧热的热化学方程式:
燃烧热的热化学方程式: 完全燃烧,会放出
完全燃烧,会放出(2)反应
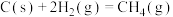
 =
= 反应,完全转化成
反应,完全转化成 ,需要
,需要(3)在25℃、101kPa下,30g由
 和
和 组成的混合气体完全燃烧生成
组成的混合气体完全燃烧生成 和液态水,放出热量1031.8kJ,则混合气体中
和液态水,放出热量1031.8kJ,则混合气体中 和
和 的物质的量分别为
的物质的量分别为
您最近一年使用:0次
名校
解题方法
6 . 完成下列计算:
(1)已知工业上制取硫酸需要发生以下反应
Ⅰ. ;Ⅱ.
;Ⅱ.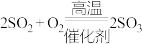 ;Ⅲ.
;Ⅲ.
①假设在生产中所有反应完全进行,则每生产1.00吨98%的浓硫酸需要
______ 吨。(保留2位小数)
②实际生产中可能会有损耗(即存在反应物没有发生反应),假设反应Ⅰ中 损耗率为20%,反应Ⅱ中
损耗率为20%,反应Ⅱ中 损耗率为10%,则实际生产1吨98%浓硫酸需要
损耗率为10%,则实际生产1吨98%浓硫酸需要
______ 吨。(保留2位小数)
(2)取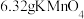 固体,加热一段时间后,剩余固体5.84g。该剩余固体与足量的浓盐酸在加热条件下充分反应生成氯气,产物中所有Mn元素均转化为
固体,加热一段时间后,剩余固体5.84g。该剩余固体与足量的浓盐酸在加热条件下充分反应生成氯气,产物中所有Mn元素均转化为 。
。
① 分解生成氧气的物质的量
分解生成氧气的物质的量
______ mol
② 分解的百分率为
分解的百分率为______ %;
③第二步反应中生成氯气的物质的量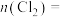
______ mol
(1)已知工业上制取硫酸需要发生以下反应
Ⅰ.
 ;Ⅱ.
;Ⅱ.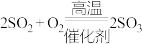 ;Ⅲ.
;Ⅲ.
①假设在生产中所有反应完全进行,则每生产1.00吨98%的浓硫酸需要

②实际生产中可能会有损耗(即存在反应物没有发生反应),假设反应Ⅰ中
 损耗率为20%,反应Ⅱ中
损耗率为20%,反应Ⅱ中 损耗率为10%,则实际生产1吨98%浓硫酸需要
损耗率为10%,则实际生产1吨98%浓硫酸需要
(2)取
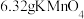 固体,加热一段时间后,剩余固体5.84g。该剩余固体与足量的浓盐酸在加热条件下充分反应生成氯气,产物中所有Mn元素均转化为
固体,加热一段时间后,剩余固体5.84g。该剩余固体与足量的浓盐酸在加热条件下充分反应生成氯气,产物中所有Mn元素均转化为 。
。①
 分解生成氧气的物质的量
分解生成氧气的物质的量
②
 分解的百分率为
分解的百分率为③第二步反应中生成氯气的物质的量
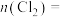
您最近一年使用:0次
2023-11-06更新
|
180次组卷
|
2卷引用:11-2023新东方高二上期中考化学11
7 . 回答下列问题
(1)已知 1g 甲烷完全燃烧生成二氧化碳和液态水释放 56kJ 的热量,则甲烷燃烧的热化学方程式___________ 。
(2)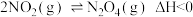 增大压强,平衡
增大压强,平衡___________ 填(“正向移动”“逆向移动”或“不移动”),颜色___________ (填“变深”“变浅”或“不变”)。
(3)工业制备纯硅的反应为 ,若将生成的HCl 通入 100mL1mol·L-1 的 NaOH 溶液中恰好完全反应,则此制备纯硅反应过程中的热效应是
,若将生成的HCl 通入 100mL1mol·L-1 的 NaOH 溶液中恰好完全反应,则此制备纯硅反应过程中的热效应是___________ kJ。
(1)已知 1g 甲烷完全燃烧生成二氧化碳和液态水释放 56kJ 的热量,则甲烷燃烧的热化学方程式
(2)
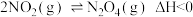 增大压强,平衡
增大压强,平衡(3)工业制备纯硅的反应为
 ,若将生成的HCl 通入 100mL1mol·L-1 的 NaOH 溶液中恰好完全反应,则此制备纯硅反应过程中的热效应是
,若将生成的HCl 通入 100mL1mol·L-1 的 NaOH 溶液中恰好完全反应,则此制备纯硅反应过程中的热效应是
您最近一年使用:0次
解题方法
8 . 将硝酸钠(NaNO3)和硝酸钡[Ba(NO3)2]的混合物29.1g放入烧杯,加入100.0g水使其完全溶解,再加入94.2g硫酸钠溶液恰好完全反应,过滤(忽略溶液的损失),称得滤液的质量为200.0g。请计算:
(1)恰好完全反应后产生的沉淀质量为______ g。
(2)所得滤液的溶质质量分数(写出完整的解题过程)________ 。
(1)恰好完全反应后产生的沉淀质量为
(2)所得滤液的溶质质量分数(写出完整的解题过程)
您最近一年使用:0次
解题方法
9 . 以甲烷为原料制取氢气是工业上常用的制氢方法。已知有关化学反应的能量变化如图所示:
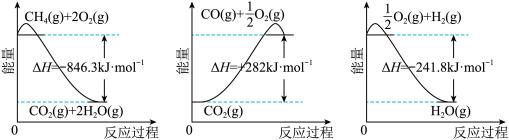
(1)下列说法正确的是___________(填字母)。
(2)CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为___________ 。

(1)下列说法正确的是___________(填字母)。
| A.CH4的摩尔燃烧焓为846.3 kJ·mol-1 |
| B.CO的摩尔燃烧焓为282 kJ·mol-1 |
| C.H2的摩尔燃烧焓为241.8 kJ·mol-1 |
| D.CO(g)+H2O(g)=CO2(g)+H2(g)为放热反应 |
您最近一年使用:0次
解题方法
10 . 回答下列问题:
(1)合成气(CO、H2)是一种重要的化工原料,在化工生产中具有十分广泛的用途。工业上用CO和H2合成CH3OH: △H。则该反应的平衡常数表达式为
△H。则该反应的平衡常数表达式为_______ ;
(2)测得不同温度下反应的平衡常数 如下表:
如下表:
下列说法错误的是_______。
(3)工业上,利用水煤气法制取合成气,其中发生的一步反应为:CO(g)+H2O(g) CO2(g)+H2(g) △H=-41.2kJ·mol-1。已知
CO2(g)+H2(g) △H=-41.2kJ·mol-1。已知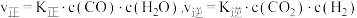 (k正、k逆为化学反应速率常数,只与温度有关,与浓度、压强无关)。830℃时,体积为2L的恒容密闭容器中,投入2molCO(g)和2molH2O(g)。5min达到平衡,测得H2的平均生成速率为0.1mol∙L-1∙min-1,则反应达到平衡后,速率常数
(k正、k逆为化学反应速率常数,只与温度有关,与浓度、压强无关)。830℃时,体积为2L的恒容密闭容器中,投入2molCO(g)和2molH2O(g)。5min达到平衡,测得H2的平均生成速率为0.1mol∙L-1∙min-1,则反应达到平衡后,速率常数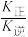 =
=_______ 。
(4)以天然气为原料生产合成气也有多种方法,其中Sparg工艺的原理为CH4(g)+CO2(g) 2CO(g)+2H2(g) △H1。T℃下,向容积可变的密闭容器中充入一定量的CH4(g)和CO2(g),改变容器体积,测得平衡时容器内气体的浓度如表所示:
2CO(g)+2H2(g) △H1。T℃下,向容积可变的密闭容器中充入一定量的CH4(g)和CO2(g),改变容器体积,测得平衡时容器内气体的浓度如表所示:
①T℃下,该反应的平衡常数K=_______ 。
②实验1中,CO的平衡体积分数为_______ %(保留三位有效数字)。
③V1:V2=_______ 。
(1)合成气(CO、H2)是一种重要的化工原料,在化工生产中具有十分广泛的用途。工业上用CO和H2合成CH3OH:
 △H。则该反应的平衡常数表达式为
△H。则该反应的平衡常数表达式为(2)测得不同温度下反应的平衡常数
 如下表:
如下表:| 温度/℃ | T1 | 100 | T2 | 200 | 300 |
| 平衡常数K | 100 | 13 | 1 | 1.9×10-2 | 2.4×10-4 |
| A.△H<0 |
| B.该反应的ΔS<0 |
| C.T2时,某时刻1L容器中含0.1mol CO、0.2mol H2和0.3mol CH3OH,此时v正>v逆 |
| D.T1时,向1L密闭容器中投入0.1mol CO和0.2mol H2,平衡时CO转化率为50% |
 CO2(g)+H2(g) △H=-41.2kJ·mol-1。已知
CO2(g)+H2(g) △H=-41.2kJ·mol-1。已知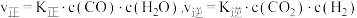 (k正、k逆为化学反应速率常数,只与温度有关,与浓度、压强无关)。830℃时,体积为2L的恒容密闭容器中,投入2molCO(g)和2molH2O(g)。5min达到平衡,测得H2的平均生成速率为0.1mol∙L-1∙min-1,则反应达到平衡后,速率常数
(k正、k逆为化学反应速率常数,只与温度有关,与浓度、压强无关)。830℃时,体积为2L的恒容密闭容器中,投入2molCO(g)和2molH2O(g)。5min达到平衡,测得H2的平均生成速率为0.1mol∙L-1∙min-1,则反应达到平衡后,速率常数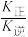 =
=(4)以天然气为原料生产合成气也有多种方法,其中Sparg工艺的原理为CH4(g)+CO2(g)
 2CO(g)+2H2(g) △H1。T℃下,向容积可变的密闭容器中充入一定量的CH4(g)和CO2(g),改变容器体积,测得平衡时容器内气体的浓度如表所示:
2CO(g)+2H2(g) △H1。T℃下,向容积可变的密闭容器中充入一定量的CH4(g)和CO2(g),改变容器体积,测得平衡时容器内气体的浓度如表所示:| 实验编号 | 容器体积 | 物质浓度/mol·L-1 | ||
| CH4 | CO2 | CO | ||
| 1 | V1 | 0.02 | 0.02 | 0.10 |
| 2 | V2 | x | x | 0.05 |
②实验1中,CO的平衡体积分数为
③V1:V2=
您最近一年使用:0次



