1 . 一定温度时,在 密闭容器中,某反应中的气体M和气体N的物质的量随时间变化的曲线如图所示:
密闭容器中,某反应中的气体M和气体N的物质的量随时间变化的曲线如图所示:___________ , 时刻N的转化率为
时刻N的转化率为___________ 。
(2)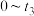 时间内用M表示的化学反应速率为
时间内用M表示的化学反应速率为___________  。
。
(3)下列能表示上述反应达到化学平衡状态的是___________(填编号)。
(4)已知:H—H的键能为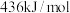 ,N—H的键能为
,N—H的键能为 ,生成
,生成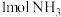 过程中放出
过程中放出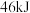 的热量。则
的热量。则 的键能为
的键能为___________  。
。
(5)化学反应速率受到很多因素的影响,例如:实验室制取氢气时一般用粗锌(含铁)代替纯锌和稀硫酸反应,这是利用___________ 原理加快了氢气生成的速率。
 密闭容器中,某反应中的气体M和气体N的物质的量随时间变化的曲线如图所示:
密闭容器中,某反应中的气体M和气体N的物质的量随时间变化的曲线如图所示: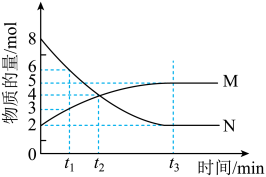
 时刻N的转化率为
时刻N的转化率为(2)
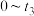 时间内用M表示的化学反应速率为
时间内用M表示的化学反应速率为 。
。(3)下列能表示上述反应达到化学平衡状态的是___________(填编号)。
A. | B.M与N的物质的量之比保持不变 |
| C.各物质浓度保持不变 | D.每消耗 ,同时生成 ,同时生成 |
(4)已知:H—H的键能为
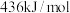 ,N—H的键能为
,N—H的键能为 ,生成
,生成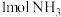 过程中放出
过程中放出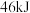 的热量。则
的热量。则 的键能为
的键能为 。
。(5)化学反应速率受到很多因素的影响,例如:实验室制取氢气时一般用粗锌(含铁)代替纯锌和稀硫酸反应,这是利用
您最近一年使用:0次
名校
2 . 硫脲 在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备
在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备 ,然后
,然后 再与CaCN2合成
再与CaCN2合成 ,实验装置(夹持及加热装置略)如图所示。
,实验装置(夹持及加热装置略)如图所示。 易溶于水,易被氧化,受热时部分发生异构化生成NH4SCN。
易溶于水,易被氧化,受热时部分发生异构化生成NH4SCN。
回答下列问题:
(1)实验前先检查装置气密性,操作为:①在E中加水至浸没导管末端,……;②微热A处三颈烧瓶,观察到E处导管末端有气泡冒出,移走酒精灯;③一段时间后,E处导管末端形成一段水柱,且高度不变。将操作①补充完整_______ 。
(2)检查气密性后加入药品,装置A中的试剂最佳组合是_______ (填字母),打开K2。
A.FeS固体+浓硫酸 B.FeS固体+稀硝酸 C.FeS固体+稀盐酸
装置B中盛装的试剂为_______ 。待A中反应结束后关闭K2,打开K1通N2一段时间,目的是_______ 。
(3)撤走搅拌器,打开K3,水浴加热D处三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温度在80℃的原因是_______ ,D处合成硫脲的化学方程式为_______ 。
(4)将装置D中液体过滤后,结晶得到粗产品。测定粗产品中硫脲纯度:称取mg产品,加水溶解配成500mL溶液,量取25mL于锥形瓶中,滴加一定量的稀硫酸使溶液显酸性,用cmol⋅L-1KMnO4标准溶液滴定,滴定至终点时消耗KMnO4标准溶液VmL。
①硫脲 中硫元素的化合价为
中硫元素的化合价为_______ 价。
②滴定时,硫脲转化为CO2、N2、 的离子方程式为
的离子方程式为_______ 。
③样品中硫脲的质量分数为_______ (用含“m,c、V”的式子表示)。
 在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备
在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备 ,然后
,然后 再与CaCN2合成
再与CaCN2合成 ,实验装置(夹持及加热装置略)如图所示。
,实验装置(夹持及加热装置略)如图所示。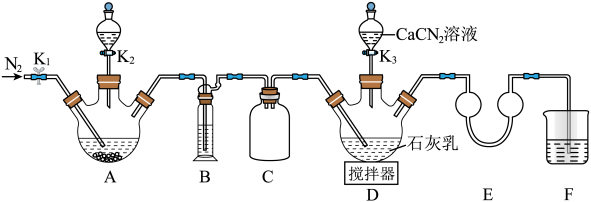
 易溶于水,易被氧化,受热时部分发生异构化生成NH4SCN。
易溶于水,易被氧化,受热时部分发生异构化生成NH4SCN。回答下列问题:
(1)实验前先检查装置气密性,操作为:①在E中加水至浸没导管末端,……;②微热A处三颈烧瓶,观察到E处导管末端有气泡冒出,移走酒精灯;③一段时间后,E处导管末端形成一段水柱,且高度不变。将操作①补充完整
(2)检查气密性后加入药品,装置A中的试剂最佳组合是
A.FeS固体+浓硫酸 B.FeS固体+稀硝酸 C.FeS固体+稀盐酸
装置B中盛装的试剂为
(3)撤走搅拌器,打开K3,水浴加热D处三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温度在80℃的原因是
(4)将装置D中液体过滤后,结晶得到粗产品。测定粗产品中硫脲纯度:称取mg产品,加水溶解配成500mL溶液,量取25mL于锥形瓶中,滴加一定量的稀硫酸使溶液显酸性,用cmol⋅L-1KMnO4标准溶液滴定,滴定至终点时消耗KMnO4标准溶液VmL。
①硫脲
 中硫元素的化合价为
中硫元素的化合价为②滴定时,硫脲转化为CO2、N2、
 的离子方程式为
的离子方程式为③样品中硫脲的质量分数为
您最近一年使用:0次
名校
解题方法
3 . 请回答以下问题:
(1)基态碳原子的价电子排布不能表示为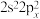 ,原因是违背
,原因是违背_______ 。
(2)下列有关乙烷(C2H6)和乙烯(C2H4)的描述正确的是_______(填字母)。
(3) 分子中Cl-C-Cl的键角
分子中Cl-C-Cl的键角_______ (填“>”、“<”或“=”)甲醛分子中H-C-H的键角。
(4)通常情况下,和乙烯的沸点(-103.7℃)比,氯乙烯(CH2=CHCl)的沸点更高(-13.9℃),其原因是_______ 。
(5)CO2在高温高压下所形成的晶体其晶胞如图所示。则该晶体的类型属于_______ 晶体;该晶体的熔点比SiO2晶体_______ (填“高”或“低”)_______ g/cm3(列出计算式即可)。
(1)基态碳原子的价电子排布不能表示为
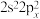 ,原因是违背
,原因是违背(2)下列有关乙烷(C2H6)和乙烯(C2H4)的描述正确的是_______(填字母)。
A.分子中均含有 键和 键和 键 键 | B.分子中的所有原子均处于同一平面上 |
| C.分子中的碳碳键键长:乙烯>乙烷 | D.乙烯中碳原子的杂化轨道类型为sp2 |
(3)
 分子中Cl-C-Cl的键角
分子中Cl-C-Cl的键角(4)通常情况下,和乙烯的沸点(-103.7℃)比,氯乙烯(CH2=CHCl)的沸点更高(-13.9℃),其原因是
(5)CO2在高温高压下所形成的晶体其晶胞如图所示。则该晶体的类型属于


您最近一年使用:0次
名校
解题方法
4 . 实验室由安息香(M=212g/mol)制备二苯乙二酮(M=210g/mol)的反应式如下:
装置示意图如下图所示,实验步骤为:
②停止加热,待沸腾平息后加入2.0g安息香,加热回流45~60min
③加入50mL水,煮沸后冷却,有黄色固体析出
④过滤,并用冷水洗涤固体3次,得到粗品
⑤粗品用75%的乙醇重结晶,干燥后得淡黄色结晶1.6g
回答下列问题:
(1)仪器B的作用是_______ ;冷却水应_______ (填“a”或“b”)口流出。
(2)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是_______ 。
(3)在本实验中,FeCl3为氧化剂且过量,其还原产物为_______ ;某同学尝试改进本实验:
采用催化量的FeCl3并通入空气制备二苯乙二酮,该方法的优点是_______ 。
(4)本实验步骤①~③在乙酸体系中进行,乙酸除作溶剂外,另一主要作用是_______ 。
(5)若粗品中混有少量未氧化的安息香,可用少量_______ 洗涤的方法除去(填标号)。
a.冷水 b.热水 c.乙酸 d.乙醇
若要得到更高纯度的产品,可用_______ 的方法进一步提纯。
(6)本实验的产率最接近于_______ (填标号)。
a.85% b.80% c.75% d.70%

| 物质 | 性状 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 安息香 | 白色固体 | 133 | 344 | 难溶于冷水、溶于热水、乙醇、乙酸 |
二苯乙二酮 | 淡黄色固体 | 95 | 347 | 不溶于水、溶于乙醇、苯、乙酸 |
| 冰乙酸 | 无色液体 | 17 | 118 | 与水、乙醇互溶 |

②停止加热,待沸腾平息后加入2.0g安息香,加热回流45~60min
③加入50mL水,煮沸后冷却,有黄色固体析出
④过滤,并用冷水洗涤固体3次,得到粗品
⑤粗品用75%的乙醇重结晶,干燥后得淡黄色结晶1.6g
回答下列问题:
(1)仪器B的作用是
(2)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是
(3)在本实验中,FeCl3为氧化剂且过量,其还原产物为
采用催化量的FeCl3并通入空气制备二苯乙二酮,该方法的优点是
(4)本实验步骤①~③在乙酸体系中进行,乙酸除作溶剂外,另一主要作用是
(5)若粗品中混有少量未氧化的安息香,可用少量
a.冷水 b.热水 c.乙酸 d.乙醇
若要得到更高纯度的产品,可用
(6)本实验的产率最接近于
a.85% b.80% c.75% d.70%
您最近一年使用:0次
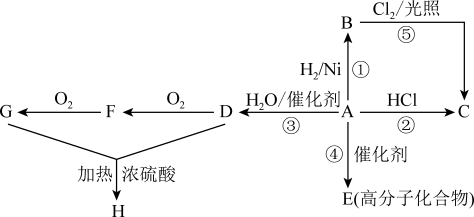
5 . 某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂。
(1)写出A、B、D、E的结构简式:A___________ ,B___________ ,D___________ ,F___________ 。
(2)A能发生聚合反应,其产物为E,E的结构简式为___________ 。
(3)写出②反应的化学反应方程式以及反应类型:②___________ ;反应类型___________ 。
(4)D可以在铜或者银的催化下,逐步氧化,请写出D氧化为F的化学反应方程式以及反应类型:D→F___________ ;反应类型___________ 。
(5)写出D和G生成H的化学反应方程式:D+G→H___________ 。
(6)反应②⑤均可制氯乙烷,反应___________ 最好(填反应序号),原因是___________ 。
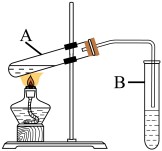
(7)反应D+G→H的实验装置如图所示,试管B中在反应前加入的是___________ 。
(1)写出A、B、D、E的结构简式:A
(2)A能发生聚合反应,其产物为E,E的结构简式为
(3)写出②反应的化学反应方程式以及反应类型:②
(4)D可以在铜或者银的催化下,逐步氧化,请写出D氧化为F的化学反应方程式以及反应类型:D→F
(5)写出D和G生成H的化学反应方程式:D+G→H
(6)反应②⑤均可制氯乙烷,反应
(7)反应D+G→H的实验装置如图所示,试管B中在反应前加入的是
您最近一年使用:0次
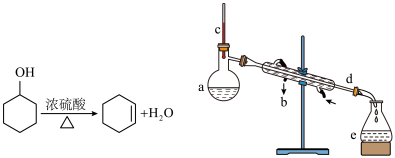
6 . 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置(省略加热和部分夹持装置)如图:
合成反应:在a中加入20g环己醇和少量碎瓷片,在搅动下慢慢加入1mL浓 ;控制馏出物的温度不超过90℃。
;控制馏出物的温度不超过90℃。
分离、提纯:反应得到的粗产物倒入分液漏斗中,分别用少量5%的碳酸钠溶液和蒸馏水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到10g纯净环己烯。
回答下列问题:
(1)装置b的名称是______ 。
(2)加入碎瓷片的作用是______ ,在合成步骤中,应按照______ 的顺序操作(填入序号)
A.先向b中通入冷却水,再开始缓慢加热a B.先开始缓慢加热a,再向b中通入冷却水
(3)分液漏斗在使用前须清洗干净并______ ,在本实验分离过程中,产物应该从分液漏斗的______ (填“上口倒出”或“下口放出”)。
(4)分离、提纯过程中加入无水氯化钙的目的是______ 。
性质物质 | 相对分子质量 | 沸点/℃ | 密度/ | 溶解性 |
环己醇 | 100 | 161 | 0.9618 | 微溶于水 |
环己烯 | 82 | 83 | 0.8102 | 难溶于水 |
 ;控制馏出物的温度不超过90℃。
;控制馏出物的温度不超过90℃。分离、提纯:反应得到的粗产物倒入分液漏斗中,分别用少量5%的碳酸钠溶液和蒸馏水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到10g纯净环己烯。
回答下列问题:
(1)装置b的名称是
(2)加入碎瓷片的作用是
A.先向b中通入冷却水,再开始缓慢加热a B.先开始缓慢加热a,再向b中通入冷却水
(3)分液漏斗在使用前须清洗干净并
(4)分离、提纯过程中加入无水氯化钙的目的是
您最近一年使用:0次
名校
7 . 氮的化合物是重要化工原料,也是空气污染物的重要来源,其转化一直是化学研究的热点。
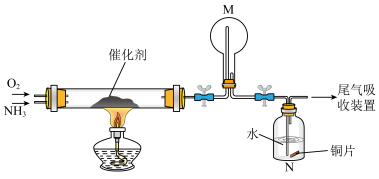
(1)氨催化氧化法是制硝酸的重要步骤,探究氨催化氧化反应的装置如图所示: 。分别生成含等物质的量氮元素的NO和
。分别生成含等物质的量氮元素的NO和 时,各自消耗的
时,各自消耗的 的物质的量之比为
的物质的量之比为______ 。
②一段时间后,观察到装置M中有白烟生成。该白烟成分是______ (写化学式).
(2)可用 将氮氧化物转化成
将氮氧化物转化成 。向1L含200mg
。向1L含200mg 的溶液中加入NaOH溶液调节至碱性,
的溶液中加入NaOH溶液调节至碱性, 转化为去除氮氧化物效果更好的
转化为去除氮氧化物效果更好的 ,再通入NO气体进行反应。碱性条件下
,再通入NO气体进行反应。碱性条件下 去除NO反应的离子方程式为
去除NO反应的离子方程式为______ 。
(3)纳米铁粉可去除水中的 。控制其他条件不变,用纳米铁粉还原水体中的
。控制其他条件不变,用纳米铁粉还原水体中的 ,测得溶液中含氮物质(
,测得溶液中含氮物质( 、
、 、
、 )浓度随时间变化如图所示:
)浓度随时间变化如图所示: 的机理:
的机理: 得到纳米铁粉失去电子转化为
得到纳米铁粉失去电子转化为 ,极少量
,极少量 在纳米铁粉或Cu表面得到电子转化为
在纳米铁粉或Cu表面得到电子转化为 。与不添加少量铜粉相比,添加少量铜粉时去除
。与不添加少量铜粉相比,添加少量铜粉时去除 效率更高,主要原因是
效率更高,主要原因是______ 。
(4)NO也可以利用电化学手段将其转化为 脱除,装置如图所示,电极为多孔惰性材料.则负极的电极反应式是
脱除,装置如图所示,电极为多孔惰性材料.则负极的电极反应式是______ 。______ 。
②b中发生反应的化学方程式为______ 。
③实验中观察到能证明浓硝酸具有强氧化性的现象是______ 。
(1)氨催化氧化法是制硝酸的重要步骤,探究氨催化氧化反应的装置如图所示:
 。分别生成含等物质的量氮元素的NO和
。分别生成含等物质的量氮元素的NO和 时,各自消耗的
时,各自消耗的 的物质的量之比为
的物质的量之比为②一段时间后,观察到装置M中有白烟生成。该白烟成分是
(2)可用
 将氮氧化物转化成
将氮氧化物转化成 。向1L含200mg
。向1L含200mg 的溶液中加入NaOH溶液调节至碱性,
的溶液中加入NaOH溶液调节至碱性, 转化为去除氮氧化物效果更好的
转化为去除氮氧化物效果更好的 ,再通入NO气体进行反应。碱性条件下
,再通入NO气体进行反应。碱性条件下 去除NO反应的离子方程式为
去除NO反应的离子方程式为(3)纳米铁粉可去除水中的
 。控制其他条件不变,用纳米铁粉还原水体中的
。控制其他条件不变,用纳米铁粉还原水体中的 ,测得溶液中含氮物质(
,测得溶液中含氮物质( 、
、 、
、 )浓度随时间变化如图所示:
)浓度随时间变化如图所示: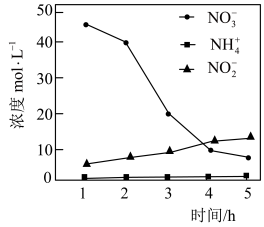
 的机理:
的机理: 得到纳米铁粉失去电子转化为
得到纳米铁粉失去电子转化为 ,极少量
,极少量 在纳米铁粉或Cu表面得到电子转化为
在纳米铁粉或Cu表面得到电子转化为 。与不添加少量铜粉相比,添加少量铜粉时去除
。与不添加少量铜粉相比,添加少量铜粉时去除 效率更高,主要原因是
效率更高,主要原因是(4)NO也可以利用电化学手段将其转化为
 脱除,装置如图所示,电极为多孔惰性材料.则负极的电极反应式是
脱除,装置如图所示,电极为多孔惰性材料.则负极的电极反应式是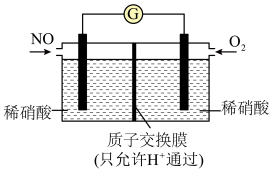
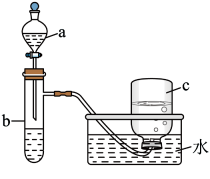
②b中发生反应的化学方程式为
③实验中观察到能证明浓硝酸具有强氧化性的现象是
您最近一年使用:0次
名校
8 . Ⅰ.汽车尾气中含有CO、NO等有害气体,某新型催化剂能促使NO、CO转化为两种无毒气体。一定温度下,在体积为2L的恒容密闭容器中加入等物质的量的NO和CO,测得部分物质的物质的量随时间的变化如图所示。___________ 逆反应速率(填“>”“<”或“=”)。
(2)该反应的化学方程式为___________ 。
(3)从反应开始到达到平衡,
___________  ;该条件下,设起始压强为P,平衡时压强为
;该条件下,设起始压强为P,平衡时压强为 ,则
,则 的值为
的值为___________ 。
(4) 、
、 和熔融
和熔融 可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用,则正极反应式为
可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用,则正极反应式为___________ 。 ,反应过程中的能量变化如图所示。
,反应过程中的能量变化如图所示。___________ (填“放热”或“吸热”)反应,生成1mol  吸收或放出的热量为
吸收或放出的热量为___________ kJ(用a,b表示)。
(6)在恒容条件下进行该反应,下列叙述能说明反应达到平衡状态的是___________ (请用相应字母填空);
a.CO和 的浓度保持不变
的浓度保持不变
b.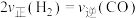
c.每生成1mol 的同时有2mol H-H键形成
的同时有2mol H-H键形成
d.容器内气体密度保持不变
e.容器内质量保持不变

(2)该反应的化学方程式为
(3)从反应开始到达到平衡,

 ;该条件下,设起始压强为P,平衡时压强为
;该条件下,设起始压强为P,平衡时压强为 ,则
,则 的值为
的值为(4)
 、
、 和熔融
和熔融 可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用,则正极反应式为
可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用,则正极反应式为
 ,反应过程中的能量变化如图所示。
,反应过程中的能量变化如图所示。
 吸收或放出的热量为
吸收或放出的热量为(6)在恒容条件下进行该反应,下列叙述能说明反应达到平衡状态的是
a.CO和
 的浓度保持不变
的浓度保持不变b.

c.每生成1mol
 的同时有2mol H-H键形成
的同时有2mol H-H键形成d.容器内气体密度保持不变
e.容器内质量保持不变
您最近一年使用:0次
名校
解题方法
9 . 含硫的物质与人们的生活密切相关。已知硫元素常见的化合价有-2、0、+4、+6四种,其不同价态的物质间可相互转化。完成下列填空:
(1)请写出硫在元素周期表的位置:___________ 。
(2)硫与硅为同一周期元素,通过下列事实能比较两者非金属性强弱的是___________。
(3)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是硫酸。以下是二氧化硫形成酸雨的两种途径: 转化成
转化成 的化学方程式:
的化学方程式:___________ 。
你认为减少酸雨产生的无效措施是___________ (填字母序号)
A.少用煤作燃料 B.把工厂烟囱造高 C.燃料脱硫 D.开发新能源
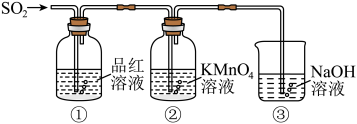
某同学利用如图所示装置探究二氧化硫气体的性质,回答下列问题:___________ 。
(5)当观察到②中溶液颜色变浅时,①中的现象是___________ 。
(6)装置③的作用是___________ 。
(7)②中的现象说明二氧化硫具有的性质是___________ 。
(8)从氧化还原角度制备硫代硫酸钠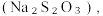 下列方案合理的是(填编号)___________。
下列方案合理的是(填编号)___________。
(9)为进一步减少 的污染并变废为宝,我国正在探索在一定条件下,用CO还原
的污染并变废为宝,我国正在探索在一定条件下,用CO还原 得到单质硫的方法来除去
得到单质硫的方法来除去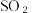 写出该反应的化学方程式:
写出该反应的化学方程式:___________ 。
(1)请写出硫在元素周期表的位置:
(2)硫与硅为同一周期元素,通过下列事实能比较两者非金属性强弱的是___________。
A.热稳定性: | B.溶解度: 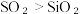 |
C.单质的熔点: | D.酸性:  |
(3)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是硫酸。以下是二氧化硫形成酸雨的两种途径:

 转化成
转化成 的化学方程式:
的化学方程式:你认为减少酸雨产生的无效措施是
A.少用煤作燃料 B.把工厂烟囱造高 C.燃料脱硫 D.开发新能源
某同学利用如图所示装置探究二氧化硫气体的性质,回答下列问题:
(5)当观察到②中溶液颜色变浅时,①中的现象是
(6)装置③的作用是
(7)②中的现象说明二氧化硫具有的性质是
(8)从氧化还原角度制备硫代硫酸钠
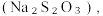 下列方案合理的是(填编号)___________。
下列方案合理的是(填编号)___________。A.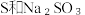 | B. 和浓 和浓 | C.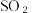 和 和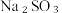 | D.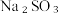 和 和 |
(9)为进一步减少
 的污染并变废为宝,我国正在探索在一定条件下,用CO还原
的污染并变废为宝,我国正在探索在一定条件下,用CO还原 得到单质硫的方法来除去
得到单质硫的方法来除去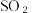 写出该反应的化学方程式:
写出该反应的化学方程式:
您最近一年使用:0次
名校
10 . 硫酸亚铁是重要的化工原料
Ⅰ.
(1)由 溶液制备硫酸亚铁晶体的方法是
溶液制备硫酸亚铁晶体的方法是___________ 。检验晶体中 是否完全变质,将晶体溶于水,加
是否完全变质,将晶体溶于水,加___________ (填试剂)。
(2) 溶液与过量的
溶液与过量的 溶液混合,可以得到含
溶液混合,可以得到含 的浊液,离子方程式是
的浊液,离子方程式是___________ 。
Ⅱ.氧化铁黄(FeOOH)是一种黄色颜料,具有非常好的耐光性和耐碱性,是氧化铁的一水合物。以 为原料制备FeOOH的流程如下:
为原料制备FeOOH的流程如下:
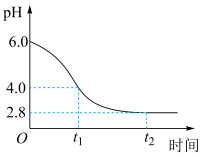
(3)若在实验室完成上述制备,不需要使用的仪器是___________ 。 时段,pH快速下降的原因是反应生成了FeOOH和
时段,pH快速下降的原因是反应生成了FeOOH和 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
② 时段,经历的反应为
时段,经历的反应为 ,该过程pH继续平缓下降的原因可能是
,该过程pH继续平缓下降的原因可能是___________ 。
(5)判断流程中产品洗涤干净的方法是___________ 。
(6)氧化铁黄(FeOOH)纯度可以通过产品的耗酸量确定,如下图所示。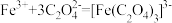 ,
,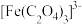 不与稀碱液反应。
不与稀碱液反应。
①在溶液c中滴加NaOH标准溶液,使用的指示剂为___________ 。
②若实验时加入了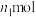 的
的 ,消耗
,消耗 ,设氧化铁黄的摩尔质量为
,设氧化铁黄的摩尔质量为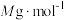 ,则氧化铁黄样品纯度为
,则氧化铁黄样品纯度为___________ (用含w、 、
、 、M的代数式表示)。
、M的代数式表示)。
③测定时,若滴入 不足量,会使实验结果
不足量,会使实验结果___________ (选填“偏大”“偏小”或“无影响”)。
Ⅰ.
(1)由
 溶液制备硫酸亚铁晶体的方法是
溶液制备硫酸亚铁晶体的方法是 是否完全变质,将晶体溶于水,加
是否完全变质,将晶体溶于水,加(2)
 溶液与过量的
溶液与过量的 溶液混合,可以得到含
溶液混合,可以得到含 的浊液,离子方程式是
的浊液,离子方程式是Ⅱ.氧化铁黄(FeOOH)是一种黄色颜料,具有非常好的耐光性和耐碱性,是氧化铁的一水合物。以
 为原料制备FeOOH的流程如下:
为原料制备FeOOH的流程如下: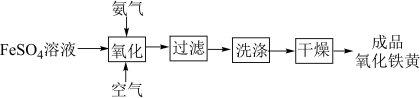
(3)若在实验室完成上述制备,不需要使用的仪器是
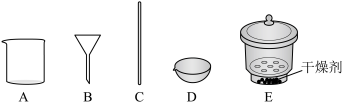
 时段,pH快速下降的原因是反应生成了FeOOH和
时段,pH快速下降的原因是反应生成了FeOOH和 ,该反应的化学方程式为
,该反应的化学方程式为②
 时段,经历的反应为
时段,经历的反应为 ,该过程pH继续平缓下降的原因可能是
,该过程pH继续平缓下降的原因可能是(5)判断流程中产品洗涤干净的方法是
(6)氧化铁黄(FeOOH)纯度可以通过产品的耗酸量确定,如下图所示。
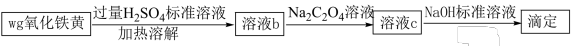
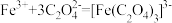 ,
,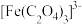 不与稀碱液反应。
不与稀碱液反应。①在溶液c中滴加NaOH标准溶液,使用的指示剂为
②若实验时加入了
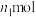 的
的 ,消耗
,消耗 ,设氧化铁黄的摩尔质量为
,设氧化铁黄的摩尔质量为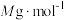 ,则氧化铁黄样品纯度为
,则氧化铁黄样品纯度为 、
、 、M的代数式表示)。
、M的代数式表示)。③测定时,若滴入
 不足量,会使实验结果
不足量,会使实验结果
您最近一年使用:0次




