解题方法
1 . 为了实现“碳达峰”和“碳中和”的目标,将CO2转化成可利用的化学能源的“负碳”技术是世界各国关注的焦点。
方法Ⅰ:CO2催化加氢制甲醇。
以CO2、H2为原料合成CH3OH涉及的反应如下:
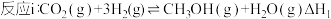
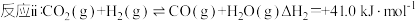

(1)计算反应i的ΔH1=___________ 。
(2)一定温度和催化剂条件下,0.73molH2、0.24molCO2和0.03molN2(已知N2不参与反应)在总压强为3.0MPa的密闭容器中进行上述反应,平衡时CO2的转化率、CH3OH和CO的选择性随温度的变化曲线如图所示。___________ 的变化(填“CO2”、“CH3OH”或“CO”)。
②上述反应体系在一定条件下建立平衡后,下列说法不正确的有___________ (填字母)。
A.降低温度,反应i~iii的正、逆反应速率都减小
B.向容器中再通入少量N2,CO2的平衡转化率下降
C.移去部分H2O(g),反应iii平衡不移动
D.选择合适的催化剂能提高CO2的平衡转化率
E.平衡时CH3OH的体积分数一定小于50%
③某温度下,t1min反应到达平衡,测得容器中CH3OH的体积分数为12.5%。此时用CH3OH的分压表示0~t1时间内的反应速率v(CH3OH)=___________ MPa·min-1。设此时n(CO)=amol,计算该温度下反应ii的平衡常数Kx=___________ (用含有a的代数式表示)。[分压=总压×该组分物质的量分数;对于反应 ,
, 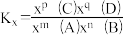 ,x为物质的量分数。]
,x为物质的量分数。]
方法Ⅱ:CO2电解法制聚乙烯
(3)常温常压下,以纳米二氧化钛(TiO2)膜为工作电极,酸性条件下电解CO2可以得到聚乙烯,该电极反应方程式为___________ 。
方法Ⅲ:CO2催化加氢制低碳烯烃(2~4个C的烯烃)
某研究小组使用Zn-Ga-O/SAPO-34双功能催化剂实现了CO2直接合成低碳烯烃,并给出了其可能的反应历程(如图所示)。H2首先在Zn-Ga-O表面解离成2个H*,随后参与到CO2的还原过程;SAPO-34则催化生成的甲醇转化为低碳烯烃。
(4)理论上,反应历程中生成的甲醇与消耗的H*的物质的量之比为___________ 。
方法Ⅰ:CO2催化加氢制甲醇。
以CO2、H2为原料合成CH3OH涉及的反应如下:
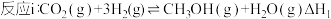
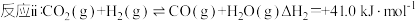

(1)计算反应i的ΔH1=
(2)一定温度和催化剂条件下,0.73molH2、0.24molCO2和0.03molN2(已知N2不参与反应)在总压强为3.0MPa的密闭容器中进行上述反应,平衡时CO2的转化率、CH3OH和CO的选择性随温度的变化曲线如图所示。

②上述反应体系在一定条件下建立平衡后,下列说法不正确的有
A.降低温度,反应i~iii的正、逆反应速率都减小
B.向容器中再通入少量N2,CO2的平衡转化率下降
C.移去部分H2O(g),反应iii平衡不移动
D.选择合适的催化剂能提高CO2的平衡转化率
E.平衡时CH3OH的体积分数一定小于50%
③某温度下,t1min反应到达平衡,测得容器中CH3OH的体积分数为12.5%。此时用CH3OH的分压表示0~t1时间内的反应速率v(CH3OH)=
 ,
, 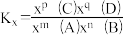 ,x为物质的量分数。]
,x为物质的量分数。]方法Ⅱ:CO2电解法制聚乙烯
(3)常温常压下,以纳米二氧化钛(TiO2)膜为工作电极,酸性条件下电解CO2可以得到聚乙烯,该电极反应方程式为
方法Ⅲ:CO2催化加氢制低碳烯烃(2~4个C的烯烃)
某研究小组使用Zn-Ga-O/SAPO-34双功能催化剂实现了CO2直接合成低碳烯烃,并给出了其可能的反应历程(如图所示)。H2首先在Zn-Ga-O表面解离成2个H*,随后参与到CO2的还原过程;SAPO-34则催化生成的甲醇转化为低碳烯烃。

(4)理论上,反应历程中生成的甲醇与消耗的H*的物质的量之比为
您最近一年使用:0次
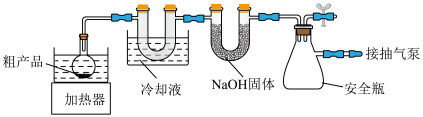
2 . 无水四氯化锡(SnCl4)常用作有机合成的氯化催化剂。实验室可用熔融的锡与氯气反应(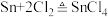 )制备SnCl4,装置如下图所示:
)制备SnCl4,装置如下图所示:
请回答:
(1)仪器①中导管的作用是___________ ;装置A中烧瓶内反应的离子方程式为___________ 。
(2)B、C、F、G盛装的试剂应依次选用下列中的___________ (填标号)。
a.浓H2SO4 b.饱和NaHCO3溶液 c.饱和NaCl溶液 d.NaOH浓溶液
(3)冷阱③和小烧杯⑤内都装入冷水,生成的SnCl4经冷凝后,收集于E装置的试管④中,该液体常常呈黄绿色,原因是___________ 。
(4)用玻璃棒蘸取少量产物SnCl4,放置在空气中,片刻即产生白色烟雾,产物为SnO2•xH2O和___________ (填化学式)。
(5)提纯:将SnCl4粗产品用如图所示的装置进行提纯。请给出操作顺序:将粗产品加入圆底烧瓶,连接好装置,关闭安全瓶上旋塞,打开抽气泵、加热器→( ) →将产品转至干燥器中保存。
c.控温到114℃ d.控温到30℃
(6)利用沉淀滴定法测定产品中Sn2+的含量,甲同学方案如下:准确称取mg产品于锥形瓶中,用蒸馏水溶解,X溶液作指示剂,用bmol/L的硝酸银标准溶液滴定,滴定终点时消耗硝酸银溶液VmL,由此可计算产品中Sn2+的质量分数。
①参考表中的数据,X溶液最好选用的是___________ (填序号)。
A.NaCl溶液 B.NaBr溶液 C.NaCN溶液 D.Na2CrO4溶液
②乙同学认为甲同学测得的Sn2+含量可能会偏高,理由___________ 。
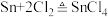 )制备SnCl4,装置如下图所示:
)制备SnCl4,装置如下图所示: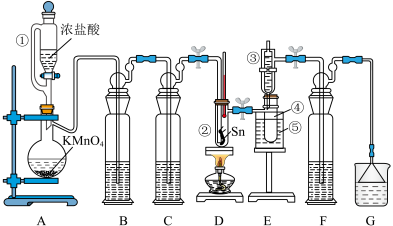
| 化学式 | Sn | SnCl2 | SnCl4 |
| 熔点/℃ | 232 | 246 | -33 |
| 沸点/℃ | 2260 | 652 | 114 |
| 其他性质 | 银白色固体金属,化学性质与Fe相似 | 无色晶体,Sn2+易被Fe3+、I2等氧化为Sn4+ | 无色液体,易水解生成SnO2·xH2O |
(1)仪器①中导管的作用是
(2)B、C、F、G盛装的试剂应依次选用下列中的
a.浓H2SO4 b.饱和NaHCO3溶液 c.饱和NaCl溶液 d.NaOH浓溶液
(3)冷阱③和小烧杯⑤内都装入冷水,生成的SnCl4经冷凝后,收集于E装置的试管④中,该液体常常呈黄绿色,原因是
(4)用玻璃棒蘸取少量产物SnCl4,放置在空气中,片刻即产生白色烟雾,产物为SnO2•xH2O和
(5)提纯:将SnCl4粗产品用如图所示的装置进行提纯。请给出操作顺序:将粗产品加入圆底烧瓶,连接好装置,关闭安全瓶上旋塞,打开抽气泵、加热器→
c.控温到114℃ d.控温到30℃
(6)利用沉淀滴定法测定产品中Sn2+的含量,甲同学方案如下:准确称取mg产品于锥形瓶中,用蒸馏水溶解,X溶液作指示剂,用bmol/L的硝酸银标准溶液滴定,滴定终点时消耗硝酸银溶液VmL,由此可计算产品中Sn2+的质量分数。
①参考表中的数据,X溶液最好选用的是
A.NaCl溶液 B.NaBr溶液 C.NaCN溶液 D.Na2CrO4溶液
| 难溶物 | AgCl | AgBr | AgCN | Ag2CrO4 |
| 颜色 | 白 | 浅黄 | 白 | 砖红 |
| Ksp | 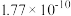 | 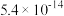 | 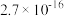 | 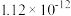 |
您最近一年使用:0次
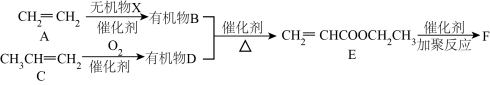
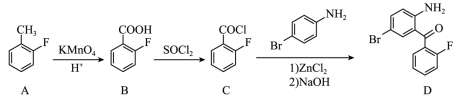
3 . F是一种皮革处理剂,一种合成F的流程如下图:
(1)E所含官能团名称是___________ 。
(2)下列化学键在有机物B中存在,且极性最强的是___________(填序号)。
(3)有机物F的结构简式为___________ 。
(4)写出C→D的化学方程式___________ 。
(1)E所含官能团名称是
(2)下列化学键在有机物B中存在,且极性最强的是___________(填序号)。
| A.C−C | B.C−H | C.C−O | D.O−H |
(3)有机物F的结构简式为
(4)写出C→D的化学方程式
您最近一年使用:0次
4 . 战略储备金属钽( )的获取可先通过溶剂萃取法对合金废料(主要成分为
)的获取可先通过溶剂萃取法对合金废料(主要成分为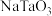 、
、 及
及 、
、 、W等氧化物)进行提纯制备
、W等氧化物)进行提纯制备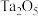 ,其工艺流程见图:
,其工艺流程见图: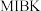 为甲基异丁基甲酮,对
为甲基异丁基甲酮,对 、
、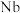 的氟络离子具有较高萃取度
的氟络离子具有较高萃取度
② 在低酸度溶液中极易被洗脱
在低酸度溶液中极易被洗脱
③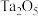 的水化物性质与
的水化物性质与 族元素相似
族元素相似
④ 的
的
回答下列问题:
(1)“酸溶”步骤中当氢氟酸过量时,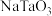 主要以
主要以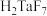 存在,写出该过程的离子方程式:
存在,写出该过程的离子方程式:_______
(2)“废液”中钛、镍、钨等杂质元素以氟络离子形态存在,其中 位于由若干个
位于由若干个 构成的正八面体空隙内,则
构成的正八面体空隙内,则 的存在形式为
的存在形式为_______
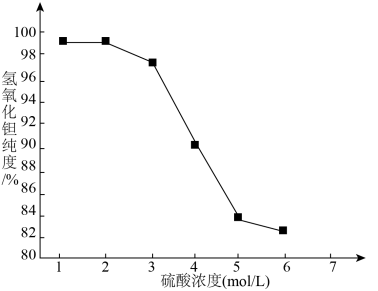
(3)“酸洗”的目的是_______ ,硫酸浓度与产物纯度的关系如图所示,则硫酸的最佳浓度为_______
(5)_______ (选填“能”或不能)用 代替
代替 进行“沉钽”,原因是
进行“沉钽”,原因是_______ 。
(6)室温下,向 反萃液中通入
反萃液中通入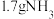 至
至 时沉淀完全,则此时
时沉淀完全,则此时
_______ 。
 )的获取可先通过溶剂萃取法对合金废料(主要成分为
)的获取可先通过溶剂萃取法对合金废料(主要成分为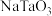 、
、 及
及 、
、 、W等氧化物)进行提纯制备
、W等氧化物)进行提纯制备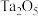 ,其工艺流程见图:
,其工艺流程见图: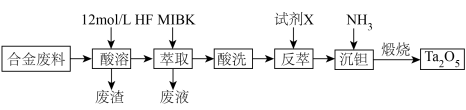
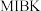 为甲基异丁基甲酮,对
为甲基异丁基甲酮,对 、
、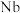 的氟络离子具有较高萃取度
的氟络离子具有较高萃取度②
 在低酸度溶液中极易被洗脱
在低酸度溶液中极易被洗脱③
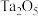 的水化物性质与
的水化物性质与 族元素相似
族元素相似④
 的
的
回答下列问题:
(1)“酸溶”步骤中当氢氟酸过量时,
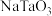 主要以
主要以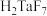 存在,写出该过程的离子方程式:
存在,写出该过程的离子方程式:(2)“废液”中钛、镍、钨等杂质元素以氟络离子形态存在,其中
 位于由若干个
位于由若干个 构成的正八面体空隙内,则
构成的正八面体空隙内,则 的存在形式为
的存在形式为(3)“酸洗”的目的是
| A.稀盐酸 | B.纯水 | C.氨水 | D. 溶液 溶液 |
(5)
 代替
代替 进行“沉钽”,原因是
进行“沉钽”,原因是(6)室温下,向
 反萃液中通入
反萃液中通入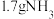 至
至 时沉淀完全,则此时
时沉淀完全,则此时
您最近一年使用:0次
5 . 化合物G可用于治疗失眠,其合成路线如图: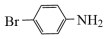 的名称为
的名称为_______ 。
(2)在水中的溶解度比较:化合物A_______ 化合物B(填“>”或“<”或“=”)。
(3)根据化合物E的结构特征,分析预测其可能的化学性质,完成表格。
(4)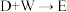 的过程中还要脱去一个
的过程中还要脱去一个 ,则试剂W的结构简式为
,则试剂W的结构简式为_______ 。
(5)下列说法不正确的是_______ 。
A.化合物A和B可通过红外光谱进行鉴别
B.B→C的反应产物除化合物C外,还有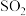 、
、
C.化合物E中含氧官能团名称为酮羰基
D.化合物F中氧原子的杂化轨道类型与氮原子的相同
E.化合物G中填充在四面体空隙中的碳原子有4个
(6)对化合物C再进行一氟取代,其产物的同分异构体中,同时满足下列条件的结构为_______ 。
①属于芳香族化合物 ②能发生银镜反应 ③分子中不同化学环境的氢原子数目比为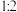
(7)以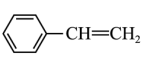 和H2NCH2CH2OH为原料合成
和H2NCH2CH2OH为原料合成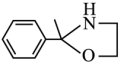 的流程图如图:
的流程图如图:
①条件A为_______ ;


 的名称为
的名称为(2)在水中的溶解度比较:化合物A
(3)根据化合物E的结构特征,分析预测其可能的化学性质,完成表格。
| 序号 | 反应试剂、条件 | 反应后新物质 | 反应类型 |
| ① |  水溶液,加热 水溶液,加热 | 水解反应 | |
| ② |  、催化剂,加热 、催化剂,加热 |
|
(4)
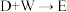 的过程中还要脱去一个
的过程中还要脱去一个 ,则试剂W的结构简式为
,则试剂W的结构简式为(5)下列说法不正确的是
A.化合物A和B可通过红外光谱进行鉴别
B.B→C的反应产物除化合物C外,还有
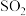 、
、
C.化合物E中含氧官能团名称为酮羰基
D.化合物F中氧原子的杂化轨道类型与氮原子的相同
E.化合物G中填充在四面体空隙中的碳原子有4个
(6)对化合物C再进行一氟取代,其产物的同分异构体中,同时满足下列条件的结构为
①属于芳香族化合物 ②能发生银镜反应 ③分子中不同化学环境的氢原子数目比为
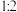
(7)以
 和H2NCH2CH2OH为原料合成
和H2NCH2CH2OH为原料合成 的流程图如图:
的流程图如图: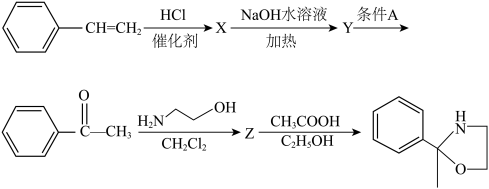
①条件A为
②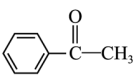
 Z的化学方程式为
Z的化学方程式为
您最近一年使用:0次
6 . 氢能是理想的可持续能源,利用甲酸( )分解可制得
)分解可制得 :
: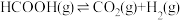 ,科学家正致力于研究该反应的高效催化剂。
,科学家正致力于研究该反应的高效催化剂。
(1)甲酸中C原子的 模型为
模型为_______ 。
(2)运用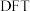 理论计算甲酸发生分解反应的路径如图(*表示催化剂表面吸附位),分解过程中的决速步骤的化学方程式为
理论计算甲酸发生分解反应的路径如图(*表示催化剂表面吸附位),分解过程中的决速步骤的化学方程式为_______ 。 合金对
合金对 脱氢的催化效果(以
脱氢的催化效果(以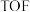 表示),图2为
表示),图2为 分别在
分别在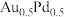 与
与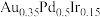 上第一步脱氢的微观示意图及部分键长数据。
上第一步脱氢的微观示意图及部分键长数据。 为46号元素,在元素周期表的位置为
为46号元素,在元素周期表的位置为_______ 。
②从微观视角解释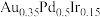 的催化效果优于
的催化效果优于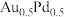 的原因是
的原因是_______ 。
(4)催化分解甲酸的过程中,存在副反应: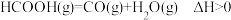 。一定温度下,向
。一定温度下,向 恒容密闭容器中充入
恒容密闭容器中充入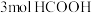 ,此时压强为
,此时压强为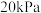 。
。 时测得容器内
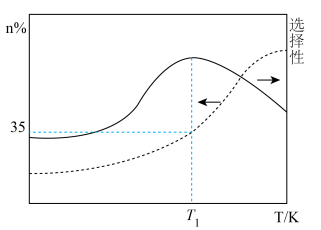
时测得容器内 的选择性、含碳物质的物质的量分数与温度的关系如图所示,
的选择性、含碳物质的物质的量分数与温度的关系如图所示, 时
时 的平衡转化率达到
的平衡转化率达到 。[已知:
。[已知: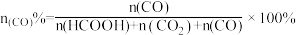 ]
] 选择性曲线变化原因
选择性曲线变化原因_______ 。
② 时,下列叙述能说明容器内反应达到平衡状态的是
时,下列叙述能说明容器内反应达到平衡状态的是_______ (填标号)
A. 和
和 的物质的量之比不再发生变化 B.混合气体的平均摩尔质量不再发生变化
的物质的量之比不再发生变化 B.混合气体的平均摩尔质量不再发生变化
C.生成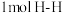 的同时,有
的同时,有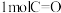 断裂生成
断裂生成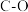 D.主反应的平衡常数不再变化
D.主反应的平衡常数不再变化
③ 时,
时,
_______ 
④请列出过程计算 时主反应的的平衡常数
时主反应的的平衡常数
_______ (以分压表示,分压=总压×物质的量分数)。
(5)利用人工光合作用可将 转化为甲酸,装置如图所示,电极2的反应式为
转化为甲酸,装置如图所示,电极2的反应式为_______ 。
 )分解可制得
)分解可制得 :
: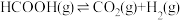 ,科学家正致力于研究该反应的高效催化剂。
,科学家正致力于研究该反应的高效催化剂。(1)甲酸中C原子的
 模型为
模型为(2)运用
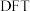 理论计算甲酸发生分解反应的路径如图(*表示催化剂表面吸附位),分解过程中的决速步骤的化学方程式为
理论计算甲酸发生分解反应的路径如图(*表示催化剂表面吸附位),分解过程中的决速步骤的化学方程式为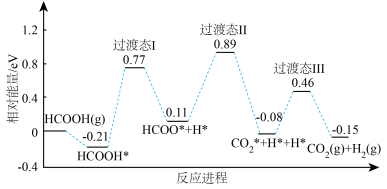
 合金对
合金对 脱氢的催化效果(以
脱氢的催化效果(以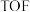 表示),图2为
表示),图2为 分别在
分别在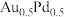 与
与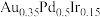 上第一步脱氢的微观示意图及部分键长数据。
上第一步脱氢的微观示意图及部分键长数据。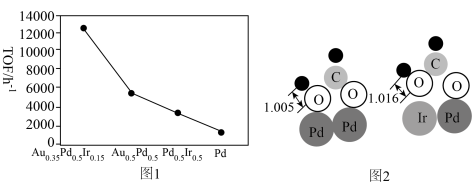
 为46号元素,在元素周期表的位置为
为46号元素,在元素周期表的位置为②从微观视角解释
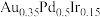 的催化效果优于
的催化效果优于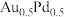 的原因是
的原因是(4)催化分解甲酸的过程中,存在副反应:
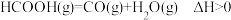 。一定温度下,向
。一定温度下,向 恒容密闭容器中充入
恒容密闭容器中充入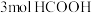 ,此时压强为
,此时压强为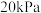 。
。 时测得容器内
时测得容器内 的选择性、含碳物质的物质的量分数与温度的关系如图所示,
的选择性、含碳物质的物质的量分数与温度的关系如图所示, 时
时 的平衡转化率达到
的平衡转化率达到 。[已知:
。[已知: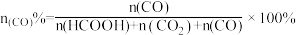 ]
]
 选择性曲线变化原因
选择性曲线变化原因②
 时,下列叙述能说明容器内反应达到平衡状态的是
时,下列叙述能说明容器内反应达到平衡状态的是A.
 和
和 的物质的量之比不再发生变化 B.混合气体的平均摩尔质量不再发生变化
的物质的量之比不再发生变化 B.混合气体的平均摩尔质量不再发生变化C.生成
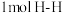 的同时,有
的同时,有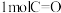 断裂生成
断裂生成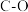 D.主反应的平衡常数不再变化
D.主反应的平衡常数不再变化③
 时,
时,

④请列出过程计算
 时主反应的的平衡常数
时主反应的的平衡常数
(5)利用人工光合作用可将
 转化为甲酸,装置如图所示,电极2的反应式为
转化为甲酸,装置如图所示,电极2的反应式为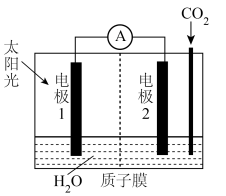
您最近一年使用:0次
7 . 醛类的银镜反应于日常生活中有重要应用。
(1)在配合物Ag(NH3)2OH中,提供空轨道用以形成配位键的微粒是_______ ,1mol该配合物中含有的共价键数目为_______ 。
(2)写出乙醛与银氨溶液反应的化学方程式_______ 。
I.某兴趣小组在进行银镜反应时发现试管内有黑色物质产生,并对其成分展开探究。
查阅资料:i.Ag2O易溶于氨水,一般生成银氨溶液。
ii.
【提出猜想】猜想a:黑色物质可能含有Ag2O;
猜想b:黑色物质可能含有碳;
猜想c:黑色物质可能含有银;
【验证猜想】设计如下实验:
(3)补充表格:试剂A为_______ ,现象为_______ 。
【提出疑问】块状Ag为银白色固体。
【补充实验】_______ (填操作和现象),推测Ag单质微粒直径介乎1~100nm之间。
【实验结论】银镜反应中伴随产生的黑色物质为_______ 。
(4)请使用绿色环保方法清洁银镜实验后的试管:_______ (用离子方程式表示)。
(5)部分小组同学未观察到银镜出现,推测乙醛可能变质。
查阅资料:乙醛在常温下会聚合生成三聚乙醛。_______ 。
(6)请写出醛类的一种生活实际应用_______ 。
(1)在配合物Ag(NH3)2OH中,提供空轨道用以形成配位键的微粒是
(2)写出乙醛与银氨溶液反应的化学方程式
I.某兴趣小组在进行银镜反应时发现试管内有黑色物质产生,并对其成分展开探究。
查阅资料:i.Ag2O易溶于氨水,一般生成银氨溶液。
ii.

【提出猜想】猜想a:黑色物质可能含有Ag2O;
猜想b:黑色物质可能含有碳;
猜想c:黑色物质可能含有银;
【验证猜想】设计如下实验:
| 序号 | 实验方案 | 实验现象 | 实验结论 |
| 1 | 取洗涤后的黑色物质于洁净试管中,加入试剂A,振荡静置,取上层清液与盐酸反应,观察现象。 | 振荡静置后发现固体明显减少。 上层清液出现沉淀。 | 猜想a成立 |
| 2 | 将上述反应未溶解的固体溶于稀硝酸,一段时间后,观察现象。 | 固体完全溶解 | 猜想b不成立 |
| 3 | 取固体溶解后所得溶液先滴加稀盐酸,再滴加氨水,观察现象。 | _______ | 猜想c成立 |
【提出疑问】块状Ag为银白色固体。
【补充实验】
【实验结论】银镜反应中伴随产生的黑色物质为
(4)请使用绿色环保方法清洁银镜实验后的试管:
(5)部分小组同学未观察到银镜出现,推测乙醛可能变质。
查阅资料:乙醛在常温下会聚合生成三聚乙醛。
3CH3CHO
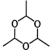
(6)请写出醛类的一种生活实际应用
您最近一年使用:0次
解题方法
8 . 某研究小组用工业钛白副产品为原料制备纳米级电池材料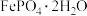 ,按如下流程开展实验。
,按如下流程开展实验。 ,含少量的
,含少量的 、
、 、
、 等杂质。
等杂质。
②已知 和
和 的氧化性随酸性的增强而增强。
的氧化性随酸性的增强而增强。
请回答:
(1)常温下步骤Ⅰ所得料液其pH___________ 7(填“>”、“<”)。
(2)下列说法不正确 的是___________。
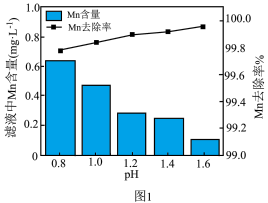
(3)步骤Ⅴ中Mn元素的去除率及滤液中Mn元素含量随着溶液pH值的关系如图1所示,___________ 。
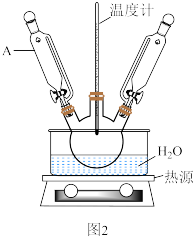
(4)步骤Ⅵ操作之一采用如图2所示装置进行(忽略夹持装置),仪器A的名称是___________ ;该操作不宜用酒精灯直接加热的原因是___________ 。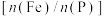 是衡量磷酸铁品质最关键的指标。
是衡量磷酸铁品质最关键的指标。
Fe元素的定量测定:①配制一系列pH=3~5, 浓度由低到高的与邻菲罗啉的橙红色络合物的标准液。②称取一定量产品,用适量盐酸溶解,再加入足量的盐酸羟胺(
浓度由低到高的与邻菲罗啉的橙红色络合物的标准液。②称取一定量产品,用适量盐酸溶解,再加入足量的盐酸羟胺( )溶液,调pH=3~5,加入邻菲罗啉。③进行比色
)溶液,调pH=3~5,加入邻菲罗啉。③进行比色
①通过比色能获得Fe元素浓度的原理是___________ 。
②测得产品中铁磷比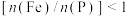 ,可能原因是
,可能原因是___________ 。
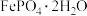 ,按如下流程开展实验。
,按如下流程开展实验。
 ,含少量的
,含少量的 、
、 、
、 等杂质。
等杂质。②已知
 和
和 的氧化性随酸性的增强而增强。
的氧化性随酸性的增强而增强。请回答:
(1)常温下步骤Ⅰ所得料液其pH
(2)下列说法
| A.步骤Ⅱ,加入Fe粉的目的是调节溶液pH值,以便Ti元素水解沉淀 |
B.步骤Ⅲ,加入 的目的是除去Mg元素 的目的是除去Mg元素 |
| C.为了提高实验效率,可以将Ⅱ、Ⅲ、Ⅴ的过滤操作合并 |
D.步骤Ⅳ中过量的 可在步骤Ⅴ中被氧化去除 可在步骤Ⅴ中被氧化去除 |
(3)步骤Ⅴ中Mn元素的去除率及滤液中Mn元素含量随着溶液pH值的关系如图1所示,
(4)步骤Ⅵ操作之一采用如图2所示装置进行(忽略夹持装置),仪器A的名称是
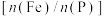 是衡量磷酸铁品质最关键的指标。
是衡量磷酸铁品质最关键的指标。Fe元素的定量测定:①配制一系列pH=3~5,
 浓度由低到高的与邻菲罗啉的橙红色络合物的标准液。②称取一定量产品,用适量盐酸溶解,再加入足量的盐酸羟胺(
浓度由低到高的与邻菲罗啉的橙红色络合物的标准液。②称取一定量产品,用适量盐酸溶解,再加入足量的盐酸羟胺( )溶液,调pH=3~5,加入邻菲罗啉。③进行比色
)溶液,调pH=3~5,加入邻菲罗啉。③进行比色①通过比色能获得Fe元素浓度的原理是
②测得产品中铁磷比
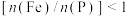 ,可能原因是
,可能原因是
您最近一年使用:0次
解题方法
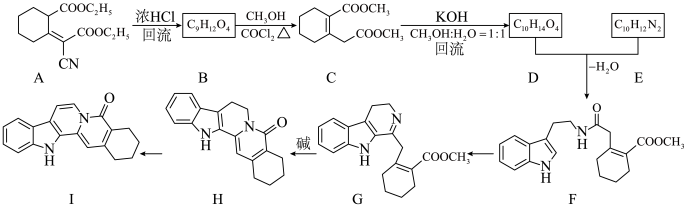
9 . 化合物Ⅰ具有良好的降血压、减肥以及治疗心脏疾病等功效,其合成路线如下(部分反应条件省略)
(1)化合物A的非全碳 官能团名称是___________ 。
(2)下列说法不正确 的是___________。
(3)化合物E的结构简式是___________ 。
(4)写出G→H的化学方程式___________ 。
(5)写出同时符合下列条件的化合物C的一种同分异构体的结构简式___________ 。
①分子中含有苯环且与 溶液发生显色反应
溶液发生显色反应
②核磁共振氢谱和红外光谱检测表明:分子中共有4种不同化学环境的氢原子,不含 键
键
(6)写出以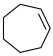 、
、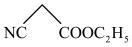 以及乙醇为原料制备化合物A的合成路线图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
以及乙醇为原料制备化合物A的合成路线图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。___________
已知:①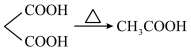
②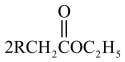
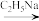
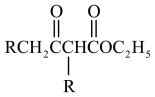
③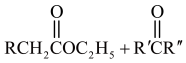

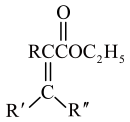
(1)化合物A的
(2)下列说法
| A.A→B的转变只是官能团种类和数量的变化 |
B.在B→C的反应中, 作催化剂 作催化剂 |
C.化合物G的分子式为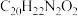 |
| D.化合物I可在酸性或碱性条件下发生水解反应 |
(3)化合物E的结构简式是
(4)写出G→H的化学方程式
(5)写出同时符合下列条件的化合物C的一种同分异构体的结构简式
①分子中含有苯环且与
 溶液发生显色反应
溶液发生显色反应②核磁共振氢谱和红外光谱检测表明:分子中共有4种不同化学环境的氢原子,不含
 键
键(6)写出以
 、
、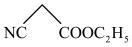 以及乙醇为原料制备化合物A的合成路线图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
以及乙醇为原料制备化合物A的合成路线图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
您最近一年使用:0次
解题方法
10 . 佐米曲坦(化合物 )是治疗偏头疼的药物,其合成路线之一如下(部分反应条件省略):
)是治疗偏头疼的药物,其合成路线之一如下(部分反应条件省略): 的化学名称
的化学名称___________ ;写出 中含氧官能团的名称
中含氧官能团的名称___________ 。
(2)写出 的反应类型
的反应类型___________ 。
(3)写出 反应的化学方程式
反应的化学方程式___________ 。
(4)在一定条件下, 发生加聚反应可制得导电聚合物,写出其反应的化学方程式
发生加聚反应可制得导电聚合物,写出其反应的化学方程式___________ 。
(5)同时满足下列条件的 的同分异构体有
的同分异构体有___________ 种(不考虑立体异构)。
③既能发生水解反应也能发生银镜反应。
写出核磁共振氢谱有6组峰,且峰面积之比为3:2:2:2:1:1的结构简式___________ (任写一种)。
 )是治疗偏头疼的药物,其合成路线之一如下(部分反应条件省略):
)是治疗偏头疼的药物,其合成路线之一如下(部分反应条件省略):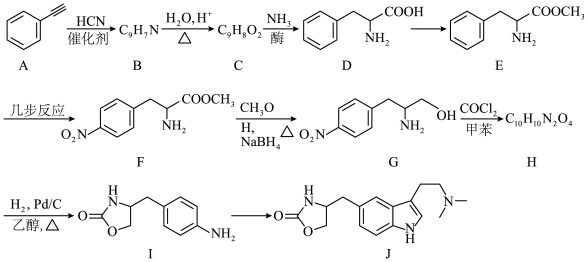
 的化学名称
的化学名称 中含氧官能团的名称
中含氧官能团的名称(2)写出
 的反应类型
的反应类型(3)写出
 反应的化学方程式
反应的化学方程式(4)在一定条件下,
 发生加聚反应可制得导电聚合物,写出其反应的化学方程式
发生加聚反应可制得导电聚合物,写出其反应的化学方程式(5)同时满足下列条件的
 的同分异构体有
的同分异构体有①含有
③既能发生水解反应也能发生银镜反应。
写出核磁共振氢谱有6组峰,且峰面积之比为3:2:2:2:1:1的结构简式
您最近一年使用:0次