名校
解题方法
1 . 室温下,通过下列实验探究 溶液的性质。
溶液的性质。
(1)实验1的溶液中存在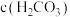
___________  (填“>”“<”或“=”)
(填“>”“<”或“=”)
(2)实验2过程中,水的电离程度___________ (填“逐渐增大”“逐渐减小”或“基本不变”)
(3)实验3反应后的溶液中,所含离子浓度大小与关系正确的是___________。
(4)从平衡移动角度解释实验4中产生气体和沉淀的原因:___________ 。
(5)若想使碳酸氢钠溶液中 的比值变小,可加入的物质是___________。
的比值变小,可加入的物质是___________。
 溶液的性质。
溶液的性质。| 实验1 | 用pH试纸测得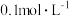  溶液的pH约为8 溶液的pH约为8 |
| 实验2 | 向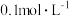  溶液中加入等体积 溶液中加入等体积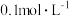 盐酸 盐酸 |
| 实验3 | 向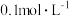  溶液中加入等体积 溶液中加入等体积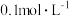 NaOH溶液 NaOH溶液 |
| 实验4 | 向浓 溶液中加入浓 溶液中加入浓 溶液,有气体和沉淀生成 溶液,有气体和沉淀生成 |
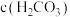
 (填“>”“<”或“=”)
(填“>”“<”或“=”)(2)实验2过程中,水的电离程度
(3)实验3反应后的溶液中,所含离子浓度大小与关系正确的是___________。
A. |
B. |
C. |
D.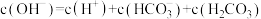 |
(5)若想使碳酸氢钠溶液中
 的比值变小,可加入的物质是___________。
的比值变小,可加入的物质是___________。| A.通入HCl | B.NaOH固体 | C.通入CO2 | D. 固体 固体 |
您最近一年使用:0次
名校
2 . 现有4.1g含杂质的烧碱样品,某小组同学为测定其纯度,将其配制成250mL待测液,准确量取10.00mL待测液,并用0.2010 mol·L-1标准盐酸滴定待测烧碱溶液(假设烧碱中不含有与酸反应的杂质),试根据实验回答。
(1)在上述溶液配制与滴定过程中,不需要用到的实验仪器是___________。
(2)选用___________ 为指示剂,滴定终点的判断依据是___________ 。
(3)根据表中数据,计算样品烧碱的质量分数为___________ (结果保留两位有效数字)。
(4)滴定过程,下列情况会使测定结果偏高的是___________。
(1)在上述溶液配制与滴定过程中,不需要用到的实验仪器是___________。
A. | B. | C. | D. |
(3)根据表中数据,计算样品烧碱的质量分数为
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
| A.量取待测液的滴定管水洗后,直接用来量取待测液 |
| B.滴定前,滴定管有气泡,滴定后消失 |
| C.滴定过程中振荡锥形瓶时不慎有少量液体溅出 |
| D.盛装待测液的锥形瓶水洗后未烘干 |
您最近一年使用:0次
名校
解题方法
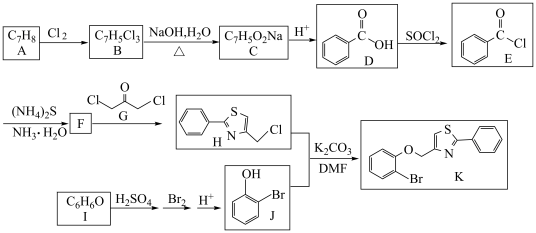
3 . 有机物K是重要的药物中间体,一种K的合成路线如下:
(1)A→B的反应条件是___________ 。D→E的反应类型为___________ 。
(2)F的结构简式为___________ 。
(3)I的化学名称是___________ 。J中官能团的名称是___________ 。
(4)反应B→C的化学方程式为___________ 。
(5)鉴别D的水溶液与I的水溶液的化学试剂为___________ 。
(6)L是D与乙醇酯化后的产物,同时满足下列条件的L的同分异构体有___________ 种;
①含有苯环;
②能发生水解反应且1molL需要2molNaOH发生反应。
其中,核磁共振氢谱有4组峰,且峰面积比为6:2:1:1的物质的结构简式为___________ (任写一种)。
已知:①
②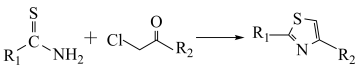
(1)A→B的反应条件是
(2)F的结构简式为
(3)I的化学名称是
(4)反应B→C的化学方程式为
(5)鉴别D的水溶液与I的水溶液的化学试剂为
(6)L是D与乙醇酯化后的产物,同时满足下列条件的L的同分异构体有
①含有苯环;
②能发生水解反应且1molL需要2molNaOH发生反应。
其中,核磁共振氢谱有4组峰,且峰面积比为6:2:1:1的物质的结构简式为
您最近一年使用:0次
名校
4 . 氟他胺 是一种可用于治疗肿瘤的药物。实验室由芳香烃
是一种可用于治疗肿瘤的药物。实验室由芳香烃 制备
制备 的合成路线如图所示:
的合成路线如图所示: 的名称是
的名称是_______ 。
(2)反应③所需的无机试剂及反应条件是_______ 。
(3) 含有的官能团的名称是
含有的官能团的名称是_______ 。
(4)反应⑤的化学方程式是_______ 。
(5)下列说法正确的是_________
a.①、③、⑥均属于取代反应
b.化合物 可以与溴水发生取代反应
可以与溴水发生取代反应
c. 中有三种官能团
中有三种官能团
(6)已知 在一定条件下水解生成
在一定条件下水解生成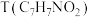 。
。 存在多种同分异构体,写出符合下列条件的
存在多种同分异构体,写出符合下列条件的 的同分异构体的结构简式:
的同分异构体的结构简式:_______ 。
① 直接连在苯环上;
直接连在苯环上;
②结构中含有酯基
③核磁共振氢谱有 组峰,且峰面积比为
组峰,且峰面积比为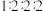
 是一种可用于治疗肿瘤的药物。实验室由芳香烃
是一种可用于治疗肿瘤的药物。实验室由芳香烃 制备
制备 的合成路线如图所示:
的合成路线如图所示: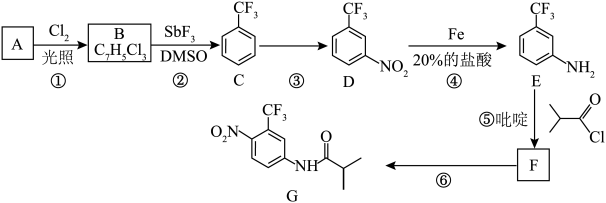
 的名称是
的名称是(2)反应③所需的无机试剂及反应条件是
(3)
 含有的官能团的名称是
含有的官能团的名称是(4)反应⑤的化学方程式是
(5)下列说法正确的是
a.①、③、⑥均属于取代反应
b.化合物
 可以与溴水发生取代反应
可以与溴水发生取代反应c.
 中有三种官能团
中有三种官能团(6)已知
 在一定条件下水解生成
在一定条件下水解生成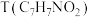 。
。 存在多种同分异构体,写出符合下列条件的
存在多种同分异构体,写出符合下列条件的 的同分异构体的结构简式:
的同分异构体的结构简式:①
 直接连在苯环上;
直接连在苯环上;②结构中含有酯基
③核磁共振氢谱有
 组峰,且峰面积比为
组峰,且峰面积比为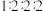
您最近一年使用:0次
7日内更新
|
91次组卷
|
2卷引用:河南省商丘市十校联考2023-2024学年高二下学期期末考试化学试题
名校
5 . 锑(Sb)是银白色金属,广泛应用于电气、医药等领域。某科研小组从精炼铋烟尘(主要成分为 、
、 、
、 等)中提炼金属锑的流程如图所示:
等)中提炼金属锑的流程如图所示: 、
、 、
、 。
。
② 易水解生成两种氯氧锑沉淀
易水解生成两种氯氧锑沉淀 、
、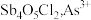 、
、 在上述情况下水解非常微弱。
在上述情况下水解非常微弱。
③ “还原熔炼”的主要反应为 ,熔炼过程中原料之间可能会形成泡渣而结块。
,熔炼过程中原料之间可能会形成泡渣而结块。
回答下列问题:
(1)基态 的价电子排布式为
的价电子排布式为_______ 。
(2)“水解”步骤发生的反应为 、
、 ,加入少量水时,
,加入少量水时, 的水解产物以
的水解产物以_______  填化学式
填化学式 为主;促进
为主;促进 转化为
转化为 的措施有
的措施有_______ (任写一种)。
(3)“转化”步骤中 转化为
转化为 的化学方程式为
的化学方程式为_______ 。
(4)“还原熔炼”时碳的用量对锑回收率的影响如图 所示。碳用量超过
所示。碳用量超过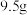 时,锑的回收率降低的原因可能是
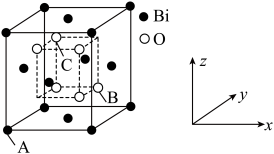
时,锑的回收率降低的原因可能是_______ 。 的立方晶胞结构如图所示
的立方晶胞结构如图所示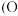 占据部分
占据部分 的四面体空隙
的四面体空隙 ,以
,以 点为原点建立分数坐标,已知
点为原点建立分数坐标,已知 点坐标为
点坐标为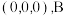 点坐标为
点坐标为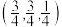 ,则
,则 点坐标为
点坐标为_______ 。晶胞边长为 ,则密度为
,则密度为_______ g cm-3(
cm-3( 的摩尔质量为
的摩尔质量为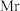 ,阿伏加德罗常数为
,阿伏加德罗常数为 )
)
 、
、 、
、 等)中提炼金属锑的流程如图所示:
等)中提炼金属锑的流程如图所示: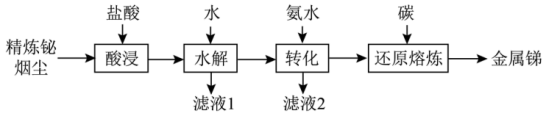
 、
、 、
、 。
。②
 易水解生成两种氯氧锑沉淀
易水解生成两种氯氧锑沉淀 、
、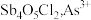 、
、 在上述情况下水解非常微弱。
在上述情况下水解非常微弱。③ “还原熔炼”的主要反应为
 ,熔炼过程中原料之间可能会形成泡渣而结块。
,熔炼过程中原料之间可能会形成泡渣而结块。回答下列问题:
(1)基态
 的价电子排布式为
的价电子排布式为(2)“水解”步骤发生的反应为
 、
、 ,加入少量水时,
,加入少量水时, 的水解产物以
的水解产物以 填化学式
填化学式 为主;促进
为主;促进 转化为
转化为 的措施有
的措施有(3)“转化”步骤中
 转化为
转化为 的化学方程式为
的化学方程式为(4)“还原熔炼”时碳的用量对锑回收率的影响如图
 所示。碳用量超过
所示。碳用量超过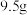 时,锑的回收率降低的原因可能是
时,锑的回收率降低的原因可能是
 的立方晶胞结构如图所示
的立方晶胞结构如图所示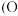 占据部分
占据部分 的四面体空隙
的四面体空隙 ,以
,以 点为原点建立分数坐标,已知
点为原点建立分数坐标,已知 点坐标为
点坐标为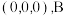 点坐标为
点坐标为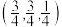 ,则
,则 点坐标为
点坐标为 ,则密度为
,则密度为 cm-3(
cm-3( 的摩尔质量为
的摩尔质量为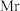 ,阿伏加德罗常数为
,阿伏加德罗常数为 )
)
您最近一年使用:0次
7日内更新
|
75次组卷
|
2卷引用:河南省商丘市十校联考2023-2024学年高二下学期期末考试化学试题
名校
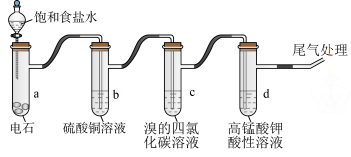
6 . I.如图是制备和研究乙炔性质的实验装置图。_______ 。
(2)b的作用是_______ 。
(3)c中溶液褪色,生成物的结构简式是_______ 。
(4)d中高锰酸钾酸性溶液褪色,说明乙炔具有的性质是_______ 。
(5)若在空气中点燃乙炔,可观察到的实验现象是_______ 。
II.某有机化合物只含 、
、 、
、 三种元素,取
三种元素,取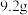 该有机化合物完全燃烧,测得只生成
该有机化合物完全燃烧,测得只生成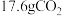 和
和 水,其质谱图和核磁共振氢谱如图所示,
水,其质谱图和核磁共振氢谱如图所示,_______
(7)有机物 的系统命名为
的系统命名为_______ 。
(8)分子式为 ,且属于烯烃的同分异构体有
,且属于烯烃的同分异构体有_______ 种(考虑顺反异构)。
(2)b的作用是
(3)c中溶液褪色,生成物的结构简式是
(4)d中高锰酸钾酸性溶液褪色,说明乙炔具有的性质是
(5)若在空气中点燃乙炔,可观察到的实验现象是
II.某有机化合物只含
 、
、 、
、 三种元素,取
三种元素,取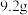 该有机化合物完全燃烧,测得只生成
该有机化合物完全燃烧,测得只生成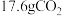 和
和 水,其质谱图和核磁共振氢谱如图所示,
水,其质谱图和核磁共振氢谱如图所示,
(7)有机物
 的系统命名为
的系统命名为(8)分子式为
 ,且属于烯烃的同分异构体有
,且属于烯烃的同分异构体有
您最近一年使用:0次
7日内更新
|
83次组卷
|
2卷引用:河南省商丘市十校联考2023-2024学年高二下学期期末考试化学试题
解题方法
7 . 及其化合物在合金工业、制药工业、电池工业有广泛的应用。回答下列问题:
(1)镓的卤化物熔点如表所示:
由表中数据可知 属于
属于___________ 晶体。
(2)镓与铝是同主族元素,性质相似。下列有关镓及其化合物的说法正确的是___________(填字母)。
(3)一种含镓的药物合成方法如图所示;___________ ,化合物I中所含元素的电负性由大到小的顺序为___________ (用元素符号表示)。
②x=___________ 。
(4)如图是氮化镓的一种晶胞结构图。___________ 。
②若晶体结构中Ga和N的最短距离为x nm,则晶体的密度为___________  。
。
(1)镓的卤化物熔点如表所示:
| 物质 |  |  | 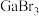 |  |
| 熔点/℃ | 1000 | 78 | 124 | 213 |
 属于
属于(2)镓与铝是同主族元素,性质相似。下列有关镓及其化合物的说法正确的是___________(填字母)。
A.基态Ga原子价层电子的轨道表示式: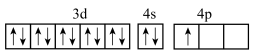 |
| B.常温下,Ga可与水剧烈反应放出氢气 |
C.一定条件下, 可与NaOH反应生成盐 可与NaOH反应生成盐 |
D. 可由 可由 受热分解得到 受热分解得到 |
(3)一种含镓的药物合成方法如图所示;
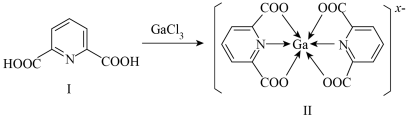
②x=
(4)如图是氮化镓的一种晶胞结构图。

②若晶体结构中Ga和N的最短距离为x nm,则晶体的密度为
 。
。
您最近一年使用:0次
解题方法
8 . 最新研究表明: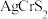 在室温下具有超离子行为,该研究成果为未来新结构二维材料的合成和探索提供了新思路。回答下列问题:
在室温下具有超离子行为,该研究成果为未来新结构二维材料的合成和探索提供了新思路。回答下列问题:
(1)基态Cr原子价层电子的轨道表达式为___________ ,同周期元素的基态原子最外层电子数与Cr相同的元素为___________ (填元素符号)。
(2)哈勃—韦斯(Haber-Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是:其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。则
___________ (填“能”或“不能”)催化双氧水分解。
(3) 中配体分子
中配体分子 、
、 以及
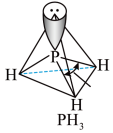
以及 分子的空间结构如图所示。
分子的空间结构如图所示。 中
中 键的数目为
键的数目为___________ ( 为阿伏加德罗常数的值),
为阿伏加德罗常数的值), 中P的杂化类型是
中P的杂化类型是___________ 。 的沸点比
的沸点比 的沸点
的沸点___________ (填“高”或“低”),原因是___________ ;水分子中H―O键的极性___________ (填“大于”“小于”或“等于”) 分子中N―H键的极性。
分子中N―H键的极性。
(4)氮化铬的晶胞结构如图所示,A点分数坐标为 。氮化铬的晶体密度为
。氮化铬的晶体密度为 ,
, 代表阿伏加德罗常数的值。
代表阿伏加德罗常数的值。___________ 。
②晶胞参数为___________ nm(写出表达式)。
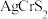 在室温下具有超离子行为,该研究成果为未来新结构二维材料的合成和探索提供了新思路。回答下列问题:
在室温下具有超离子行为,该研究成果为未来新结构二维材料的合成和探索提供了新思路。回答下列问题:(1)基态Cr原子价层电子的轨道表达式为
(2)哈勃—韦斯(Haber-Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是:其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。则

(3)
 中配体分子
中配体分子 、
、 以及
以及 分子的空间结构如图所示。
分子的空间结构如图所示。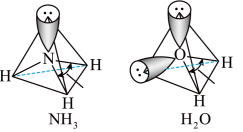
 中
中 键的数目为
键的数目为 为阿伏加德罗常数的值),
为阿伏加德罗常数的值), 中P的杂化类型是
中P的杂化类型是 的沸点比
的沸点比 的沸点
的沸点 分子中N―H键的极性。
分子中N―H键的极性。(4)氮化铬的晶胞结构如图所示,A点分数坐标为
 。氮化铬的晶体密度为
。氮化铬的晶体密度为 ,
, 代表阿伏加德罗常数的值。
代表阿伏加德罗常数的值。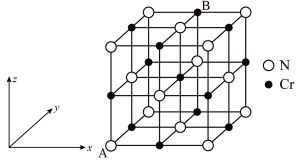
②晶胞参数为
您最近一年使用:0次
名校
解题方法
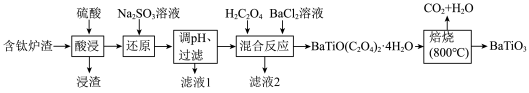
9 . BaTiO3,被用作陶瓷电容器的介电材料、麦克风和其他传感器的压电材料。以含钛炉渣(主要成分是TiO2,含少量Fe2O3、CaO、SiO2等)为原料制备BaTiO3的流程如下:
回答下列问题:
(1)下列为Ba粒子简化电子排布式,其中能量最高的是 (填字母)。
(2)“还原”中发生反应的离子方程式为________ 。若省去“还原”工艺,则________ 。
(3)设计实验检验滤液1中是否含有Fe2+:________ 。
(4)BaTiO(C2O4)2·4H2O中Ti的化合价为________ ,“焙烧”发生反应的化学方程式为________ 。
(5)经X射线分析鉴定,钛酸钡(BaTiO3)的晶胞结构如下图所示(Ti4+、Ba2+均与O2-相接触),已知晶胞边长为 pm,O2-的半径为
pm,O2-的半径为 pm,则Ti4+、Ba2+的半径分别为
pm,则Ti4+、Ba2+的半径分别为______ pm、______ pm。(用含 、
、 的代数式表示)
的代数式表示)
| 金属离子 | TiO2+ | Fe2+ | Fe3+ |
| 开始沉淀的pH | 0.5 | 6.3 | 1.5 |
| 完全沉淀的pH | 2.5 | 8.3 | 2.8 |
(1)下列为Ba粒子简化电子排布式,其中能量最高的是 (填字母)。
| A.[Xe]6s2 | B.[Xe]6s1 | C.[Xe]6s16p1 | D.[Xe]6s0p2 |
(2)“还原”中发生反应的离子方程式为
(3)设计实验检验滤液1中是否含有Fe2+:
(4)BaTiO(C2O4)2·4H2O中Ti的化合价为
(5)经X射线分析鉴定,钛酸钡(BaTiO3)的晶胞结构如下图所示(Ti4+、Ba2+均与O2-相接触),已知晶胞边长为
 pm,O2-的半径为
pm,O2-的半径为 pm,则Ti4+、Ba2+的半径分别为
pm,则Ti4+、Ba2+的半径分别为 、
、 的代数式表示)
的代数式表示)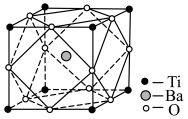
您最近一年使用:0次
名校
解题方法
10 . 某柔性屏手机的柔性电池以碳纳米管作电极材料,以吸收 溶液的有机高聚物(结构片段如图所示)作固态电解质,其电池总反应为
溶液的有机高聚物(结构片段如图所示)作固态电解质,其电池总反应为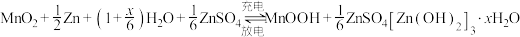 ,电池结构如图所示。
,电池结构如图所示。
(1)如图所示的几种含碳物质中,不与碳纳米管互为同素异形体的是___________ (填名称,下同),存在分子间作用力的是___________ ;属于共价晶体的是___________ 。 中
中 的化合价是
的化合价是_________ ,有机高聚物中C的杂化方式为__________ 。
(3) 键中离子键成分的百分数小于
键中离子键成分的百分数小于 键,原因是
键,原因是___________ 。 的第二电离能
的第二电离能___________ (填“大于”或“小于”) 。
。
(4)一种新型稀磁半导体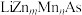 的立方晶胞结构如图所示。
的立方晶胞结构如图所示。___________ ,n=___________ 。
②已知 为阿伏加德罗常数的值,
为阿伏加德罗常数的值,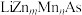 的摩尔质量为
的摩尔质量为 ,晶体密度为
,晶体密度为 。该晶体中
。该晶体中 原子与
原子与 原子之间的最短距离为
原子之间的最短距离为___________ nm(列出计算式)。
 溶液的有机高聚物(结构片段如图所示)作固态电解质,其电池总反应为
溶液的有机高聚物(结构片段如图所示)作固态电解质,其电池总反应为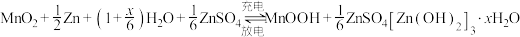 ,电池结构如图所示。
,电池结构如图所示。
(1)如图所示的几种含碳物质中,不与碳纳米管互为同素异形体的是

 中
中 的化合价是
的化合价是(3)
 键中离子键成分的百分数小于
键中离子键成分的百分数小于 键,原因是
键,原因是 的第二电离能
的第二电离能 。
。(4)一种新型稀磁半导体
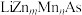 的立方晶胞结构如图所示。
的立方晶胞结构如图所示。
②已知
 为阿伏加德罗常数的值,
为阿伏加德罗常数的值,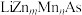 的摩尔质量为
的摩尔质量为 ,晶体密度为
,晶体密度为 。该晶体中
。该晶体中 原子与
原子与 原子之间的最短距离为
原子之间的最短距离为
您最近一年使用:0次



