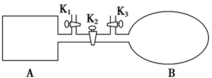
1 . A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的透明气球。关闭 ,将等量且少量的
,将等量且少量的 通过
通过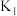 、
、 分别充入A、B中,反应起始时,A、B的体积相同
分别充入A、B中,反应起始时,A、B的体积相同 已知:
已知: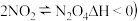 。下列叙述正确的是
。下列叙述正确的是
 ,将等量且少量的
,将等量且少量的 通过
通过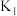 、
、 分别充入A、B中,反应起始时,A、B的体积相同
分别充入A、B中,反应起始时,A、B的体积相同 已知:
已知: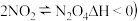 。下列叙述正确的是
。下列叙述正确的是
A.达到平衡时A和B中 气体体积分数相同 气体体积分数相同 |
B.若在A、B中再充入与初始量相等的 ,再次达到平衡后A中 ,再次达到平衡后A中 转化率增大,B中 转化率增大,B中 转化率不变 转化率不变 |
| C.若气球的体积不再改变,表明B中反应已达到平衡 |
| D.室温下,若设法使A、B都保持体积不变,将A套上一个绝热层,B与外界可以进行热传递,则达到平衡时B中气体的颜色较深 |
您最近一年使用:0次
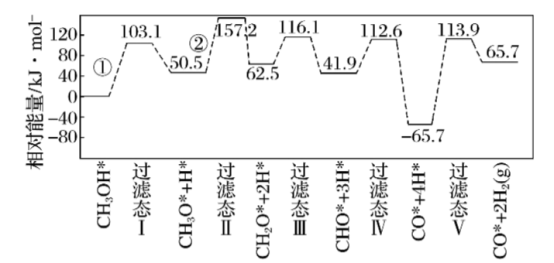
2 . 工业上可采用CH3OH CO+2H2的方法来制取高纯度的CO和H2。我国科研人员通过计算机模拟,研究了在钯基催化剂表面甲醇制氢的反应历程如图所示,其中吸附在钯催化剂表面上的物种用
CO+2H2的方法来制取高纯度的CO和H2。我国科研人员通过计算机模拟,研究了在钯基催化剂表面甲醇制氢的反应历程如图所示,其中吸附在钯催化剂表面上的物种用 标注。下列说法正确的是
标注。下列说法正确的是
CHO*+3H*→CO*+4H*
已知:甲醇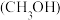 脱氢反应的第一步历程,有两种可能方式:
脱氢反应的第一步历程,有两种可能方式:
方式Ⅰ:

方式Ⅱ:

 CO+2H2的方法来制取高纯度的CO和H2。我国科研人员通过计算机模拟,研究了在钯基催化剂表面甲醇制氢的反应历程如图所示,其中吸附在钯催化剂表面上的物种用
CO+2H2的方法来制取高纯度的CO和H2。我国科研人员通过计算机模拟,研究了在钯基催化剂表面甲醇制氢的反应历程如图所示,其中吸附在钯催化剂表面上的物种用 标注。下列说法正确的是
标注。下列说法正确的是
CHO*+3H*→CO*+4H*
已知:甲醇
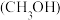 脱氢反应的第一步历程,有两种可能方式:
脱氢反应的第一步历程,有两种可能方式:方式Ⅰ:


方式Ⅱ:


A.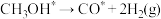 的 的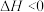 |
| B.①②都为O—H键的断裂过程 |
| C.由活化能E值推测,甲醇脱氢过程主要历经的方式应为Ⅰ |
D.放热最多阶段的化学方程式为 |
您最近一年使用:0次
解题方法
3 . 最近科学家研发了“全氢电池”,其工作原理如图所示。下列说法不正确的是
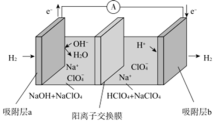

| A.吸附层a是负极,发生氧化反应,吸附层b是正极,发生还原反应 |
| B.“全氢电池”的总反应为:H+ + OH-=H2O |
| C.NaClO4的作用是传导离子并参与电极反应 |
D.Na+在装置中从左侧向右侧移动,ClO 从右侧向左侧移动 从右侧向左侧移动 |
您最近一年使用:0次
4 . 室温下,向20 mL含有0.10 mol/L Cr2+和0.10mol/L Fe2+的混合溶液中滴加0.10 mol/L NaOH溶液,金属阳离子的浓度与滴入NaOH溶液体积的关系如图所示。若溶液中金属阳离子浓度小于10-5 mol/L可视为完全沉淀,则下列说法正确的是

已知Ksp [Cr(OH)2]=2.0×10-16 mol3/L3,Ksp [Fe(OH)2]=8.0×10-16 mol3/L3

已知Ksp [Cr(OH)2]=2.0×10-16 mol3/L3,Ksp [Fe(OH)2]=8.0×10-16 mol3/L3
| A.曲线A表示c(Cr2+)与NaOH溶液体积的关系 |
| B.当V(NaOH)=30mL时,Cr2+刚刚开始沉淀 |
| C.当pH=7时,溶液中Fe2+、Cr2+均未完全沉淀 |
| D.当Cr(OH)2和Fe(OH)2都析出时,溶液中c(Fe2+):c(Cr2+)=4∶1 |
您最近一年使用:0次
解题方法
5 . 短周期主族元素X、Y、Z、W的原子序数依次增大,其中X、Y、W分别位于不同的周期,且最外层电子数之和为9.Y的简单氢化物可用作制冷剂,X和Z可以形成X2Z和X2Z2两种分子。下列说法不正确的是
| A.Z的简单离子比W的简单离子半径小 |
| B.Z的简单氢化物的热稳定性比Y的弱 |
| C.Y和Z都能与X形成既含极性键又含非极性键的分子 |
| D.W和Y的最高价氧化物对应的水化物能相互反应 |
您最近一年使用:0次
解题方法
6 . 某无色澄清溶液中可能含有:①Na+② ③Cl-④
③Cl-④ ⑤
⑤ ⑥H+⑦Cu2+中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
⑥H+⑦Cu2+中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
下列结论正确的是
 ③Cl-④
③Cl-④ ⑤
⑤ ⑥H+⑦Cu2+中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
⑥H+⑦Cu2+中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:| 步骤 | 操作 | 现象 |
| (1) | 用紫色石蕊试液检验 | 溶液变红 |
| (2) | 向溶液中滴加BaCl2溶液和稀盐酸 | 有白色沉淀生成 |
| (3) | 将(2)中所得混合物过滤,向滤液中加入AgNO3溶液和稀HNO3 | 有白色沉淀生成 |
| A.该实验无法确定是否含有③ |
| B.肯定含有的离子是②③⑥ |
| C.可能含有的离子是①③⑦ |
| D.肯定没有的离子是④⑤⑦,可能含有的离子是①③ |
您最近一年使用:0次
2021-02-23更新
|
137次组卷
|
2卷引用:湖北省鄂州市2020-2021学年高一上学期期末质量监测化学试题
名校
7 . 如图所示,左室容积为右室的两倍,温度相同,现分别按照如图所示的量充入气体,同时加入少量固体催化剂使两室内气体充分反应达到平衡,打开活塞,继续反应再次达到平衡,下列说法正确的是( )
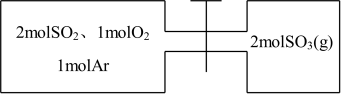

| A.第一次平衡时,SO2的物质的量左室更多 |
| B.充入气体未反应前,左室压强比右室大 |
| C.第一次平衡时,左室内压强一定小于右室 |
| D.第二次平衡时,SO2的总物质的量比第一次平衡时左室SO2的物质的量的2倍还要多 |
您最近一年使用:0次
2020-11-26更新
|
398次组卷
|
6卷引用:湖北省鄂州市部分高中联考协作体2020-2021学年高二上学期期中考试化学试题
解题方法
8 . CO常用于工业冶炼金属,如图是在不同温度下CO还原四种金属氧化物达平衡后气体中lg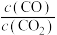 与温度(T)的关系曲线图。下列说法正确的是( )
与温度(T)的关系曲线图。下列说法正确的是( )

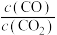 与温度(T)的关系曲线图。下列说法正确的是( )
与温度(T)的关系曲线图。下列说法正确的是( )
| A.工业上可以通过增高反应装置来延长矿石和CO接触的时间,减少尾气中CO的含量 |
| B.CO不适宜用于工业冶炼金属铬(Cr) |
| C.工业冶炼金属铜(Cu)时较高的温度有利于提高CO的利用率 |
| D.CO还原PbO2的反应ΔH<0 |
您最近一年使用:0次
9 . 对于2NO(g)+2CO(g) N2(g)+2CO2(g),于1 L的恒容密闭容器中进行反应。下列能说明该反应已经达到平衡状态的是( )
N2(g)+2CO2(g),于1 L的恒容密闭容器中进行反应。下列能说明该反应已经达到平衡状态的是( )
 N2(g)+2CO2(g),于1 L的恒容密闭容器中进行反应。下列能说明该反应已经达到平衡状态的是( )
N2(g)+2CO2(g),于1 L的恒容密闭容器中进行反应。下列能说明该反应已经达到平衡状态的是( )| A.c(CO)=c(CO2) | B.容器中混合气体的密度不变 |
| C.2v(N2)正=v(NO)逆 | D.容器中混合气体的平均摩尔质量不变 |
您最近一年使用:0次
10 . 下列说法正确的是( )
| A.已知冰的熔化热为6.0 kJ·mol-1,冰中氢键键能为20 kJ·mol-1,假设1 mol冰中有2 mol氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键 |
| B.已知氯气、溴蒸气分别与氢气反应的热化学方程式为H2(g)+Cl2(g)=2HCl(g) ΔH1;H2(g)+Br2(g)=2HBr(g) ΔH2,则ΔH1<ΔH2 |
| C.需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应 |
D.已知:①反应H2(g)+Cl2(g)=2HCl(g) ΔH=-a kJ·mol-1,②  ,且a、b、c均大于零,则断开1 mol H—Cl键所需的能量为(a+b+c)kJ ,且a、b、c均大于零,则断开1 mol H—Cl键所需的能量为(a+b+c)kJ |
您最近一年使用:0次



