名校
1 . 回答下列问题
(1)现有5种元素A、B、C、D、E,其中有3种金属元素,1种稀有气体元素,其I1~I3分别如下表。
根据表中数据判断其中的金属元素为___________ ,稀有气体元素为___________ ,显正二价的金属元素是___________ 。(填字母)
(2)水分子是H2O而不是H3O,是因为共价键具有___________ 性;水分子的键角为105°,是因为共价键具有___________ 性。
(3)1mol乙酸分子CH3COOH中含有的π键与σ键的数目之比为___________ 。
(4)已知NH5为离子化合物,则1molNH5晶体中含有的共价键数目为___________ 。
(1)现有5种元素A、B、C、D、E,其中有3种金属元素,1种稀有气体元素,其I1~I3分别如下表。
| 元素 | I1/eV | I2/eV | I3/eV |
| A | 13.0 | 23.9 | 40.0 |
| B | 4.3 | 31.9 | 47.8 |
| C | 5.7 | 47.4 | 71.8 |
| D | 7.7 | 15.1 | 80.3 |
| E | 21.6 | 41.1 | 65.2 |
(2)水分子是H2O而不是H3O,是因为共价键具有
(3)1mol乙酸分子CH3COOH中含有的π键与σ键的数目之比为
(4)已知NH5为离子化合物,则1molNH5晶体中含有的共价键数目为
您最近一年使用:0次
2 . 根据表中数据(室温),回答下列问题:
已知氢氟酸、醋酸、次氯酸(HClO)、碳酸的电离常数分别为:
(1)写出以下反应的离子方程式:
①足量的氢氟酸与碳酸钠溶液混合:___________ ;
②少量的CO2通入NaClO溶液:___________ 。
(2)25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)___________ mol/L(填精确值), =
=___________ 。
(3)25℃时,将pH=3的H2SO4溶液和pH=12的NaOH溶液混合,充分混合后所得溶液的pH=10,则H2SO4溶液与NaOH溶液的体积比为___________ 。
(4)室温下pH=9的NaOH溶液和pH=10的CH3COONa溶液,设由水电离产生的OH﹣的物质的量浓度分别为A和B,则A/B等于___________ 。
(5)甲醇与CO可以生成醋酸,常温下将amol/L的醋酸与bmol∙L-1Ba(OH)2溶液以2∶1体积比混合,混合溶液中2c(Ba2+)=c(CH3COO-),则醋酸的电离平衡常数为_______ (用含a和b的代数式表示)。
已知氢氟酸、醋酸、次氯酸(HClO)、碳酸的电离常数分别为:
| HF | Ka=6.8×10-4mol•L-1 |
| CH3COOH | Ka=1.7×10-5mol•L-1 |
| HClO | Ka=2.9×10-8mol•L-1 |
| H2CO3 | Ka1=4.4×10-7mol•L-1 Ka2=4.7×10-11mol•L-1 |
①足量的氢氟酸与碳酸钠溶液混合:
②少量的CO2通入NaClO溶液:
(2)25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)
 =
=(3)25℃时,将pH=3的H2SO4溶液和pH=12的NaOH溶液混合,充分混合后所得溶液的pH=10,则H2SO4溶液与NaOH溶液的体积比为
(4)室温下pH=9的NaOH溶液和pH=10的CH3COONa溶液,设由水电离产生的OH﹣的物质的量浓度分别为A和B,则A/B等于
(5)甲醇与CO可以生成醋酸,常温下将amol/L的醋酸与bmol∙L-1Ba(OH)2溶液以2∶1体积比混合,混合溶液中2c(Ba2+)=c(CH3COO-),则醋酸的电离平衡常数为
您最近一年使用:0次
3 . 工业废水中含 会污染环境,必须进行处理。某化学兴趣小组设计了三种方案。
会污染环境,必须进行处理。某化学兴趣小组设计了三种方案。
方案1:还原法。
处理工艺流程如下:

(1) 中铬元素的化合价为
中铬元素的化合价为_____ 。
(2)下列溶液中,可替代 的是_____(填选项序号字母)。
的是_____(填选项序号字母)。
(3)常温下, 的
的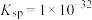 ,当
,当 恰好完全沉淀时(当离子浓度为
恰好完全沉淀时(当离子浓度为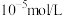 ,可认为离子完全沉淀),溶液的
,可认为离子完全沉淀),溶液的
_____ 。
(4)用离子方程式表示水溶液中 转化为
转化为 的平衡
的平衡_____ ;
方案2:电解法。
下图是以 处理含的酸性废水的电解装置示意图(电极材料分别为铁和石墨)。
处理含的酸性废水的电解装置示意图(电极材料分别为铁和石墨)。

(5)装置中b电极反应式为_____ 。该处理过程中, 被还原成
被还原成 的离子方程式为
的离子方程式为_____ 。若处理 ,电路中转移电子的数目最少为
,电路中转移电子的数目最少为_____ 。
 会污染环境,必须进行处理。某化学兴趣小组设计了三种方案。
会污染环境,必须进行处理。某化学兴趣小组设计了三种方案。方案1:还原法。
处理工艺流程如下:

(1)
 中铬元素的化合价为
中铬元素的化合价为(2)下列溶液中,可替代
 的是_____(填选项序号字母)。
的是_____(填选项序号字母)。A. 溶液 溶液 | B.浓 溶液 溶液 |
C.酸性 溶液 溶液 | D. 溶液 溶液 |
 的
的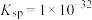 ,当
,当 恰好完全沉淀时(当离子浓度为
恰好完全沉淀时(当离子浓度为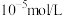 ,可认为离子完全沉淀),溶液的
,可认为离子完全沉淀),溶液的
(4)用离子方程式表示水溶液中
 转化为
转化为 的平衡
的平衡方案2:电解法。
下图是以
 处理含的酸性废水的电解装置示意图(电极材料分别为铁和石墨)。
处理含的酸性废水的电解装置示意图(电极材料分别为铁和石墨)。
(5)装置中b电极反应式为
 被还原成
被还原成 的离子方程式为
的离子方程式为 ,电路中转移电子的数目最少为
,电路中转移电子的数目最少为
您最近一年使用:0次
名校
解题方法
4 . 化学与生产生活、社会发展息息相关,下列说法正确的是
| A.C919大型客机使用的碳纤维材料属于有机高分子材料 |
| B.碘酒、“84”消毒液、75%的酒精、生理盐水都可用于消毒 |
| C.发泡塑料盒不适合于盛放含油较多的食品,可用于微波炉加热 |
| D.战国·曾侯乙编钟属于青铜制品,青铜是我国使用最早的合金 |
您最近一年使用:0次
5 . 下列说法正确的是
①Be与Al在周期表中处于对角线位置,可推出:Be(OH)2+2OH-=BeO +2H2O
+2H2O
②最外层电子数为ns2的元素都在元素化学性质都相似
③充有氖气的霓虹灯管通电时会发出红色光的主要原因,是电子由基态向激发态跃迁
时吸收除红光以外的光线
④某价层电子排布为4d54s1的基态原子,该元素位于周期表中第四周期第ⅠB族
⑤电子云图中的小黑点的疏密程度表示电子在原子核外单位体积内出现概率的大小
①Be与Al在周期表中处于对角线位置,可推出:Be(OH)2+2OH-=BeO
 +2H2O
+2H2O②最外层电子数为ns2的元素都在元素化学性质都相似
③充有氖气的霓虹灯管通电时会发出红色光的主要原因,是电子由基态向激发态跃迁
时吸收除红光以外的光线
④某价层电子排布为4d54s1的基态原子,该元素位于周期表中第四周期第ⅠB族
⑤电子云图中的小黑点的疏密程度表示电子在原子核外单位体积内出现概率的大小
| A.③⑤ | B.①②⑤ | C.②③④ | D.①⑤ |
您最近一年使用:0次
名校
解题方法
6 . 下列实验装置能达到对应实验目、实验结论正确的是
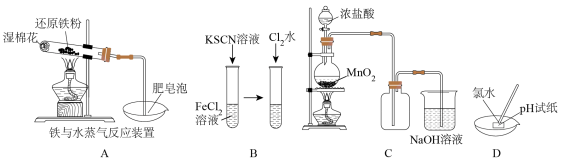

| A.过量铁粉与水蒸气反应后,可用磁铁将剩余铁粉分离出来 |
| B.用图装置操作方法,可检验Fe2+ |
| C.若二氧化锰过量,则盐酸可全部消耗完 |
| D.测新制氯水的pH值 |
您最近一年使用:0次
2023-09-04更新
|
428次组卷
|
2卷引用:辽宁省大连市第八中学2021-2022学年高一上学期12月月考化学试题
名校
7 . 下列有关叙述正确的有几个:
①工业上通常采用铁触媒、400~500℃和10MPa~30Mpa的条件下合成氨。
②等体积、等pH的盐酸和醋酸,分别与等浓度的NaOH反应,醋酸消耗的NaOH体积大。
③为了除去除垢中的CaSO4,可用Na2CO3溶液浸泡水垢,使之转化为疏松、易溶于酸的CaCO3,然后用酸除去。
④将AlCl3溶液加热蒸干并灼烧,所得产物是Al(OH)3
⑤强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强
⑥医疗上使用BaSO4作“钡餐”,而不使用BaCO3,与沉淀溶解平衡无关。
⑦反应CaSO4(s)=CaO(s)+SO3(g) ΔH>0在高温下能自发进行
⑧用标准HCl溶液滴定NaHCO3溶液来测定其浓度,选择酚酞为指示剂
⑨通过压缩体积增大压强,可以提高单位体积内活化分子百分数,从而提高反应速率
⑩在中和热的测定实验中,每组实验至少三次使用温度计。
①工业上通常采用铁触媒、400~500℃和10MPa~30Mpa的条件下合成氨。
②等体积、等pH的盐酸和醋酸,分别与等浓度的NaOH反应,醋酸消耗的NaOH体积大。
③为了除去除垢中的CaSO4,可用Na2CO3溶液浸泡水垢,使之转化为疏松、易溶于酸的CaCO3,然后用酸除去。
④将AlCl3溶液加热蒸干并灼烧,所得产物是Al(OH)3
⑤强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强
⑥医疗上使用BaSO4作“钡餐”,而不使用BaCO3,与沉淀溶解平衡无关。
⑦反应CaSO4(s)=CaO(s)+SO3(g) ΔH>0在高温下能自发进行
⑧用标准HCl溶液滴定NaHCO3溶液来测定其浓度,选择酚酞为指示剂
⑨通过压缩体积增大压强,可以提高单位体积内活化分子百分数,从而提高反应速率
⑩在中和热的测定实验中,每组实验至少三次使用温度计。
| A.3 | B.4 | C.5 | D.6 |
您最近一年使用:0次
名校
8 . 由金、氯、铯三种元素组成的晶体M的晶胞结构如图所示( 为铯,
为铯, 为氯,
为氯, 为金),其中金原子有两种不同的化学环境,形成2种−1价的配离子。设阿伏加德罗常数的值为NA,下列说法错误的是
为金),其中金原子有两种不同的化学环境,形成2种−1价的配离子。设阿伏加德罗常数的值为NA,下列说法错误的是

 为铯,
为铯, 为氯,
为氯, 为金),其中金原子有两种不同的化学环境,形成2种−1价的配离子。设阿伏加德罗常数的值为NA,下列说法错误的是
为金),其中金原子有两种不同的化学环境,形成2种−1价的配离子。设阿伏加德罗常数的值为NA,下列说法错误的是
| A.M的化学式为CsAuCl |
B.金原子形成的两种配离子分别为AuCl 、AuCl 、AuCl |
| C.位于体心的Au处于由Au构成的八面体空隙中 |
D.金晶体(Au)是面心立方堆积,其晶胞参数为408pm,金晶体密度为 g∙cm−3 g∙cm−3 |
您最近一年使用:0次
2022-09-11更新
|
343次组卷
|
2卷引用:辽宁省抚顺市第二中学2021-2022学年高三上学期10月月考化学试题
解题方法
9 . 我国提出争取在2030年前实现碳达峰,2060年前实现碳中和,这对于改善环境、实现绿色发展至关重要。因此,研发二氧化碳利用技术、降低空气中二氧化碳含量成为研究热点。回答下列问题:
(1)某模拟“人工树叶”的电化学实验装置如图1所示,该装置能将H2O和CO2转化为O2和丙醇(C3H8O)燃料,所有气体均换算成标准状况下。
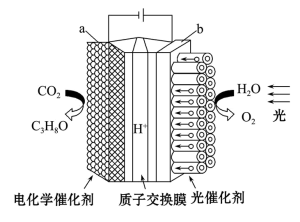
图1
①a电极为电解池的____ (填“阴极”或“阳极”),发生____ (填“氧化”或“还原”)反应。
②b电极上的电极反应式为____ ,每消耗5.6LCO2,同时生成O2的质量为____ g。
(2)利用如图2所示装置从海水中提取CO2,有利于减少温室气体的含量。
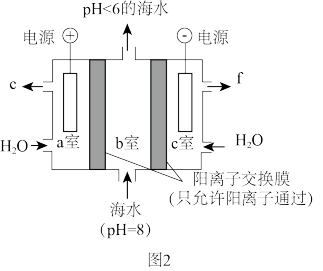
①气体e为____ (填化学式)。
②电解过程中产生的H+通过阳离子交换膜由____ (填“a室→b室”或“b室→a室”);海水中因含有HCO ,使得海水显碱性,写出提取CO2的离子方程式:
,使得海水显碱性,写出提取CO2的离子方程式:____ 。
(3)科学家利用电化学装置可实现CH4和CO2两种分子的耦合转化,其原理如图3所示。若生成的乙烯和乙烷的体积之比为3:4,则消耗CH4和CO2的体积之比为____ 。
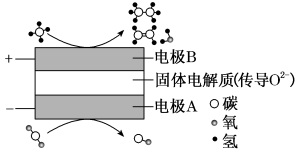
图3
(1)某模拟“人工树叶”的电化学实验装置如图1所示,该装置能将H2O和CO2转化为O2和丙醇(C3H8O)燃料,所有气体均换算成标准状况下。

图1
①a电极为电解池的
②b电极上的电极反应式为
(2)利用如图2所示装置从海水中提取CO2,有利于减少温室气体的含量。

①气体e为
②电解过程中产生的H+通过阳离子交换膜由
 ,使得海水显碱性,写出提取CO2的离子方程式:
,使得海水显碱性,写出提取CO2的离子方程式:(3)科学家利用电化学装置可实现CH4和CO2两种分子的耦合转化,其原理如图3所示。若生成的乙烯和乙烷的体积之比为3:4,则消耗CH4和CO2的体积之比为

图3
您最近一年使用:0次
10 . 室温下,向0.01mol·L-1的CH3COOH溶液中不断加水稀释,其溶液的pH变化如图所示[已知:Ka(CH3COOH)=1.6×10-5,lg2=0.3,电离度= ×100%,pH=-lgc(H+),忽略溶液体积和温度的变化],下列说法正确的是
×100%,pH=-lgc(H+),忽略溶液体积和温度的变化],下列说法正确的是

 ×100%,pH=-lgc(H+),忽略溶液体积和温度的变化],下列说法正确的是
×100%,pH=-lgc(H+),忽略溶液体积和温度的变化],下列说法正确的是
| A.x点的pH为3.2 |
| B.x点与y点CH3COOH的电离平衡常数:Kx>Ky |
| C.室温下,0.01mol·L-1的CH3COOH溶液中,CH3COOH的电离度约为4% |
| D.升高温度,c(H+)增大,Ka的大小保持不变 |
您最近一年使用:0次
2022-09-02更新
|
493次组卷
|
3卷引用:辽宁省葫芦岛市协作校2021-2022学年高二上学期第二次考试化学试题



