名校
1 . 某化学小组用图中的实验装置证明过氧化钠可用作供氧剂,有关说法错误的是


A.利用A装置可以制备 , , , , 气体 气体 |
B.B装置中应加入饱和 溶液,加入该试剂的目的是除去HCl气体 溶液,加入该试剂的目的是除去HCl气体 |
C.C装置中应加入 固体,相关反应为 固体,相关反应为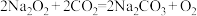 |
D.D装置中应加入浓NaOH溶液,加入该试剂的目的是除去多余的 气体 气体 |
您最近一年使用:0次
2021-12-04更新
|
246次组卷
|
4卷引用:江西省吉安市峡江中学2021-2022学年高二上学期开学考试化学(理科)试题
2 . 某化学兴趣小组设计了如下实验装置证明乙醇与Na反应产生氢气。已知:乙醇能与无水CaCl2反应生成配合物CaCl2·xCH3CH2OH。下列说法中不正确的是
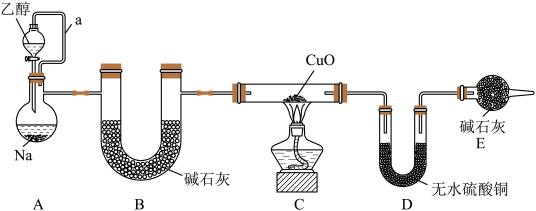
| A.a的作用是平衡气压,使乙醇液体顺利滴下 |
| B.若装置C中黑色粉末变红,D中白色粉末变蓝,即可证明乙醇与Na反应生成了氢气 |
| C.装置E的作用是防止空气中的水蒸气进入装置D中 |
| D.若将装置B中的碱石灰换成无水CaCl2,更合理 |
您最近一年使用:0次
2022-07-12更新
|
382次组卷
|
7卷引用:江西省兴国县第三中学2020-2021学年高一下学期第三次月考化学(兴特班)试题
名校
3 . (1)实验室用过量的锌和一定体积的盐酸制取氢气,如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,在盐酸中分别加入等体积的下列溶液,你认为可行的是__ (填字母)。
A.CH3COONa溶液 B.NaNO3溶液 C.KCl溶液 D.Na2CO3溶液
(2)下列说法可以证明H2(g)+I2(g) ⇌ 2HI(g)已达平衡状态的是__ 。
A.单位时间内生成nmolH2的同时,生成nmolHI
B.一个H—H键断裂的同时有两个H—I键断裂
C.温度和体积一定时,混合气体颜色不再变化
D.反应速率v(H2)=v(I2)= v(HI)
v(HI)
E.温度和体积一定时,容器内压强不再变化
F.温度和体积一定时,混合气体的密度不再变化
A.CH3COONa溶液 B.NaNO3溶液 C.KCl溶液 D.Na2CO3溶液
(2)下列说法可以证明H2(g)+I2(g) ⇌ 2HI(g)已达平衡状态的是
A.单位时间内生成nmolH2的同时,生成nmolHI
B.一个H—H键断裂的同时有两个H—I键断裂
C.温度和体积一定时,混合气体颜色不再变化
D.反应速率v(H2)=v(I2)=
 v(HI)
v(HI)E.温度和体积一定时,容器内压强不再变化
F.温度和体积一定时,混合气体的密度不再变化
您最近一年使用:0次
名校
4 . 对于 H2O2 分解反应,Cu2+也有一定的催化作用。为比较 Fe3+和 Cu2+对 H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。下列说法不正确的是

| A.图甲可通过观察气泡产生快慢来比较反应速率的大小 |
| B.用图乙装置测定反应速率时,若 10s 产生标况下氢气 22.4ml,则用氢气表示的10s 内反应速率为 0.0001mol·s-1 |
| C.图甲所示实验中,若左边试管里的反应速率大于右边的,则证明 Fe3+对 H2O2 分解的催化效果比 Cu2+的好 |
| D.为检查乙装置的气密性,可关闭 a 处旋塞,将注射器活塞拉出一定距离,一段时间后松 开活塞,观察活塞是否回到原位 |
您最近一年使用:0次
2021-10-16更新
|
306次组卷
|
3卷引用:江西省临川第十中学2021-2022学年高二上学期第一次月考化学试题
名校
解题方法
5 . 2020年2月9日晚,湖北省新冠肺炎疫情防控指挥部的第19场新闻发布会上,华中科大公共卫生学院副院长徐顺清介绍,新型冠状病毒的主要传播途径有直接传播(飞沫传播)和接触传播,目前没有直接证据证明病毒通过气溶胶传播。下列说法不正确 的是
| A.云、烟、雾均属于气溶胶 |
| B.PM2.5是对空气中直径小于或等于2.5μm(2.5×10-6m)的固体颗粒或液滴的总称,其分散在空气中一定形成气溶胶 |
| C.胶体是混合物,可用丁达尔效应来鉴别胶体和溶液 |
| D.胶体的分散质粒子大小在1nm到l00nm之间,能通过滤纸不能透过半透膜 |
您最近一年使用:0次
2021-10-20更新
|
355次组卷
|
8卷引用:江西省丰城市第九中学2021-2022学年高一上学期期中考试(日新班)化学试题
名校
解题方法
6 . 25°C时,下列说法不正确的是
| A.等体积Na2CO3和NaHCO3溶液,以甲基橙作指示剂,达滴定终点时,消耗等量的HCl标准液,则NaHCO3浓度更大 |
| B.欲证明HA为弱酸,可将pH=3的HA溶液稀释为原体积的10倍后,测定pH>4 |
C.均为0.10 mol·L-1的Na2CO3、Na2SO3、Na2SO4溶液中阴离子的浓度依次减小〔已知:Ka(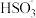 )=6.1×10-8;Ka( )=6.1×10-8;Ka( )=4.7×10-11〕 )=4.7×10-11〕 |
| D.常温下pH=11的纯碱溶液中水电离产生的n(H+)大于该溶液中n(H+) |
您最近一年使用:0次
2021-09-06更新
|
529次组卷
|
4卷引用:江西省南昌市2022届高三摸底考试化学试题
名校
解题方法
7 . 对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。下列说法不正确的是


| A.图甲可通过观察气泡产生快慢来比较反应速率的大小 |
| B.图甲所示实验中,若左边试管里的反应速率大于右边的,则证明Fe3+对H2O2分解的催化效果比Cu2+的好 |
| C.用图乙装置测定反应速率,可测定反应产生的气体体积及反应时间 |
| D.为检查乙装置的气密性,可关闭a处旋塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位 |
您最近一年使用:0次
2021-10-10更新
|
282次组卷
|
7卷引用:江西省南昌八一中学2021-2022学年高二上学期10月份月考化学试题
名校
8 . 某研究性学习小组欲用下图所示的装置证明酸性:H2SO3>HClO。下列有关说法正确的是
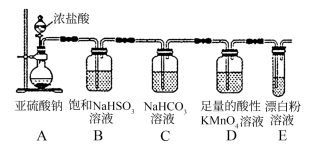

| A.装置E中反应的化学方程式为:H2O+SO2+Ca(ClO)2=CaSO3↓+2HClO |
| B.去掉装置C不影响实验效果 |
| C.反应过程中装置D中溶液的颜色变浅但不褪去 |
| D.通过本实验可得出非金属性:S>Cl |
您最近一年使用:0次
名校
9 . 下列有关装置的说法正确的是
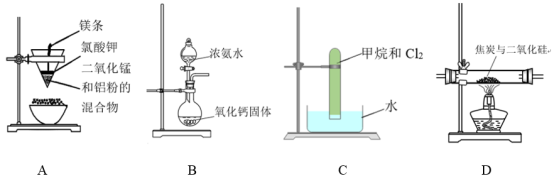

| A.此装置可制得金属锰 |
B.打开分液漏斗活塞后,产生能使湿润的红色石蕊试纸变蓝的气体,证明 的碱性强于 的碱性强于 |
| C.将该装置放在暗处一段时间后,试管内气体颜色变浅,液面上升,能证明甲烷与氯气在暗处能发生取代反应 |
D.检验出有 生成,能证明焦炭与二氧化硅发生了反应 生成,能证明焦炭与二氧化硅发生了反应 |
您最近一年使用:0次
2021-01-03更新
|
397次组卷
|
2卷引用:江西景德镇市浮梁一中2020-2021学年高二下学期4月月考争优部化学试题
名校
10 . 保险粉Na2S2O4大量用于印染业,并用来漂白纸张、纸浆和陶土等。某化学兴趣小组同学用甲酸法制取保险粉的装置如图所示(加持装置略去)。
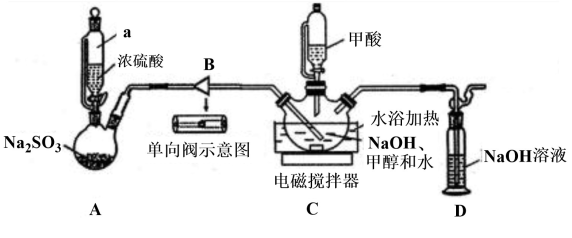
已知:保险粉易溶于水,不溶于甲醇,具有强还原性,在空气中易被氧化:2Na2S2O4+O2+2H2O=NaHSO3或Na2S2O4 +O2+H2O =NaHSO3+NaHSO4。实验时先把甲酸(HCOOH)与溶于甲醇和水混合溶剂的NaOH混合,再通入SO2气体。回答下列问题:
(1)仪器a的名称是______ ;装置B的作用是______ 。
(2)装置C中甲醇不参加反应,甲醇的作用是______ ;生成Na2S2O4的离子方程式为______ 。
(3)下列有关该实验的说法正确的是______ (填序号)。
A.可用硝酸和BaCl2溶液检验制得的Na2S2O4中是否混有NaHSO4
B.实验中甲酸和NaOH最合适的物质的量之比为1:1
C.用N2排尽装置内的空气,有利于提高 的Na2S2O4纯度
D.得到Na2S2O4固体后可用甲醇洗涤
(4)测定产品中Na2S2O4质量分数,其实验步骤如下,准确称取0.5000g产品放入锥形瓶中,加入适量水使其溶解。然后加入足量甲醛,充分反应,再滴加几滴指示剂,用0.2000mol·L-1的标准I2溶液滴定,至终点时,消耗25.00mL标准I2溶液。实验过程中涉及的反应:Na2S2O4+2HCHO+H2O =NaHSO3·HCHO+NaHSO2·HCHO;NaHSO2·HCHO+2I2+2H2O= NaHSO4+HCHO+4HI。该实验加入指示剂是______ ,产品Na2S2O4 (M=174g·mol-1)的质量分数为 ______ % (保留一位小数)。
(5)探究Na2S2O4的性质。隔绝空气加热Na2S2O4固体完全分解是到固体产物Na2SO3,Na2S2O3和SO2,但该兴趣小组没有做到完全隔绝空气,得到的固体产物中还含有Na2SO4。请设计实验证明该分解产物中含有Na2SO4。实验方案是______ 。(可选试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、KMnO4溶液)

已知:保险粉易溶于水,不溶于甲醇,具有强还原性,在空气中易被氧化:2Na2S2O4+O2+2H2O=NaHSO3或Na2S2O4 +O2+H2O =NaHSO3+NaHSO4。实验时先把甲酸(HCOOH)与溶于甲醇和水混合溶剂的NaOH混合,再通入SO2气体。回答下列问题:
(1)仪器a的名称是
(2)装置C中甲醇不参加反应,甲醇的作用是
(3)下列有关该实验的说法正确的是
A.可用硝酸和BaCl2溶液检验制得的Na2S2O4中是否混有NaHSO4
B.实验中甲酸和NaOH最合适的物质的量之比为1:1
C.用N2排尽装置内的空气,有利于提高 的Na2S2O4纯度
D.得到Na2S2O4固体后可用甲醇洗涤
(4)测定产品中Na2S2O4质量分数,其实验步骤如下,准确称取0.5000g产品放入锥形瓶中,加入适量水使其溶解。然后加入足量甲醛,充分反应,再滴加几滴指示剂,用0.2000mol·L-1的标准I2溶液滴定,至终点时,消耗25.00mL标准I2溶液。实验过程中涉及的反应:Na2S2O4+2HCHO+H2O =NaHSO3·HCHO+NaHSO2·HCHO;NaHSO2·HCHO+2I2+2H2O= NaHSO4+HCHO+4HI。该实验加入指示剂是
(5)探究Na2S2O4的性质。隔绝空气加热Na2S2O4固体完全分解是到固体产物Na2SO3,Na2S2O3和SO2,但该兴趣小组没有做到完全隔绝空气,得到的固体产物中还含有Na2SO4。请设计实验证明该分解产物中含有Na2SO4。实验方案是
您最近一年使用:0次
2020-12-21更新
|
1183次组卷
|
6卷引用:江西省南昌市第二中学2021-2022学年高三上学期第一次检测理综化学试题
江西省南昌市第二中学2021-2022学年高三上学期第一次检测理综化学试题(已下线)培优01 无机制备类实验 基础训练-2021年高考化学大题培优练(新高考地区专用)(已下线)解密06 金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密06 金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练辽宁省沈阳市第一二〇中学2021-2022学年高三上学期第四次质量监测化学试题四川省成都市第七中学2021届高三一诊模拟考试理综化学试题



