名校
解题方法
1 . 已知反应:
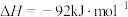 ,温度不同(T2>T1)。下列图像正确的是
,温度不同(T2>T1)。下列图像正确的是

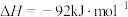 ,温度不同(T2>T1)。下列图像正确的是
,温度不同(T2>T1)。下列图像正确的是A.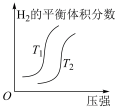 | B.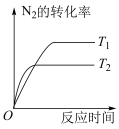 |
C.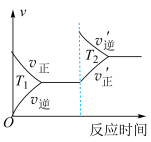 | D.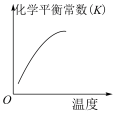 |
您最近一年使用:0次
2023-11-03更新
|
402次组卷
|
19卷引用:河南省新乡市长垣市2022-2023学年高二上学期11月期中考试化学试题
河南省新乡市长垣市2022-2023学年高二上学期11月期中考试化学试题湖南省部分学校2022-2023学年高二上学期期中考试化学试题江西省赣州市十六县(市)二十校2022-2023学年高二上学期期中联考化学试题广西贵港市桂平市浔州高级中学2022-2023学年高二上学期期中考试化学试题河北省邢台市南和区第一中学2022-2023学年高二上学期期中考试化学试题江西省赣州市重点中学六校2022-2023学年高二上学期期中联考化学试题河北省部分学校2022-2023学年高二上学期期中考试化学试题湖北省部分学校2022-2023学年高二上学期期中考试化学试题辽宁省抚顺市六校协作体2022-2023学年高二上学期期中考试化学试题河北省保定市唐县第一中学2022-2023学年高二上学期11月期中考试化学试题河南省获嘉县第一中学2023-2024学年高二上学期第一次月考化学试卷(已下线)第06讲 化学反应速率与化学平衡的图像-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)云南省昆明市云南师范大学附属中学2023-2024学年高二上学期期中联考化学试题宁夏回族自治区石嘴山市第三中学2023-2024学年高二9月月考化学试题浙江省嘉兴八校2023-2024学年高二上学期11月期中联考化学试题宁夏六盘山高级中学2023-2024学年高二上学期第二次月考化学试题云南省宣威市第六中学2023-2024学年高二上学期12月月考化学试题河南省郑州学森实验学校2023-2024学年高二上学期1月月考 化学试题安徽省马鞍山市第二中学2023-2024学年高二上学期期末检测化学试题
名校
解题方法
2 . 将0.42g 和0.53g
和0.53g 混合并配成溶液,向该溶液中滴加0.05
混合并配成溶液,向该溶液中滴加0.05 的稀盐酸。下列图像能正确表示加入盐酸的体积和生成
的稀盐酸。下列图像能正确表示加入盐酸的体积和生成 的质量的关系的是
的质量的关系的是
 和0.53g
和0.53g 混合并配成溶液,向该溶液中滴加0.05
混合并配成溶液,向该溶液中滴加0.05 的稀盐酸。下列图像能正确表示加入盐酸的体积和生成
的稀盐酸。下列图像能正确表示加入盐酸的体积和生成 的质量的关系的是
的质量的关系的是A. | B. |
C. | D. |
您最近一年使用:0次
3 . 已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CH3COOH⇌CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是
| A.加少量烧碱固体 | B.升高温度 |
| C.加少量冰醋酸 | D.加CH3COONa固体 |
您最近一年使用:0次
2023-09-08更新
|
771次组卷
|
15卷引用:河南省宏力学校2021-2022学年高二上学期期末考试化学试题
河南省宏力学校2021-2022学年高二上学期期末考试化学试题湖南省邵阳邵东市第四中学2022-2023学年高二上学期期中考试化学试题新疆和田地区第二中学2022-2023学年高二上学期11月期中考试化学试题【全国百强校】甘肃省静宁县第一中学2018-2019学年高二上学期10月月考化学试题(已下线)【南昌新东方】江西省九江一中2016-2017学年高二上学期期末化学试卷辽宁省沈阳市第八十三中学2021-2022学年高二上学期期初考试化学试题山西省运城市2021~2022学年高二上学期10月份月考化学试卷山西省晋中市平遥县第二中学2021-2022学年高二上学期12月考试化学试题黑龙江省饶河县高级中学2021-2022学年高二上学期期中考试化学试题山西省大同市第一中学校2023-2024学年高二上学期10月月考化学试题广西南宁市广西大学附属中学2023-2024学年高二上学期期中考试化学试题四川省绵阳南山中学实验学校2023-2024学年高二上学期10月月考化学试题(已下线)寒假作业05 电离平衡及溶液的酸碱性-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)广西桂林市第十一中学2023-2024学年高二上学期11月期中化学试题河南省郑州学森实验学校2023-2024学年高二上学期1月月考 化学试题
4 . 已知:Ksp(AgCl)=1.8×10-10 ,Ksp(AgI)=1.5×10-16,Ksp(Ag2CrO4)=2.0×10-12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是
| A.AgCl>AgI>Ag2CrO4 | B.AgCl>Ag2CrO4>AgI |
| C.Ag2CrO4>AgCl>AgI | D.Ag2CrO4>AgI>AgCl |
您最近一年使用:0次
2023-08-14更新
|
1016次组卷
|
55卷引用:河南省新乡市第一中学2022-2023学年高二上学期第一次月考化学试题
河南省新乡市第一中学2022-2023学年高二上学期第一次月考化学试题黑龙江省大庆中学2021-2022学年高二上学期期末考试化学试题(已下线)第33练 沉淀溶解平衡-2023年高考化学一轮复习小题多维练(全国通用)湖南省长沙市宁乡市四校联考2022-2023学年高二上学期11月月考化学试题2010年普通高等学校招生全国统一考试化学试题(海南卷)2010年高考化学试题分项专题十 电解质溶液(已下线)2010年北京五中高二下学期期末考试化学试题(已下线)2010—2011学年山西省大同一中高二上学期期末考试化学试卷(已下线)2011-2012学年湖北省襄阳市四校高二上学期期中考试化学试卷(已下线)2011-2012学年江西省九江一中高二上学期第二次月考化学试卷(已下线)2011-2012学年江苏省南京三中高二下学期期末考试化学选修试卷(已下线)2011-2012学年河北省元氏一中高二上学期期中考试化学试卷(已下线)2012-2013学年山东省济宁市泗水一中高二12月质量检测化学试卷(已下线)2012-2013学年福建省南安一中高二上学期期末考试化学试卷(已下线)2013-2014学年湖北省恩施高中高二12月月考化学试卷2014-2015湖南省怀化市中小学课改高二上学期期末化学试卷2014-2015河北省隆化县存瑞中学高二下学期期中考试化学试卷2015-2016学年湖南省衡阳县高二上学期期末统考化学试卷2015-2016学年湖北省武汉三十九中高二上学期期末化学试卷2015-2016学年青海师大附属二中高二下4月月考化学试卷2015-2016学年福建师大附中高二下期中化学试卷2017届湖北省枣阳市高级中学高三上学期8月月考化学试卷2017届内蒙古赤峰二中高三上第二次月考化学试卷广西陆川县中学2017-2018学年高二上学期期中考试化学试题河北省衡水市安平中学2017-2018学年高二上学期期中考试化学试题高中化学人教版 选修四 第三章 水溶液中的离子反应 第四节 难溶电解质的溶解平衡 难溶电解质的溶解平衡内蒙古包头市第四中学2017-2018学年高二上学期期末考试化学试题(已下线)2018年11月15日 《每日一题》人教选修4-溶度积的应用【全国百强校】贵州省铜仁市第一中学2018-2019学年高二下学期开学考试化学试题步步为赢 高二化学暑假作业:作业十 水溶液中的离子平衡陕西省吴起高级中学2019-2020学年高二上学期期中考试化学(基础卷)试题(已下线)2019年11月13日 《每日一题》人教版(选修4)——溶度积的有关计算黑龙江省哈尔滨市第三中学2019-2020学年高二上学期期中考试化学(理)试题陕西省咸阳市西藏民族大学附属中学2019-2020学年高二上学期第二次月考化学试题2019年秋高三化学复习强化练习—— 与浓度积的相关计算(强化练)湖南省雅礼中学2019-2020学年高二上学期第一次月考化学试题吉林省通化市梅河口市博文学校2019-2020学年高二上学期第二次月考化学试题(已下线)山东省邹城市2018-2019学年高二上学期12月月考化学试卷湖北省恩施州清江外国语学校2020-2021学年高二上学期10月月考化学试题河北省石家庄市辛集市第一中学2019-2020学年高二第二次考试(二)化学试题鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡湖南省长郡中学2020-2021学年高二上学期期中考试化学试题(已下线)练习14 难溶电解质的沉淀溶解平衡-2020-2021学年【补习教材·寒假作业】高二化学(苏教版)贵州省蟠龙高级中学2020-2021学年高二上学期第二次月考化学试题云南省楚雄天人中学2021-2022学年高二上学期12月月考化学试题(B卷)湖北省罗田县第一中学2021-2022学年高二上学期12月月考化学试题山西省太原市英才学校2021-2022学年高二上学期第二次月考化学试题山东省潍坊第一中学2022-2023学年高二上学期期末考试化学试题(已下线)考点巩固卷09 水溶液中的离子反应与平衡(4大考点62题)-2024年高考化学一轮复习考点通关卷(新高考通用)第1课时 沉淀溶解平衡与溶度积作业(二十一) 沉淀溶解平衡与溶度积天津市第一中学2023-2024学年高二上学期期末考试化学试卷山东师大附中幸福柳分校2023-2024学年高二上学期12月份化学学科阶段性测试(已下线)湖南省郴州市临武县第一中学2023-2024学年高三下学期5月期中化学试题
名校
5 . 铁及其化合物在生产生活中有极其重要的用途,请回答下列问题:
I. 是一种重要的含铁盐。
是一种重要的含铁盐。
(1)将饱和 溶液滴入沸水中可制得
溶液滴入沸水中可制得 胶体,其实验装置如图所示。
胶体,其实验装置如图所示。 胶体具有良好的净水效果,胶体中分散质微粒大小范围为
胶体具有良好的净水效果,胶体中分散质微粒大小范围为_______ ,鉴别氯化铁溶液和氢氧化铁胶体,除了可通过观察颜色以外,还可采取的方法是_______ 。

(2)在现代半导体工业生产中,常利用 腐蚀铜的原理制作印刷线路板,该原理的离子方程式为
腐蚀铜的原理制作印刷线路板,该原理的离子方程式为_______ 。
(3)向氯化铁溶液中同时加入铁粉和铜粉,反应结束后烧杯底部不可能出现的是_______(填标号)。
Ⅱ.硫酸亚铁可用于制造铁氧体、净水剂等,医学上可用作补铁剂。
(4)实验室在配制 溶液时,为了防止
溶液时,为了防止 溶液变质,经常会向其中加入一些铁粉,其原因是
溶液变质,经常会向其中加入一些铁粉,其原因是_______ (用离子方程式表示)。
(5) 可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将
可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将 转化为
转化为 ,以利于人体吸收。为了验证这一猜想,设计了如下实验:
,以利于人体吸收。为了验证这一猜想,设计了如下实验:
由上述实验能否得出“维生素C可将 转化为
转化为 ”的结论?请说明理由:
”的结论?请说明理由:_______ 。
(6)锶铁氧体是由锶和铁的氧化物组成的复合磁性材料,某种锶铁氧体可表示为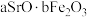 ,其中
,其中 和
和 的质量比为0.13,则
的质量比为0.13,则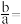
_______ 。(取整数)。
I.
 是一种重要的含铁盐。
是一种重要的含铁盐。(1)将饱和
 溶液滴入沸水中可制得
溶液滴入沸水中可制得 胶体,其实验装置如图所示。
胶体,其实验装置如图所示。 胶体具有良好的净水效果,胶体中分散质微粒大小范围为
胶体具有良好的净水效果,胶体中分散质微粒大小范围为
(2)在现代半导体工业生产中,常利用
 腐蚀铜的原理制作印刷线路板,该原理的离子方程式为
腐蚀铜的原理制作印刷线路板,该原理的离子方程式为(3)向氯化铁溶液中同时加入铁粉和铜粉,反应结束后烧杯底部不可能出现的是_______(填标号)。
| A.有铁无铜 | B.有铜无铁 | C.有铁有铜 | D.无铁无铜 |
Ⅱ.硫酸亚铁可用于制造铁氧体、净水剂等,医学上可用作补铁剂。
(4)实验室在配制
 溶液时,为了防止
溶液时,为了防止 溶液变质,经常会向其中加入一些铁粉,其原因是
溶液变质,经常会向其中加入一些铁粉,其原因是(5)
 可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将
可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将 转化为
转化为 ,以利于人体吸收。为了验证这一猜想,设计了如下实验:
,以利于人体吸收。为了验证这一猜想,设计了如下实验:| 实验方案 | 实验现象 |
取适量 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液 | 紫色褪去 |
 转化为
转化为 ”的结论?请说明理由:
”的结论?请说明理由:(6)锶铁氧体是由锶和铁的氧化物组成的复合磁性材料,某种锶铁氧体可表示为
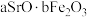 ,其中
,其中 和
和 的质量比为0.13,则
的质量比为0.13,则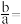
您最近一年使用:0次
2023-07-30更新
|
139次组卷
|
2卷引用:河南省新乡市2022-2023学年高一上学期选科调研第二次测试化学试题
名校
6 . 分类法是学习和研究化学物质的一种常用科学方法。下列“链状连环”图案中,相连的两种物质在一定条件下可以发生反应,相交部分X、Y、Z、W、M为其反应类型。请回答下列问题:

(1)关于上述反应类型,属于氧化还原反应的是_______ (填字母)。
(2)④在水中的电离方程式为_______ ,⑤与⑥在水中发生反应的离子方程式为_______ 。
(3)②与③发生反应的化学方程式为_______ ,每消耗
 ,反应中生成的
,反应中生成的 分子数为
分子数为_______ 。
(4) 固体中含有少量⑥,可通过加热的方法除去⑥,发生反应的化学方程式为
固体中含有少量⑥,可通过加热的方法除去⑥,发生反应的化学方程式为_______ 。
(5)将微粒直径为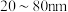 的①均匀分散在水中,下列关于该分散系的说法正确的是
的①均匀分散在水中,下列关于该分散系的说法正确的是_______ (填标号)。
A.该分散系是胶体
B.可用丁达尔效应区分该分散系与 胶体
胶体
C.该分散系区别于其他分散系的本质特征是分散质微粒直径大小的不同

(1)关于上述反应类型,属于氧化还原反应的是
(2)④在水中的电离方程式为
(3)②与③发生反应的化学方程式为

 ,反应中生成的
,反应中生成的 分子数为
分子数为(4)
 固体中含有少量⑥,可通过加热的方法除去⑥,发生反应的化学方程式为
固体中含有少量⑥,可通过加热的方法除去⑥,发生反应的化学方程式为(5)将微粒直径为
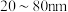 的①均匀分散在水中,下列关于该分散系的说法正确的是
的①均匀分散在水中,下列关于该分散系的说法正确的是A.该分散系是胶体
B.可用丁达尔效应区分该分散系与
 胶体
胶体C.该分散系区别于其他分散系的本质特征是分散质微粒直径大小的不同
您最近一年使用:0次
2023-07-30更新
|
91次组卷
|
2卷引用:河南省新乡市2022-2023学年高一上学期选科调研第二次测试化学试题
名校
7 . 微粒观的形成对化学学习具有重要的意义。下列离子方程式书写正确的是
A.铁与足量稀盐酸反应: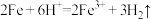 |
B.向硝酸银溶液中投入一小块钠: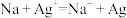 |
C.向澄清石灰水中滴加少量 溶液: 溶液: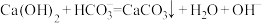 |
D.向氢氧化钡溶液中滴加少量 溶液: 溶液: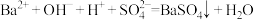 |
您最近一年使用:0次
2023-07-30更新
|
170次组卷
|
2卷引用:河南省新乡市2022-2023学年高一上学期选科调研第二次测试化学试题
名校
8 . 在下列物质中,属于电解质的是
| A.蔗糖 | B. 固体 固体 | C.石墨 | D.盐酸 |
您最近一年使用:0次
2023-07-30更新
|
181次组卷
|
2卷引用:河南省新乡市2022-2023学年高一上学期选科调研第二次测试化学试题
9 . 下列非物质文化遗产的主要制作过程中没有涉及氧化还原反应的是
 |  |  |  |
| A.痘姆古陶 | B.徽州木雕 | C.千年古井贡酒 | D.符离集烧鸡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-07-30更新
|
85次组卷
|
2卷引用:河南省新乡市2022-2023学年高一上学期选科调研第二次测试化学试题
10 . 丙烯是三大合成材料的基本原料之一,其中生产聚丙烯时丙烯用量最大。另外,丙烯还可用于生产多种重要有机化工原料。由丙烷(C3H8)制丙烯(C3H6)的两种方法如下:
I.丙烷催化脱氢法: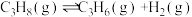 ΔH1
ΔH1
II.丙烷催化氧化法: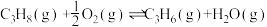 ΔH2=-118kJ·mol-1
ΔH2=-118kJ·mol-1
请回答下列问题:
(1)已知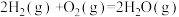 ΔH=-484kJ·mol-1,由此计算ΔH1=
ΔH=-484kJ·mol-1,由此计算ΔH1=_________ kJ·mol-1。
(2)T℃下,向2L恒容密闭容器中充入0.8molC3H8(g),加入催化剂发生催化脱氢反应。体系内压强变化如表所示。
①下列能说明该反应达到平衡状态的是___________ (填标号)。
a.丙烷的消耗速率等于丙烯的生成速率
b.容器内气体的密度不再发生变化
c.容器内的压强不再发生变化
d.容器内气体平均相对分子质量不再变化
②0~3min内,用H2(g)表示该反应的反应速率为___________ mol·L-1·min-1。
③C3H8(g)的平衡转化率为___________ ,该反应的平衡常数Kp=___________ kPa(Kp为以分压表示的平衡了常数,分压=总压×物质的量分数,保留2位小数)。
(3)在催化剂的作用下,丙烷催化氧化除生成丙烯外,还生成碳的氧化物等物质。相同时间内丙烷转化率和丙烯产率随温度变化关系如图所示。

①T1℃前,丙烷的转化率随温度升高而上升的可能原因有___________ 。
②T1~T2℃,丙烷转化率提高,而丙烯产率大幅降低的主要原因是___________ 。
I.丙烷催化脱氢法:
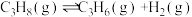 ΔH1
ΔH1II.丙烷催化氧化法:
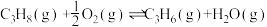 ΔH2=-118kJ·mol-1
ΔH2=-118kJ·mol-1请回答下列问题:
(1)已知
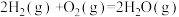 ΔH=-484kJ·mol-1,由此计算ΔH1=
ΔH=-484kJ·mol-1,由此计算ΔH1=(2)T℃下,向2L恒容密闭容器中充入0.8molC3H8(g),加入催化剂发生催化脱氢反应。体系内压强变化如表所示。
| 时间/min | 0 | 1 | 3 | 5 | 7 |
| 压强/kPa | 10p0 | 11.5p0 | 13p0 | 14p0 | 14p0 |
a.丙烷的消耗速率等于丙烯的生成速率
b.容器内气体的密度不再发生变化
c.容器内的压强不再发生变化
d.容器内气体平均相对分子质量不再变化
②0~3min内,用H2(g)表示该反应的反应速率为
③C3H8(g)的平衡转化率为
(3)在催化剂的作用下,丙烷催化氧化除生成丙烯外,还生成碳的氧化物等物质。相同时间内丙烷转化率和丙烯产率随温度变化关系如图所示。

①T1℃前,丙烷的转化率随温度升高而上升的可能原因有
②T1~T2℃,丙烷转化率提高,而丙烯产率大幅降低的主要原因是
您最近一年使用:0次



