1 . 下列图示变化为吸热反应的是
A.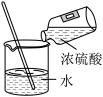 | B.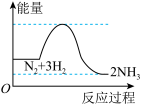 |
C.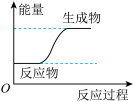 | D.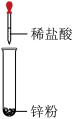 |
您最近一年使用:0次
2023-12-27更新
|
290次组卷
|
173卷引用:河南省鹤壁市高中2022-2023学年高二上学期10月居家测试化学试题
河南省鹤壁市高中2022-2023学年高二上学期10月居家测试化学试题安徽省蚌埠第三中学2021-2022学年高二下学期开学测试化学试题湖南省邵阳邵东市第一中学2021-2022学年高一下学期第一次月考(学考班)化学试题湖南省长沙市湖南师范大学附属中学2021-2022高一下学期期中考试化学试题黑龙江省哈尔滨市第三十二中学校2021-2022学年高一下学期期中考试化学试题广东省广州市第六中学2021-2022学年高一下学期综合考试化学试题辽宁省营口市第二高级中学2021-2022学年高一6月月考化学试题新疆和田地区皮山县高级中学2021-2022学年高一下学期期中考试化学试题广东省揭阳华侨高级中学2021-2022学年高一下学期第一次阶段化学试题陕西省铜川市第一中学2021-2022学年高一下学期期中考试化学试题浙江省温州市苍南县金乡卫城中学2021-2022学年高一下学期第一次月考化学试题广东省茂名市电白区水东中学2021-2022学年高一下学期3月测试化学试题安徽省名校联盟2022-2023学年高二上学期阶段测试(一)化学试题新疆乌鲁木齐市第三十一中学2021-2022学年高一下学期期中考试化学试题海南省海口嘉勋高级中学2021-2022学年高二下学期(2月)检测化学试题江苏省句容高级中学2022-2023学年高二上学期学业水平合格性考试调研(一)化学试题河南省安阳市第二中学2021-2022学年高一下学期第一次段考化学试题四川省资阳中学2022-2023学年高二上学期期末考试化学试题安徽省合肥市肥西县2022-2023学年高二上学期10月月考化学试题(已下线)2012-2013学年北京市房山区房山中学高一下学期期中考试化学试卷2014-2015辽宁师大附中高一下学期第一次月考化学试卷2014-2015广西桂林市第十八中学高一下学期期中考试化学试卷2014-2015学年北京市房山区周口店中学高一下期中考试化学试卷2015-2016学年江西省南昌二中高二上第一次月考化学试卷2015-2016学年河北省邢台一中高一下第一次月考化学试卷2015-2016学年湖南师大附中高一下第一次阶段测化学试卷2015-2016学年江苏省淮阴中学高一下4月阶段测化学试卷2015-2016学年贵州省习水一中高一下学期期中考试化学试卷2015-2016学年江西省临川二中高一下期中化学试卷2015-2016学年广东省普宁一中高一下学期第二次月考化学试卷2015-2016学年山西省康杰中学高一下期中化学试卷2015-2016学年湖南东部六校高一下期中化学试卷2015-2016学年青海师大附二中高一下期中化学试卷2015-2016学年贵州凯里一中高一下期中理科化学试卷2015-2016学年江西省乐安一中高一下学期期中考试化学试卷2015-2016学年陕西省西安七十中高一5月月考化学试卷2015-2016学年湖南师大附中高一下第一次段考化学试卷2015-2016学年广东省肇庆市高一下学期期末化学试卷2015-2016学年新疆农业大学附中高一下学期期中化学试卷2015-2016学年黑龙江省伊春二中高一下期末化学试卷12015-2016学年黑龙江省伊春二中高一下期末化学试卷22017届广西桂林市第十八中学高三上第二次月考化学试卷2016-2017学年贵州铜仁市一中高二上期中考试化学试卷2016-2017学年江西省宜春中学高一3月月考化学试卷2016-2017学年河北省张家口市第一中学高一(衔接班)3月月考(文)化学试卷2016-2017学年湖南省衡阳市第八中学高一下学期理科实验班第一次月考理科综合化学试卷2016-2017学年广西桂林第18中学高一下学期期中模拟化学试卷安徽省淮北市第一中学2016-2017学年高一下学期期中考试化学试题1山西省晋中市名校2016-2017学年高一下学期期中考试化学试题河北省衡水中学2016-2017学年高一下学期期中考试化学试题贵州省遵义航天高级中学2016-2017学年高一下学期期中考试理科综合化学试题江苏省南菁高级中学2016-2017学年高一下学期期中考试化学试题2吉林省吉林油田实验中学2016-2017学年高一下学期期中考试化学试题辽宁省庄河市高级中学2016-2017学年高一下学期期中考试化学试题四川省成都市盐道街中学2016~2017学年高一下学期五月月考化学试题四川省广安市2016-2017学年高一下学期期末考试化学试题四川省广安市2016-2017学年高一上学期期末化学试题江苏省兴化市第一中学2016-2017学年高一下学期期末考试化学试题山西省怀仁县第一中学(两校区)2016-2017学年高一下学期期末考试化学试题陕西省咸阳市武功县普集高中2017-2018学年高二上学期第二次月考(9月)化学试题吉林省汪清县第六中学2018届高三9月月考化学试题湖南省茶陵县第三中学2017-2018学年高一上学期第二次月考化学试题人教版高二化学选修四专题:化学反应与能量变化同步练习题河北省蠡县中学2018-2019学年高二上学期第一次(8月)月考化学试题河北省保定市蠡县中学2018-2019学年高二上学期9月月考化学试题浙江省杭州市西湖高级中学2017-2018学年高二12月月考化学试题高二人教版选修4 第一章 章末基础排查(一)甘肃省武威第五中学2018-2019学年高一下学期5月月考化学试题广东省江门市第二中学2018-2019学年高一5月月考化学试题黑龙江省齐齐哈尔市第八中学2018-2019学年高一下学期期中考试化学试题新疆沙雅县第二中学2018-2019学年高一下学期期末考试化学试题黑龙江省大庆十中2018-2019学年高一下学期期末考试化学试题福建省长乐高级中学2018-2019学年高二下学期期末考试化学试题(已下线)2019年8月20日《每日一题》选修4—— 吸热反应与放热反应的判断广东省阳春市第一中学2019-2020学年高二上学期月考一化学试题河北省邢台市第八中学2019-2020学年高二上学期第一次月考化学试题黑龙江省双鸭山市第一中学2019-2020学年高二上学期第一次月考化学试题陕西省榆林市第二中学2019-2020学年高二上学期期中考试化学试题河北省张家口市第一中学2019-2020学年高二上学期期中考试化学试题山东省枣庄市第八中学2019-2020学年高二上学期期中考试化学试题安徽省天长市炳辉中学2019-2020学年高二上学期第二次月考化学试题福建省莆田第七中学2019-2020学年高二上学期期中考试化学试题2020届高三化学选修4二轮专题练——中和热及其测定【选择精编25题】山西省大同市天镇一中2019-2020学年高二上学期期中考试化学试题2020届高三化学知识点强化训练—化学反应中能量变化陕西省渭南市韩城市象山中学2019-2020学年高一下学期第一次月考化学试题天津市第二南开学校2019-2020学年高一下学期阶段性检测化学试题第二章 化学反应与能量学 易错疑难集训(一)——A学习区 夯实基础(人教版必修2)第一节 化学反应与能量变化 易错疑难集训(一)——A学习区 夯实基础(人教版(2019)第二册)广东省郁南县连滩中学2019-2020学年高一下学期期中考试化学试题河北省邯郸市磁县第二中学2019-2020学年高一下学期期中考试化学试卷黑龙江省鸡西市鸡东县第二中学2019-2020学年高一下学期线上考试化学试题新疆昌吉市教育共同体2019-2020学年高一下学期期中考试化学试题甘肃省张掖市第二中学2019-2020学年高一4月开学测试化学试题广东省揭阳市第三中学2019-2020学年高一下学期第一次阶段考试化学试题湖南省郴州市2019-2020学年高一4月线上考试化学试题贵州省毕节市实验高级中学2019-2020学年高一下学期期中考试化学试题甘肃省靖远县第四中学2019-2020学年高一下学期期中考试化学(普通班)试题甘肃省靖远县第四中学2019-2020学年高一下学期期中考试化学(实验班)试题辽宁省阜新市第二高级中学2019-2020学年高一下学期第一次学考化学试题贵州省思南中学2019-2020学年高一下学期期中考试化学试题山东省济宁市实验中学2019-2020学年高一6月月考化学试题四川省内江市威远中学2019-2020学年高一下学期第二次月考化学试题(已下线)第10练 燃烧热 热源-2020年【衔接教材·暑假作业】新高二化学(人教版)广东省第二师范学院番禺附属中学2019-2020学年高一下学期期中段考化学试题安徽省安庆市第一中学2019-2020学年高一下学期月考化学试题湖北省黄冈市黄梅国际育才高级中学2019-2020学年高一下学期期中考试化学试题广东省汕头市金山中学2019-2020学年高一下学期6月月考化学试题江苏省启东市2019-2020学年高一下学期期末调研测试化学试题吉林省普通高中友好学校联合体第三十届基础年段2019-2020学年高一下学期期末联考化学试题(已下线)1.1.1焓变 反应热(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)第一章 化学反应与能量(基础过关)-2020-2021学年高二化学单元测试定心卷(人教版选修4)(已下线)第01章 化学反应的热效应(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)(已下线)1.1.1+焓变+反应热-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)河南省三门峡市第一高级中学2020-2021学年高二上学期9月月考化学试题陕西省西安中学2018-2019学年高一下学期期末考试化学题必修第二册RJ第6章易错疑难集训(一)人教版(2019)高二选择性必修第一册 第一章 化学反应的热效应 章末综合检测卷河南省安阳市第一中学2020-2021学年高二上学期第一次阶段考试化学试题吉林省大安市第六中学2020-2021学年高二上学期期中考试化学试题福建省莆田第十五中学2018-2019学年高二上学期期末考试化学试题高中化学苏教2019版必修第二册-专题6 第二单元 第1课时 放热反应与吸热反应浙江省湖州市德清县第三中学2020-2021学年高二下学期返校考试化学试题江苏省盐城市伍佑中学2020-2021学年高一下学期第一次阶段考试化学试题广西钦州市浦北县浦北中学2020-2021学年高一3月月考化学试题黑龙江省牡丹江市海林市朝鲜族中学2020-2021学年高一4月月考化学试题云南省楚雄天人中学2019-2020学年高一下学期5月月考化学试题辽宁省盘锦市第二高级中学2020-2021学年高一下学期第一次阶段考试化学试题浙江省宁波市咸祥中学2020-2021学年高一下学期期中考试化学试题宁夏银川市贺兰县景博中学2020-2021学年高一下学期期中考试化学试题山东省济宁市兖州区2020-2021学年高一下学期期中考试化学试题甘肃省白银市靖远县第四中学2020-2021学年高一下学期期中考试化学(理)试题四川省成都市蒲江县蒲江中学2020-2021学年高二上学期10月月考化学试题河南省许昌市2020-2021学年高一下学期期末质量检测化学试题安徽省六安市舒城县2020-2021学年高一下学期期末考试化学试题安徽省安庆市2020-2021学年高一下学期期末考试化学试题黑龙江省鹤岗市第一中学2020-2021学年高一下学期期末考试化学试题黑龙江省牡丹江市第十五中学2020-2021学年高一下学期期中考试化学(文)试题河北省张家口市第一中学2021-2022学年高二上学期开学检测化学试题浙江省金华市磐安县第二中学2019-2020学年高一下学期期中考试化学试题吉林省敦化市实验中学2020-2021学年高一下学期期末考试化学试题吉林省长春市九台区第四中学2021-2022学年高二上学期9月月考化学试卷题福建省泉州现代中学2021-2022学年高二上学期9月月考化学试题江苏省盐城市实验高级中学(新洋高级中学)2020-2021学年高二下学期期中考试化学试题辽宁省朝阳市建平县实验中学2021-2022学年高二上学期期中考试化学试题吉林省汪清县第六中学2021-2022学年高二上学期期中考试化学试题河北省邯郸市魏县第五中学2021-2022学年高二上学期期中考试化学试题四川省广安代市中学校2020-2021学年高二下学期第二次月考化学试卷黑龙江省哈尔滨市延寿县第二中学2021-2022学年高二上学期期中考试化学试题青海省西宁市海湖中学2021-2022学年高二上学期期中考试化学试题江西省上饶市2019-2020学年高二下学期期末教学质量测试化学试题江西省上饶市2019-2020学年高一下学期期末教学质量测试化学试题江西省赣州市南康区第三中学2022-2023学年高一下学期期中考试化学试题浙江省台州市八校联盟2022-2023学年高一下学期期中联考化学试题宁夏青铜峡市宁朔中学2022-2023学年高一下学期期中考试化学试题广东省华南师范大学附属中学2022-2023学年高二上学期1月期末化学试题甘肃省兰州第一中学2023-2024学年高二上学期10月月考化学试题广东省广州市六校联考2023-2024学年高二上学期11月期中化学试题广东省东莞中学2023-2024学年高二上学期10月第一次月考化学试题辽宁省辽西联合校2023-2024学年高二上学期期中考试化学试题陕西省咸阳市兴平市西郊高级中学2023-2024学年高二上学期期中考试化学试题四川省自贡市第一中学校2023-2024学年高二上学期10月月考化学试题广东省化州市第一中学2023-2024学年高二上学期12月质量检测化学试卷 (已下线)寒假收官卷01-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)吉林省辽源市田家炳高中友好学校七十六届期末联考2023-2024学年高二上学期1月期末化学试题云南省昭通市盐津县第二中学2023-2024学年高二上学期期末考试化学试题江西省丰城市东煌学校2022-2023学年高一下学期6月期末考试化学试题海南省海口市秀英区某校2023-2024学年高二上学期期中检测化学试题(已下线)6.1.1 化学反应与热能北京市大兴一中2023-2024学年高一下学期3月月考化学试题福建省永春第一中学2023-2024学年高一下学期4月月考化学试题宁夏开元学校2023-2024学年高二学年下学期开学收心测试化学试题北京市八一学校2023-2024学年高一下学期期中测试化学试题
2 . 肼(N2H4)又称联氨,为二元弱碱,在水中的电离与氨类似。已知常温下,N2H4第一步电离平衡N2H4+H2O
 +OH-,Kb1=8.7×10-7。下列说法错误的是
+OH-,Kb1=8.7×10-7。下列说法错误的是

 +OH-,Kb1=8.7×10-7。下列说法错误的是
+OH-,Kb1=8.7×10-7。下列说法错误的是A.N2H4的水溶液中存在:c( )+2c( )+2c(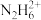 )+c(H+)=c(OH-) )+c(H+)=c(OH-) |
B.反应 N2H4+H+  的平衡常数K=8.7×107 的平衡常数K=8.7×107 |
| C.联氨与硫酸形成酸式盐的化学式为N2H5HSO4 |
D.向N2H4的水溶液中加水,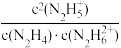 不变 不变 |
您最近一年使用:0次
2023-08-26更新
|
605次组卷
|
7卷引用:河南省鹤壁市高中2022-2023学年高二上学期10月居家测试化学(宏奥班)试题
名校
解题方法
3 . 下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是
选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
A | 纯碱可用于治疗胃溃疡 | 纯碱可与盐酸反应 | Ⅰ对,Ⅱ对,有 |
B |  中的少量HCl杂质可将气体通入饱和 中的少量HCl杂质可将气体通入饱和 溶液除去 溶液除去 |  可与HCl反应 可与HCl反应 | Ⅰ对,Ⅱ错,无 |
C |  溶液中混有少量 溶液中混有少量 杂质,可加入适量NaOH除去 杂质,可加入适量NaOH除去 |  可与NaOH反应生成 可与NaOH反应生成 | Ⅰ对,Ⅱ对,有 |
D |  是淡黄色粉末 是淡黄色粉末 |  做供氧剂 做供氧剂 | Ⅰ对,Ⅱ对,有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-08更新
|
329次组卷
|
11卷引用:河南省鹤壁市浚县第一中学2022-2023学年高一上学期10月考试化学试题
河南省鹤壁市浚县第一中学2022-2023学年高一上学期10月考试化学试题期中学业水平测试第一节 钠及其化合物 第2课时 钠的化合物 焰色试验河南省南阳市第一中学校2022-2023学年高一上学期12月月考化学试题黑龙江省勃利县高级中学2022-2023学年高一上学期11月期中考试化学试题河北省石家庄市第十八中学2021-2022学年高一上学期期中考试化学试题安徽省肥东凯悦中学2021-2022学年高一上学期第三次自主检测化学试题广东省茂名化州市第一中学2021-2022学年高一上学期第二次月考化学试题辽宁省大连市金州高级中学2023-2024学年高一上学期10月月考化学试题辽宁省朝阳市名校联考2023-2024学年高一上学期期中考试化学试题 广东省广州市广外、铁一、广大附中等三校2023~2024学年高一上学期期中联考化学试题
解题方法
4 . 聚苯醚(PPO)是一种性能优异的热塑性工程塑料,其一种合成路线如图:
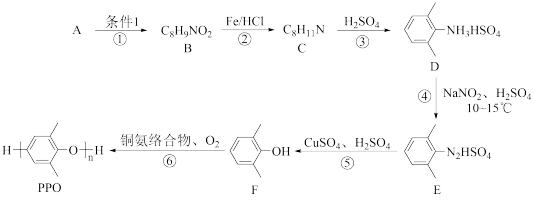
已知:R-NO2 R-NH2
R-NH2
回答下列问题:
(1)苯的同系物A中碳的质量分数为90.6%,A的名称为_______ 。
(2)条件1为_______ ,C中官能团名称为 _______ 。
(3)反应⑤的反应类型为_______ 。
(4)写出反应⑥的化学方程式:_______ 。
(5)对合成产物PPO进行核磁共振氢谱分析,如图在PPO结构简式上用*标出谱图上吸收峰c所表示的氢原子:_______ 。
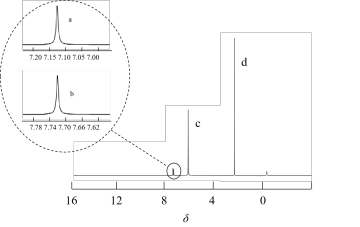
(6)F有多种同分异构体,其中能使FeCl3溶液发生显色反应的有_______ 种(不包括F本身)。写出苯环上一氯代物只有两种结构的结构简式:_______ (任写一种)

已知:R-NO2
 R-NH2
R-NH2回答下列问题:
(1)苯的同系物A中碳的质量分数为90.6%,A的名称为
(2)条件1为
(3)反应⑤的反应类型为
(4)写出反应⑥的化学方程式:
(5)对合成产物PPO进行核磁共振氢谱分析,如图在PPO结构简式上用*标出谱图上吸收峰c所表示的氢原子:

(6)F有多种同分异构体,其中能使FeCl3溶液发生显色反应的有
您最近一年使用:0次
5 . 硫代硫酸钠晶体(Na2S2O3•5H2O,Na2S2O3为弱酸盐)是重要的化工原料,已知它易溶于水,难溶于乙醇,在中性和碱性环境中稳定,在40~45℃熔化,48℃分解。某兴趣小组用两种方法制取硫代硫酸钠晶体并加以应用
I.制备Na2S2O3•5H2O
方法一:亚硫酸钠法。
反应原理:S+ =Na2S2O3
=Na2S2O3
实验步骤:称取一定量的 于烧杯中,溶于水。另取过量的硫粉,加入少量乙醇充分搅拌均匀后,加到上述溶液中。水浴加热,微沸,反应后趁热过滤。滤液蒸发浓缩、冷却结晶后析出Na2S2O3•5H2O晶体。再进行减压过滤、洗涤并低温干燥。
于烧杯中,溶于水。另取过量的硫粉,加入少量乙醇充分搅拌均匀后,加到上述溶液中。水浴加热,微沸,反应后趁热过滤。滤液蒸发浓缩、冷却结晶后析出Na2S2O3•5H2O晶体。再进行减压过滤、洗涤并低温干燥。
(1)向硫粉中加入少量乙醇充分搅拌均匀的目的是_______ 。
(2)趁热过滤的目的是_______ ,低温干燥的目的是 _______ 。
(3)下列说法正确的是 _______。(填标号)
方法二:硫化碱法,装置如图。
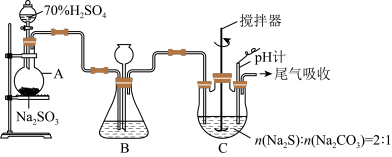
(4)装置C中,将Na2S和Na2CO3以2:1的物质的量之比配成溶液再通入SO2,便可制得Na2S2O3。反应过程中有淡黄色固体析出,后淡黄色固体逐渐溶解,反应大致可分为三步进行,反应的化学方程式分别为SO2+Na2CO3=Na2SO3+CO2,_______ ,S+Na2SO3=Na2S2O3。
(5)装置B中盛放浓硫酸,除干燥气体外,装置B还起到的作用有_______ 。
(6)当pH计读数接近7.0时,应立即停止通SO2的原因是_______ 。
Ⅱ.Na2S2O3的应用
(7)用Na2S2O3溶液测定废水中Ba2+浓度,实验步骤如下:取废水25.00mL,控制适当的酸度加入足量K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解。此时CrO 全部转化为Cr2O
全部转化为Cr2O ;再加过量KI溶液,充分反应,加入淀粉溶液作指示剂,用0.0200mol•L-的Na2S2O3标准溶液进行滴定,反应完全时,消耗Na2S2O3标准溶液体积为15.00mL。已知:
;再加过量KI溶液,充分反应,加入淀粉溶液作指示剂,用0.0200mol•L-的Na2S2O3标准溶液进行滴定,反应完全时,消耗Na2S2O3标准溶液体积为15.00mL。已知: ,则该废水中Ba2+的含量为
,则该废水中Ba2+的含量为 _______ g/L。
I.制备Na2S2O3•5H2O
方法一:亚硫酸钠法。
反应原理:S+
 =Na2S2O3
=Na2S2O3实验步骤:称取一定量的
 于烧杯中,溶于水。另取过量的硫粉,加入少量乙醇充分搅拌均匀后,加到上述溶液中。水浴加热,微沸,反应后趁热过滤。滤液蒸发浓缩、冷却结晶后析出Na2S2O3•5H2O晶体。再进行减压过滤、洗涤并低温干燥。
于烧杯中,溶于水。另取过量的硫粉,加入少量乙醇充分搅拌均匀后,加到上述溶液中。水浴加热,微沸,反应后趁热过滤。滤液蒸发浓缩、冷却结晶后析出Na2S2O3•5H2O晶体。再进行减压过滤、洗涤并低温干燥。(1)向硫粉中加入少量乙醇充分搅拌均匀的目的是
(2)趁热过滤的目的是
(3)下列说法正确的是 _______。(填标号)
| A.蒸发浓缩至溶液表面出现晶膜时,停止加热 |
| B.快速冷却,可析出较大晶体颗粒 |
| C.冷却结晶后的固液混合物中加入乙醇可提高产率 |
| D.洗涤时选用热水作洗涤剂 |
方法二:硫化碱法,装置如图。
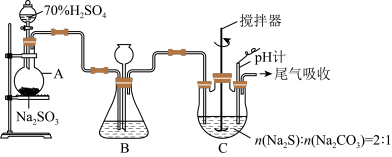
(4)装置C中,将Na2S和Na2CO3以2:1的物质的量之比配成溶液再通入SO2,便可制得Na2S2O3。反应过程中有淡黄色固体析出,后淡黄色固体逐渐溶解,反应大致可分为三步进行,反应的化学方程式分别为SO2+Na2CO3=Na2SO3+CO2,
(5)装置B中盛放浓硫酸,除干燥气体外,装置B还起到的作用有
(6)当pH计读数接近7.0时,应立即停止通SO2的原因是
Ⅱ.Na2S2O3的应用
(7)用Na2S2O3溶液测定废水中Ba2+浓度,实验步骤如下:取废水25.00mL,控制适当的酸度加入足量K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解。此时CrO
 全部转化为Cr2O
全部转化为Cr2O ;再加过量KI溶液,充分反应,加入淀粉溶液作指示剂,用0.0200mol•L-的Na2S2O3标准溶液进行滴定,反应完全时,消耗Na2S2O3标准溶液体积为15.00mL。已知:
;再加过量KI溶液,充分反应,加入淀粉溶液作指示剂,用0.0200mol•L-的Na2S2O3标准溶液进行滴定,反应完全时,消耗Na2S2O3标准溶液体积为15.00mL。已知: ,则该废水中Ba2+的含量为
,则该废水中Ba2+的含量为
您最近一年使用:0次
6 . 燃煤烟气脱硝常用在富O2条件下,氨气选择性的与NO发生反应,某文献报道的一种在V2O5-WO3/TiO2催化剂上脱硝的反应机理如图所示,则下列说法正确的是
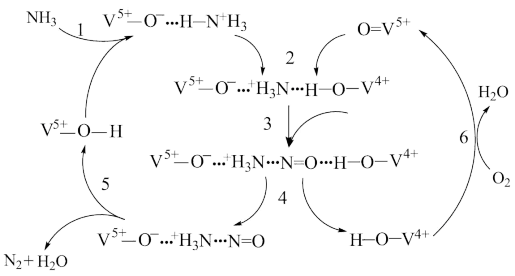

| A.H-O-V4+为该循环反应的催化剂,反应前后质量和化学性质均不变 |
| B.该反应消除了NO和NH3的污染,生成了无毒无害的H2O和N2 |
| C.反应1要在强碱性环境中进行 |
| D.总反应一定为4NH3+4NO+O2=4N2+6H2O |
您最近一年使用:0次
解题方法
7 . 下列实验操作能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 证明Ksp(ZnS)>Ksp(CuS) | 向盛有10滴0.1 mol/L Na2S溶液的试管中滴入0.1 mol/L ZnSO4溶液,至不再有白色沉淀生成;再向其中加入几滴0.1 mol/L CuSO4溶液,观察到产生黑色沉淀 |
| B | 除去碱式滴定管尖嘴处的气泡 | 将尖嘴垂直向下,挤压橡胶管内玻璃球,将气泡排出 |
| C | 探究浓度对反应速率影响 | 向均盛有5mL 0.1mol/L KMnO4溶液的两支试管中,分别加入2mL 0.2mol/L和0.1mol/L H2C2O4溶液,记录溶液褪色所需要的时间 |
| D | 检验溶液中是否含有NH | 取少量溶液加入NaOH稀溶液,并用湿润的红色石蕊试纸检验 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 用活性炭还原NO2可防止空气污染,其反应原理为2C(s)+2NO2(g)  N2(g)+2CO2(g)。在密闭容器中1 mol NO2和足量C发生上述反应,反应相同时间内测得NO2的生成速率与N2的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内测得NO2的转化率随压强的变化如图2所示。
N2(g)+2CO2(g)。在密闭容器中1 mol NO2和足量C发生上述反应,反应相同时间内测得NO2的生成速率与N2的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内测得NO2的转化率随压强的变化如图2所示。
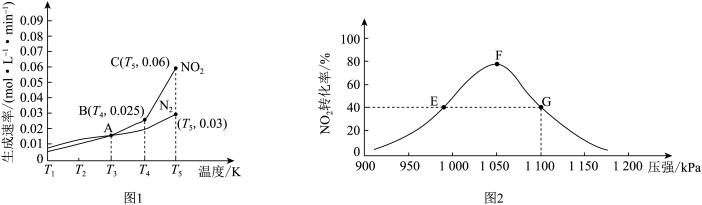
下列说法错误的是
 N2(g)+2CO2(g)。在密闭容器中1 mol NO2和足量C发生上述反应,反应相同时间内测得NO2的生成速率与N2的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内测得NO2的转化率随压强的变化如图2所示。
N2(g)+2CO2(g)。在密闭容器中1 mol NO2和足量C发生上述反应,反应相同时间内测得NO2的生成速率与N2的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内测得NO2的转化率随压强的变化如图2所示。
下列说法错误的是
| A.图1中的A、B、C三个点中只有C点达平衡状态 |
| B.图2中E点的v逆小于F点的v正 |
| C.图2中平衡常数K(E)=K(G),则NO2的平衡浓度c(E)=c(G) |
| D.在恒温恒容下,向图2中G点平衡体系中充入一定量的NO2,与原平衡相比,NO2的平衡转化率减小 |
您最近一年使用:0次
2022-12-02更新
|
1251次组卷
|
23卷引用:河南省鹤壁市高中2022-2023学年高二上学期10月居家测试化学试题
河南省鹤壁市高中2022-2023学年高二上学期10月居家测试化学试题(已下线)押新高考卷09题 速率和平衡-备战2022年高考化学临考题号押题(新高考通版)全书综合测评2吉林省长春市十一高中2022-2023学年高二上学期第一学程考试化学试题湖北省襄阳市第五中学2022-2023学年高二上学期9月化学试题福建省厦门第一中学2022-2023学年高二上学期期中考试化学试题北京市第二中学2022-2023学年高二上学期11月月考化学试题山东省济宁市梁山县第一中学2022-2023学年高二10月月考化学试题福建省莆田第六中学2022-2023学年高二上学期第二次月考(A卷)化学试题山东省济宁市梁山一中2022-2023学年高二上学期11月月考化学试题辽宁省大连市滨城高中联盟2022-2023学年高二上学期期中考试化学试题河南省大联考2022届高三上学期阶段性测试(一)化学试题山东省烟台市莱州第一中学2021-2022学年高二上学期10月月考化学试题黑龙江省哈尔滨市第六中学2021-2022学年高二上学期第一次月考化学试题四川省成都市树德中学2021-2022学年高二上学期10月阶段性测试化学试题湖北省华中师范大学第一附属中学2021-2022学年高二上学期期中检测化学试题(已下线)必考点03 化学平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)山东省“山东学情”2021-2022学年高二11月期中联考化学(A)试题山东师范大学附属中学2021-2022学年高二上学期期中考试化学试题湖南省长沙市雅礼中学2021-2022学年高三上学期第四次月考化学试题 辽宁省辽河油田第一高级中学2021-2022学年高二(甲部)上学期11月考化学试题四川省成都市郫都区2021-2022学年高二上学期期中考试化学试题重庆市万州第二高级中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
9 . 回答下列问题:
I.双氧水和84消毒液是生活中常用的两种消毒剂。
(1)某同学设计如下实验研究H2O2的性质,能证明H2O2有还原性的实验是_____________ (填序号),可作为证据的实验现象是_____________ (填字母序号)。
(2)某届奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是NaClO与H2O2反应产生O2促进藻类快速生长。该反应说明氧化性:NaClO____ H2O2 (填“>”或“<”);当有1个O2生成时,转移电子的个数为_____________ 。
II.全球一半左右的碘是以智利硝石提取硝酸钠后的母液为原料,加入亚硫酸氢钠制取,相关反应如下,配平此化学方程式。
(3) NaIO3+ NaHSO3—— NaHSO4+ Na2SO4+ I2+ H2O;_____
III.锑(Sb)被广泛用于生产各种阻燃剂、合金、陶瓷、半导体元件、医药用品等。以辉锑矿为原料制备金属锑的一种工艺流程如下图。已知:辉锑矿的主要成分为Sb2S3,还含As2S5、PbS、CuO和SiO2等;浸出液主要含盐酸和SbCl3,还含CuCl2、AlCl3和PbCl2等。
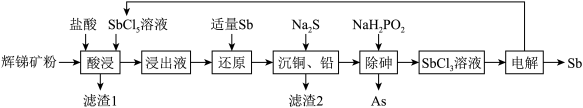
(4)“酸浸”过程中SbCl5和Sb2S3反应有S生成,该反应的还原产物是__________ (填化学式)。
(5)写出“还原”反应的化学方程式__________ 。
I.双氧水和84消毒液是生活中常用的两种消毒剂。
(1)某同学设计如下实验研究H2O2的性质,能证明H2O2有还原性的实验是
| 序号 | 实验 | 实验现象 |
| 1 | 向5% H2O2溶液中滴加酸性KMnO4溶液 | a.溶液紫色褪去;b.有大量气泡产生 |
| 2 | 向5% H2O2溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
II.全球一半左右的碘是以智利硝石提取硝酸钠后的母液为原料,加入亚硫酸氢钠制取,相关反应如下,配平此化学方程式。
(3) NaIO3+ NaHSO3—— NaHSO4+ Na2SO4+ I2+ H2O;
III.锑(Sb)被广泛用于生产各种阻燃剂、合金、陶瓷、半导体元件、医药用品等。以辉锑矿为原料制备金属锑的一种工艺流程如下图。已知:辉锑矿的主要成分为Sb2S3,还含As2S5、PbS、CuO和SiO2等;浸出液主要含盐酸和SbCl3,还含CuCl2、AlCl3和PbCl2等。

(4)“酸浸”过程中SbCl5和Sb2S3反应有S生成,该反应的还原产物是
(5)写出“还原”反应的化学方程式
您最近一年使用:0次
名校
10 . 磁性材料产业是21世纪各国竞相发展的高科技支柱产业之一,磁性材料广泛用于电子信息、军事技术等领域。碳酸锰主要用于制备软磁铁氧体,工业上用氯化铵焙烧锰矿粉制备高纯度碳酸锰的工艺流程如下:
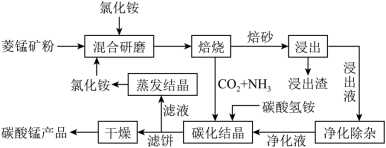
已知:①锰和粉的主要成分是 ,还含少量Fe、Al、Ca、Mg等元素。
,还含少量Fe、Al、Ca、Mg等元素。
②相关金属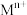 离于
离于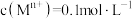 形成
形成 沉淀的pH范围如下:
沉淀的pH范围如下:
回答下列问题:
(1)“焙烧时发生的主要反应的化学方程式为_______ 。
(2)浸出液“净化除杂”过程如下:
①加入 将
将 氧化为
氧化为 ,反应的离子方程式为
,反应的离子方程式为_______ 。
②加入 调节溶液pH范围为
调节溶液pH范围为_______ ,将 、
、 变为沉淀除去。
变为沉淀除去。
(3)碳化结晶时,反应的离子方程式为_______ 。
(4)流程中能循环利用的物质除了氯化铵之外还有_______ 。

已知:①锰和粉的主要成分是
 ,还含少量Fe、Al、Ca、Mg等元素。
,还含少量Fe、Al、Ca、Mg等元素。②相关金属
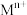 离于
离于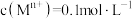 形成
形成 沉淀的pH范围如下:
沉淀的pH范围如下:| 金属离子 |  | 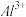 |  |  |  |  |
| 开始沉淀的pH | 1.5 | 3.8 | 6.3 | 9.6 | 10.6 | 8.8 |
| 沉淀完全的pH | 2.8 | 5.2 | 8.3 | 11.6 | 12.6 | 10.8 |
回答下列问题:
(1)“焙烧时发生的主要反应的化学方程式为
(2)浸出液“净化除杂”过程如下:
①加入
 将
将 氧化为
氧化为 ,反应的离子方程式为
,反应的离子方程式为②加入
 调节溶液pH范围为
调节溶液pH范围为 、
、 变为沉淀除去。
变为沉淀除去。(3)碳化结晶时,反应的离子方程式为
(4)流程中能循环利用的物质除了氯化铵之外还有
您最近一年使用:0次



