名校
1 . 某活动小组用碳素钢进行了如下活动:
(1)常温下,可以用铁质容器盛放冷的浓硫酸,其原因是_______ 。
(2)称取碳素钢6g放入15mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用_______ (选填序号)。
A.KSCN溶液和氯水 B.铁粉和KSCN溶液
C.浓氨水 D.酸性KMnO4溶液
②乙同学取560mL(标准状况)气体Y通入足量溴水中,溴水褪色,由此推知混合气体Y中含有_______ ,其化学方程式为:_______ ,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66g,由此推知气体Y中该气体的体积分数为_______ 。
(1)常温下,可以用铁质容器盛放冷的浓硫酸,其原因是
(2)称取碳素钢6g放入15mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用
A.KSCN溶液和氯水 B.铁粉和KSCN溶液
C.浓氨水 D.酸性KMnO4溶液
②乙同学取560mL(标准状况)气体Y通入足量溴水中,溴水褪色,由此推知混合气体Y中含有
您最近一年使用:0次
名校
2 . 钠和钠的化合物有许多重要的用途,碳酸钠可用于从海水提取溴,涉及的反应如下:3Br2+6Na2CO3+3H2O=5NaBr+NaBrO3+6NaHCO3。
(1)用双线桥法标出电子转移的方向和数目_______ 。
(2)该反应的离子方程式为_______ 。
(3)该反应中氧化剂与还原剂的物质的量之比是_______ 。
(4)钠着火时应采取的灭火措施是_______ ,不能用水灭火,原因是_______ (涉及反应的离子方程式)。
(5)用洁净的铂丝蘸取Na2CO3溶液置于酒精灯火焰上灼烧,火焰呈_______ 色。
(6)等质量的Na2CO3和NaHCO3分别与足量的盐酸反应,在相同条件下产生CO2的体积V(Na2CO3)_______ V(NaHCO3)(填“大于”,“小于”或“等于”)。
(7)若加热10.00g的碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了2.48g,则原混合物中碳酸钠的质量分数为_______ 。
(1)用双线桥法标出电子转移的方向和数目
(2)该反应的离子方程式为
(3)该反应中氧化剂与还原剂的物质的量之比是
(4)钠着火时应采取的灭火措施是
(5)用洁净的铂丝蘸取Na2CO3溶液置于酒精灯火焰上灼烧,火焰呈
(6)等质量的Na2CO3和NaHCO3分别与足量的盐酸反应,在相同条件下产生CO2的体积V(Na2CO3)
(7)若加热10.00g的碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了2.48g,则原混合物中碳酸钠的质量分数为
您最近一年使用:0次
名校
3 . 实验室制备“引火铁”(反应活性很高的铁粉)的装置如图所示。下列说法错误的是


| A.稀硫酸中加入少量CuSO4可加快反应速率 |
| B.②和④的主要作用均为吸收水蒸气 |
| C.实验过程中,③中固体颜色发生明显变化 |
| D.点燃酒精灯前,应先在⑤处收集气体并验纯 |
您最近一年使用:0次
名校
4 . 在给定条件下,下列选项所示的物质间转化不能实现的是
A.CaCl2 CaCO3 CaCO3 CaO CaO |
B.NaHCO3 Na2CO3 Na2CO3 NaOH NaOH |
C.Fe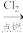 FeCl3 FeCl3 Fe(OH)3 Fe(OH)3 |
D.Al2O3 AlCl3 AlCl3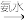 Al(OH)3 Al(OH)3 |
您最近一年使用:0次
5 . 中国传统文化对人类文明贡献巨大,古代文献中充分记载了古代化学研究成果。下列有关古代文献记载的古代中国化学成就,对其说明不合理的是
| 选项 | 目的 | 古代文献 | 说明 |
| A | 运用 | “此物出铜处有,形似曾青,兼绿相间,味极酸苦,磨铁作铜色”——《唐本草》 | 铁能置换铜 |
| B | 鉴别 | 区分硝石(KNO3)和朴消(Na2SO4):“强烧之,紫青烟起,云是真硝石也”——《本草经集注》 | 利用KNO3分解生成氧气的反应 |
| C | 提纯 | “将蓖麻、苏麻子碾碎入一釜中,注水滚煎,其上浮沫即油,以勺掠取,倾于干釜内,其下慢火熬干水气,油即成矣”——《天工开物》 | 萃取、分液、蒸发 |
| D | 性质 | “(火药)乃焰消(KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者”——《本草纲目》 | 利用KNO3和硫的氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 下列有关金属性质和用途的说法正确的是
| A.Na2O常用作呼吸面具的供氧剂 | B.氧化镁的熔点高,可用作耐高温材料 |
| C.实验室常用铝制容器盛装稀硫酸 | D.用于熔化烧碱的坩埚,可用Al2O3制成 |
您最近一年使用:0次
7 . 我国力争于2030年前实现碳达峰,2060年前实现碳中和。 与
与 的反应是降低
的反应是降低 排放的研究热点:
排放的研究热点: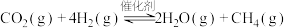
 。回答下列问题:
。回答下列问题:
(1)
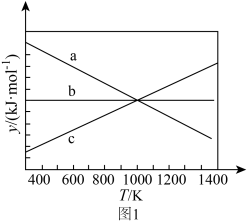
___________ (填“>”或“<”)0,设 ,y随温度的变化关系如图1所示。上述反应对应的曲线是
,y随温度的变化关系如图1所示。上述反应对应的曲线是___________ (填标号)。
(2)生产过程中,为了提高效率,下列对该反应采取的措施中合适的是___________(填标号)。
(3)T℃时,将 和
和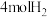 充入密闭容器中发生上述反应,测得平衡时
充入密闭容器中发生上述反应,测得平衡时 和
和 的物质的量浓度与平衡总压的关系如图2所示。则A、B、C三点中
的物质的量浓度与平衡总压的关系如图2所示。则A、B、C三点中 的转化率由大到小的顺序为
的转化率由大到小的顺序为_______ ,C点时 的分压
的分压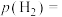
________ MPa,B点时该反应的压强平衡常数
________  (用平衡分压代替浓度)。
(用平衡分压代替浓度)。

(4)在相同条件下, 与
与 还会发生副反应:
还会发生副反应:
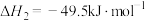 。
。
①一定压强下,随着温度的降低,气体中 与
与 的物质的量
的物质的量___________ (填标号)。
A.均增大 B.均减小 C.均不变
②已知反应速率常数与温度的关系为 ,k为速率常数,R为摩尔气体常量,T为热力学温度,
,k为速率常数,R为摩尔气体常量,T为热力学温度, 为活化能,A为指前因子,为常数。在反应器中按
为活化能,A为指前因子,为常数。在反应器中按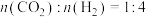 通入反应物,在不同温度、相同的催化剂条件下,反应进行到2min时,测得反应器中
通入反应物,在不同温度、相同的催化剂条件下,反应进行到2min时,测得反应器中 ,
, 的浓度(
的浓度( )如表所示。升高温度时,反应速率增加的倍数大的是活化能大的反应;通过下表可知活化能大的反应是
)如表所示。升高温度时,反应速率增加的倍数大的是活化能大的反应;通过下表可知活化能大的反应是___________ (填“主”或“副”)反应。升高温度,k___________ (填“增大”或“减小”)。
 与
与 的反应是降低
的反应是降低 排放的研究热点:
排放的研究热点: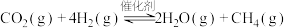
 。回答下列问题:
。回答下列问题:(1)

 ,y随温度的变化关系如图1所示。上述反应对应的曲线是
,y随温度的变化关系如图1所示。上述反应对应的曲线是
(2)生产过程中,为了提高效率,下列对该反应采取的措施中合适的是___________(填标号)。
| A.反应温度愈高愈好 | B.适当增大压强 |
| C.选择合适的催化剂 | D.通入一定量的氮气 |
 和
和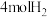 充入密闭容器中发生上述反应,测得平衡时
充入密闭容器中发生上述反应,测得平衡时 和
和 的物质的量浓度与平衡总压的关系如图2所示。则A、B、C三点中
的物质的量浓度与平衡总压的关系如图2所示。则A、B、C三点中 的转化率由大到小的顺序为
的转化率由大到小的顺序为 的分压
的分压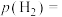

 (用平衡分压代替浓度)。
(用平衡分压代替浓度)。
(4)在相同条件下,
 与
与 还会发生副反应:
还会发生副反应:
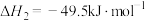 。
。①一定压强下,随着温度的降低,气体中
 与
与 的物质的量
的物质的量A.均增大 B.均减小 C.均不变
②已知反应速率常数与温度的关系为
 ,k为速率常数,R为摩尔气体常量,T为热力学温度,
,k为速率常数,R为摩尔气体常量,T为热力学温度, 为活化能,A为指前因子,为常数。在反应器中按
为活化能,A为指前因子,为常数。在反应器中按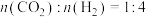 通入反应物,在不同温度、相同的催化剂条件下,反应进行到2min时,测得反应器中
通入反应物,在不同温度、相同的催化剂条件下,反应进行到2min时,测得反应器中 ,
, 的浓度(
的浓度( )如表所示。升高温度时,反应速率增加的倍数大的是活化能大的反应;通过下表可知活化能大的反应是
)如表所示。升高温度时,反应速率增加的倍数大的是活化能大的反应;通过下表可知活化能大的反应是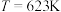 | 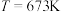 | ||
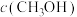 |  | 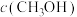 |  |
| 10.8 | 12722 | 345.2 | 42780 |
您最近一年使用:0次
解题方法
8 . 工业上硫酸锰( )常作合成脂肪酸的催化剂。以软锰矿(主要成分为
)常作合成脂肪酸的催化剂。以软锰矿(主要成分为 ,还含有
,还含有 、
、 、CaO、
、CaO、 等)与废铁屑为原料制取硫酸锰的工艺流程如图所示,回答下列问题:
等)与废铁屑为原料制取硫酸锰的工艺流程如图所示,回答下列问题:

(1)“酸浸”前需要将软锰矿粉碎,理由是______ ,废铁屑先与稀硫酸反应生成 ,生成的
,生成的 再与
再与 反应,该过程中每生成
反应,该过程中每生成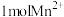 ,至少要消耗
,至少要消耗_______ 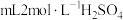 溶液。
溶液。
(2)“滤渣1”的主要成分是______ (填化学式,下同),“滤渣3”的主要成分是_______ 。
(3)“滤渣2”的主要成分为 和
和 ,从化学平衡的角度分析:加
,从化学平衡的角度分析:加 生成“滤渣2”的原因是
生成“滤渣2”的原因是___________ (用离子方程式结合文字表述)。
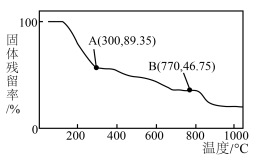
(4)在空气中加热 ,固体残留率随温度的变化如图所示。A点对应固体的成分为
,固体残留率随温度的变化如图所示。A点对应固体的成分为___________ (填化学式,下同),B点对应固体的成分为___________ 。
(5)工业上,常用惰性电极电解硫酸酸化的 溶液制取
溶液制取 。若外电路转移
。若外电路转移 (
( 为阿佛伽德罗常数的值)个电子,则理论上阳极获得
为阿佛伽德罗常数的值)个电子,则理论上阳极获得___________ 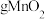 。
。
 )常作合成脂肪酸的催化剂。以软锰矿(主要成分为
)常作合成脂肪酸的催化剂。以软锰矿(主要成分为 ,还含有
,还含有 、
、 、CaO、
、CaO、 等)与废铁屑为原料制取硫酸锰的工艺流程如图所示,回答下列问题:
等)与废铁屑为原料制取硫酸锰的工艺流程如图所示,回答下列问题:
(1)“酸浸”前需要将软锰矿粉碎,理由是
 ,生成的
,生成的 再与
再与 反应,该过程中每生成
反应,该过程中每生成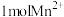 ,至少要消耗
,至少要消耗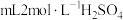 溶液。
溶液。(2)“滤渣1”的主要成分是
(3)“滤渣2”的主要成分为
 和
和 ,从化学平衡的角度分析:加
,从化学平衡的角度分析:加 生成“滤渣2”的原因是
生成“滤渣2”的原因是(4)在空气中加热
 ,固体残留率随温度的变化如图所示。A点对应固体的成分为
,固体残留率随温度的变化如图所示。A点对应固体的成分为
(5)工业上,常用惰性电极电解硫酸酸化的
 溶液制取
溶液制取 。若外电路转移
。若外电路转移 (
( 为阿佛伽德罗常数的值)个电子,则理论上阳极获得
为阿佛伽德罗常数的值)个电子,则理论上阳极获得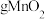 。
。
您最近一年使用:0次
9 . LiClO可广泛用于纺织、造纸、半导体抛光腐蚀等工业。市售的LiClO样品中含有少量LiCl,某实验小组为测定LiClO样品组成,设计了相关实验,实验步骤如下:
I.配制250mLLiClO样品溶液。
准确称取0.67gLiClO样品,加少量水溶解后,冷却至室温,转移并定容。
Ⅱ.测定样品溶液中有效氯含量。
量取25.00mLLiClO样品待测溶液装入碘量瓶中,先迅速加入10mLKI溶液(过量),再加入4mL稀硫酸,立即盖紧瓶塞,于暗处静置5min。小心冲洗瓶塞和瓶壁,加入指示剂,用 的
的 标准溶液滴定至终点。重复实验2次,平均消耗
标准溶液滴定至终点。重复实验2次,平均消耗 标准溶液的体积为20.00mL。
标准溶液的体积为20.00mL。
已知:①光照可加快 被空气氧化的速率;
被空气氧化的速率;
② 。
。
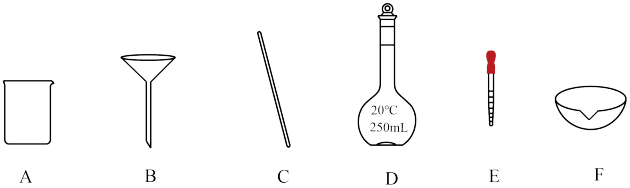
(1)步骤Ⅰ中配制LiClO样品溶液时,下列仪器不需要用到的是___________ (填标号),若定容时,滴加的蒸馏水超过了刻度线,需要采取的措施是___________ 。
(2)步骤Ⅱ中LiClO、KI与稀硫酸发生反应的离子方程式为___________ ,“于暗处静置5min”的目的是___________ 。
(3) 标准溶液应盛放于
标准溶液应盛放于___________ (填“酸式”或“碱式”)滴定管中,滴定时应选用的指示剂为___________ ,滴定终点的现象为___________ 。
(4)LiClO样品的组成可表示为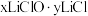 (x、y均为整数),则
(x、y均为整数),则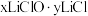 的化学式为
的化学式为___________ 。
I.配制250mLLiClO样品溶液。
准确称取0.67gLiClO样品,加少量水溶解后,冷却至室温,转移并定容。
Ⅱ.测定样品溶液中有效氯含量。
量取25.00mLLiClO样品待测溶液装入碘量瓶中,先迅速加入10mLKI溶液(过量),再加入4mL稀硫酸,立即盖紧瓶塞,于暗处静置5min。小心冲洗瓶塞和瓶壁,加入指示剂,用
 的
的 标准溶液滴定至终点。重复实验2次,平均消耗
标准溶液滴定至终点。重复实验2次,平均消耗 标准溶液的体积为20.00mL。
标准溶液的体积为20.00mL。已知:①光照可加快
 被空气氧化的速率;
被空气氧化的速率;②
 。
。(1)步骤Ⅰ中配制LiClO样品溶液时,下列仪器不需要用到的是

(2)步骤Ⅱ中LiClO、KI与稀硫酸发生反应的离子方程式为
(3)
 标准溶液应盛放于
标准溶液应盛放于(4)LiClO样品的组成可表示为
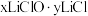 (x、y均为整数),则
(x、y均为整数),则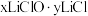 的化学式为
的化学式为
您最近一年使用:0次
解题方法
10 . 含氮物质的回收和利用是环境科学的热点课题之一。
(1)氮位于元素周期表第___________ 周期___________ 族。
(2) 的电子式为
的电子式为___________ 。
(3)在铂原子表面 还原NO的历程如图所示。
还原NO的历程如图所示。

在铂催化剂作用下,NO和 反应的产物中除
反应的产物中除 、
、 和
和 外,还有
外,还有___________ (填化学式),在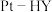 界面上生成
界面上生成 的反应式为
的反应式为___________ 。
(4)工业上,常用纯碱溶液吸收 制备两种含氮的盐,发生反应的离子方程式为
制备两种含氮的盐,发生反应的离子方程式为___________ ,该反应中氧化剂与还原剂的质量之比为___________ 。
(5) (亚硝酸钙)广泛应用于钢筋混凝土工程中,主要用作水泥硬化促进剂和防冻阻锈剂,其部分工艺流程如图。
(亚硝酸钙)广泛应用于钢筋混凝土工程中,主要用作水泥硬化促进剂和防冻阻锈剂,其部分工艺流程如图。

① 中N的化合价为
中N的化合价为___________ 价。
②“滤渣”的主要成分为___________ (填化学式)。
③该工艺需控制NO和 的物质的量之比接近1:1,若
的物质的量之比接近1:1,若 ,则会导致
,则会导致___________ ;若 ,则会导致
,则会导致___________ 。
④生产中需保持弱碱性,在酸性溶液中 会分解,产物之一为NO,该反应的离子方程式为
会分解,产物之一为NO,该反应的离子方程式为___________ 。
(1)氮位于元素周期表第
(2)
 的电子式为
的电子式为(3)在铂原子表面
 还原NO的历程如图所示。
还原NO的历程如图所示。
在铂催化剂作用下,NO和
 反应的产物中除
反应的产物中除 、
、 和
和 外,还有
外,还有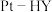 界面上生成
界面上生成 的反应式为
的反应式为(4)工业上,常用纯碱溶液吸收
 制备两种含氮的盐,发生反应的离子方程式为
制备两种含氮的盐,发生反应的离子方程式为(5)
 (亚硝酸钙)广泛应用于钢筋混凝土工程中,主要用作水泥硬化促进剂和防冻阻锈剂,其部分工艺流程如图。
(亚硝酸钙)广泛应用于钢筋混凝土工程中,主要用作水泥硬化促进剂和防冻阻锈剂,其部分工艺流程如图。
①
 中N的化合价为
中N的化合价为②“滤渣”的主要成分为
③该工艺需控制NO和
 的物质的量之比接近1:1,若
的物质的量之比接近1:1,若 ,则会导致
,则会导致 ,则会导致
,则会导致④生产中需保持弱碱性,在酸性溶液中
 会分解,产物之一为NO,该反应的离子方程式为
会分解,产物之一为NO,该反应的离子方程式为
您最近一年使用:0次



