1 . 氧化剂和还原剂在生产生活中应用非常广泛。
(1)我国古代四大发明之一的黑火药是由硫磺粉、硝石(KNO3)、木炭粉按一定比例混合而成,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。在该反应中,氧化剂是_______ ,还原剂是_______ ,氧化产物是_______ ,还原产物是_______ 。
(2)水是生命之源,在常温常压下为无色无味液体,作为一种化学物质,水也会参与很多化学反应,如:
①2Na+2H2O=2NaOH+H2↑
②3NO2+H2O=2HNO3+NO
③2F2+2H2O=4HF+O2
④2H2O=2H2↑+O2↑
以上反应中,H2O只作氧化剂的是_______ ;H2O只作还原剂的是_______ ;H2O既作氧化剂,又作还原剂的是_______ ;H2O既不作氧化剂,又不作还原剂的是_______ 。
(3)高锰酸钾和浓盐酸可以发生如下反应制备氯气(Cl2):2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
①已知KMnO4和MnCl2皆属于可溶盐,写出该反应的离子方程式_______ ;
②抄写化学方程式,用单线桥法标出电子转移的方向和数目_______ ;
③其中,氧化剂和还原剂的个数比为_______ 。
④在酸性溶液中,氧化性:KMnO4_______ Cl2(填大于或小于)。
(4)次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性。H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2的化学方程式:_______ 。
(1)我国古代四大发明之一的黑火药是由硫磺粉、硝石(KNO3)、木炭粉按一定比例混合而成,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。在该反应中,氧化剂是
(2)水是生命之源,在常温常压下为无色无味液体,作为一种化学物质,水也会参与很多化学反应,如:
①2Na+2H2O=2NaOH+H2↑
②3NO2+H2O=2HNO3+NO
③2F2+2H2O=4HF+O2
④2H2O=2H2↑+O2↑
以上反应中,H2O只作氧化剂的是
(3)高锰酸钾和浓盐酸可以发生如下反应制备氯气(Cl2):2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
①已知KMnO4和MnCl2皆属于可溶盐,写出该反应的离子方程式
②抄写化学方程式,用单线桥法标出电子转移的方向和数目
③其中,氧化剂和还原剂的个数比为
④在酸性溶液中,氧化性:KMnO4
(4)次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性。H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2的化学方程式:
您最近一年使用:0次
2 . 东晋《华阳国志•南中志》记载云南镍白铜(铜镍合金),曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子3d能级上的未成对电子数为_____ 。单质铜及镍都是由_____ 键形成的晶体。
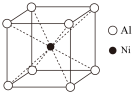
(2)一种铝镍合金的结构如图,与其结构相似的化合物是_____ (填字母)。
(3)雷尼镍(Raney-Ni)是一种历史悠久、应用广泛的催化剂,它催化的一实例为
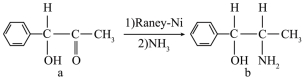
化合物a中所含元素电负性由大到小排序为_____ (填元素符号,下同),化合物b中进行sp3杂化的原子有_____ 。
(4)实验室检验Ni2+可用丁二酮肟(甲)与之作用生成红色配合物沉淀(乙)。反应原理如图:
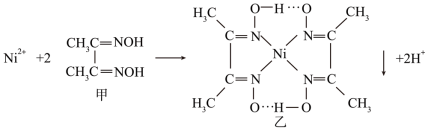
①甲中σ键与π键的个数之比是_____ ,乙中提供空轨道的是_____ (填微粒符号)。
②乙中的化学键类型有_____ (填字母)。
A.极性键 B.π键 C.氢键 D.配位键
(1)镍元素基态原子3d能级上的未成对电子数为
(2)一种铝镍合金的结构如图,与其结构相似的化合物是

| A.氯化钠 | B.氯化铯 | C.石英 | D.金刚石 |

化合物a中所含元素电负性由大到小排序为
(4)实验室检验Ni2+可用丁二酮肟(甲)与之作用生成红色配合物沉淀(乙)。反应原理如图:

①甲中σ键与π键的个数之比是
②乙中的化学键类型有
A.极性键 B.π键 C.氢键 D.配位键
您最近一年使用:0次
3 . I.用燃烧法确定有机物M的元素组成,其实验装置如图所示。

(1)若有机物M样品中只含C、H、O三种元素中的两种或三种,准确称取14.8 g样品,经充分反应后,D装置质量增加10.8 g,E装置质量增加26.4 g,则该M的实验式为_____ 。
(2)该样品的质谱图、核磁共振氢谱图如图,则M的结构简式可能为_____ (填字母)。

(3)仅根据质谱图和下列红外光谱图中信息_____ (填“能”或“不能”)确定该有机物M的结构。

II.按要求回答下列问题:
(4) 的系统命名为
的系统命名为_____ 。
(5) 中含有的官能团名称为
中含有的官能团名称为_____ 。
(6)2-甲基-1-丁烯的结构简式为(不考虑顺反异构)_____ 。
(7)丙烯在一定条件下发生加聚反应的化学方程式为_____ 。

(1)若有机物M样品中只含C、H、O三种元素中的两种或三种,准确称取14.8 g样品,经充分反应后,D装置质量增加10.8 g,E装置质量增加26.4 g,则该M的实验式为
(2)该样品的质谱图、核磁共振氢谱图如图,则M的结构简式可能为

| A.CH3OCH3 | B.CH3CH2OH |
| C.CH3CH2CHO | D.CH3CH2COOH |

II.按要求回答下列问题:
(4)
 的系统命名为
的系统命名为(5)
 中含有的官能团名称为
中含有的官能团名称为(6)2-甲基-1-丁烯的结构简式为(不考虑顺反异构)
(7)丙烯在一定条件下发生加聚反应的化学方程式为
您最近一年使用:0次
4 . 某金属冶炼厂的管道烟泥中含有某些金属,随机取样对烟泥进行分析。由下表中的数据可知,在烟泥中含有一定量的铜、锌以及能造成污染的硫。因此从效益和环保角度出发,应考虑把铜、锌回收利用,并对含硫物质用适当方法进行处理。
【设计方案】

(1)写出步骤①②中含铜元素的物质发生反应的化学方程式:___________ 、___________ 。
(2)本方案中处理废气可以选用的试剂是___________ (填字母)。
a、稀盐酸 b、饱和碳酸钠溶液 c、氢氧化钠溶液 d、饱和碳酸氢钠溶液
(3)步骤⑤中所用的操作方法是___________ 。
(4)在步骤④中,可选用试剂___________ 从混合溶液 中得到铜。
中得到铜。
| 编号 |  |  |  |
| 1 | 10.3% | 5.0% | 1.2% |
| 2 | 11.5% | 4.9% | 1.8% |
| 3 | 12.4% | 10.3% | 0.9% |
【设计方案】

(1)写出步骤①②中含铜元素的物质发生反应的化学方程式:
(2)本方案中处理废气可以选用的试剂是
a、稀盐酸 b、饱和碳酸钠溶液 c、氢氧化钠溶液 d、饱和碳酸氢钠溶液
(3)步骤⑤中所用的操作方法是
(4)在步骤④中,可选用试剂
 中得到铜。
中得到铜。
您最近一年使用:0次
名校
解题方法
5 . 图是有关物质的转化,下列说法不正确的是


| A.转化①②③④均有可能通过化合反应来实现 |
| B.X一定含有碳元素 |
| C.转化④需吸收热量 |
| D.若X是碳,转化①也可以反向进行 |
您最近一年使用:0次
2022-12-11更新
|
239次组卷
|
3卷引用:甘肃省张掖市、陇南2地联考2022-2023学年高一上学期12月期中考试化学试题
名校
6 . 部分短周期元素原子半径与原子序数的关系如图所示, 与
与 形成的化合物
形成的化合物 中每个原子的最外层都达到8电子稳定结构,则下列说法正确的是
中每个原子的最外层都达到8电子稳定结构,则下列说法正确的是

 与
与 形成的化合物
形成的化合物 中每个原子的最外层都达到8电子稳定结构,则下列说法正确的是
中每个原子的最外层都达到8电子稳定结构,则下列说法正确的是
A. 在周期表中的位置为第三周期第Ⅳ族 在周期表中的位置为第三周期第Ⅳ族 |
B. 和 和 形成的化合物为离子化合物 形成的化合物为离子化合物 |
C. 的气态氢化物难溶于水 的气态氢化物难溶于水 |
D. 的结构式为 的结构式为 |
您最近一年使用:0次
名校
7 . 已知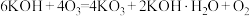 ,
,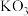 是一种橙红色晶体,能缓慢地分解成
是一种橙红色晶体,能缓慢地分解成 和
和 。下列叙述
。下列叙述不正确 的是
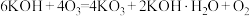 ,
,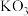 是一种橙红色晶体,能缓慢地分解成
是一种橙红色晶体,能缓慢地分解成 和
和 。下列叙述
。下列叙述A. 与 与 都含有 都含有 |
B.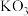 与足量的水反应得到的溶液显碱性 与足量的水反应得到的溶液显碱性 |
C. 完全分解成 完全分解成 和 和 的过程中转移 的过程中转移 电子 电子 |
D.反应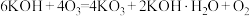 中, 中, 是还原剂 是还原剂 |
您最近一年使用:0次
名校
解题方法
8 . Ⅰ.甲醇是人们开发和利用的一种新能源已知:
①2H2(g)+O2(g)=2H2O(l) △H=-571.8 kJ/mol;
②CH3OH(g)+ O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ/mol。
O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ/mol。
(1)甲醇蒸气完全燃烧的热化学方程式为___________ 。
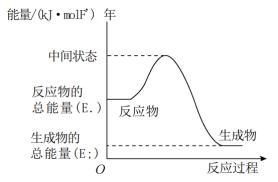
(2)反应②的能量变化如图所示,则△H2=___________ (用E1、E2的代数式表示)。
(3)请你分析H2(g)作为能源与甲醇蒸气作为能源相比的优点:___________ (写出两点即可)。
Ⅱ.碳的单质及其化合物是人类生产生活的主要能源物质。回答下列问题:
(4)有机物M经过太阳光照射可转化成N,转化过程如下:
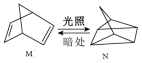 △H=+88.6 kJ/mol。则M、N相比,较稳定的是
△H=+88.6 kJ/mol。则M、N相比,较稳定的是___________ 。
(5)已知CH3OH(l)的燃烧热为-726.5 kJ/mol,CH3OH(l)+ O2(g)=CO2(g)+2H2(g) △H=-a kJ/mol,则a
O2(g)=CO2(g)+2H2(g) △H=-a kJ/mol,则a___________ (填“>”“<”或“=”)726.5。
(6)使Cl2和H2O(g)通过均热的碳层,生成HCl气体和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:___________ 。
①2H2(g)+O2(g)=2H2O(l) △H=-571.8 kJ/mol;
②CH3OH(g)+
 O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ/mol。
O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ/mol。(1)甲醇蒸气完全燃烧的热化学方程式为
(2)反应②的能量变化如图所示,则△H2=

(3)请你分析H2(g)作为能源与甲醇蒸气作为能源相比的优点:
Ⅱ.碳的单质及其化合物是人类生产生活的主要能源物质。回答下列问题:
(4)有机物M经过太阳光照射可转化成N,转化过程如下:
 △H=+88.6 kJ/mol。则M、N相比,较稳定的是
△H=+88.6 kJ/mol。则M、N相比,较稳定的是(5)已知CH3OH(l)的燃烧热为-726.5 kJ/mol,CH3OH(l)+
 O2(g)=CO2(g)+2H2(g) △H=-a kJ/mol,则a
O2(g)=CO2(g)+2H2(g) △H=-a kJ/mol,则a(6)使Cl2和H2O(g)通过均热的碳层,生成HCl气体和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:
您最近一年使用:0次
名校
解题方法
9 . 硒(Se)与硫属于同一主族元素,含硒的几种物质存在如图所示的转化关系。下列说法错误的是


| A.图中只有反应④和⑤不属于氧化还原反应 |
B.反应②中可能有 生成 生成 |
C. 属于二元酸, 属于二元酸, 属于正盐 属于正盐 |
| D.反应⑥中氧化产物与还原产物的物质的量之比为8:1 |
您最近一年使用:0次
名校
10 . 化学和生活密切相关,下列事实与勒夏特列原理无关的是
| A.工业合成氨时,使用高效催化剂 |
B.用饱和食盐水除去 中含有的少量 中含有的少量 |
| C.实验室制取乙酸乙酯时,将乙酸乙酯不断蒸出 |
D. 与 与 反应制备 反应制备 时,通入过量 时,通入过量 |
您最近一年使用:0次
2022-10-14更新
|
175次组卷
|
3卷引用:甘肃省张掖市高台县第一中学2022-2023学年高二上学期期中考试化学试题



