解题方法
1 . 氢溴酸是无色、易挥发的液体,在化工领域用途广泛。实验室模拟一种工业制备氢溴酸的主要流程如下:
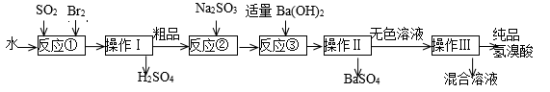
完成下列填空:
(1)写出反应①的离子方程式___________ 。该反应需要在冰水浴中进行,可能的原因是___________ 。
(2)操作I用到的玻璃仪器有蒸馏烧瓶、温度计、___________ 、接液管和锥形瓶。
(3)反应②中Na2SO3的目的是___________ 。
(4)反应③中的Ba(OH)2溶液能否用BaCl2或者Ba(NO3)2溶液代替?说明理由___________ 。
(5)工业氢溴酸往往呈淡黄色:①可能是因为像工业盐酸一样含Fe3+,②还可能是因为含___________ ,如何证明?___________ 。

完成下列填空:
(1)写出反应①的离子方程式
(2)操作I用到的玻璃仪器有蒸馏烧瓶、温度计、
(3)反应②中Na2SO3的目的是
(4)反应③中的Ba(OH)2溶液能否用BaCl2或者Ba(NO3)2溶液代替?说明理由
(5)工业氢溴酸往往呈淡黄色:①可能是因为像工业盐酸一样含Fe3+,②还可能是因为含
您最近一年使用:0次
名校
解题方法
2 . 钠是活泼金属,受热后与氧气剧烈反应,发出黄色火焰,生成一种淡黄色固体——过氧化钠,由于空气中还有其它成分,因此可能还有一些同时发生的其它反应”。某校化学兴趣小组同学据此进行了有关探究。
【猜想】钠在空气中燃烧,生成过氧化钠、氧化钠,还有氮化钠。
【查阅资料】氮化钠与水反应能生成氢氧化钠和氨气。
【实验】①取11.5g钠单质放在一块薄铁皮上,上扣一玻璃罩(玻璃罩内为干燥且无酸性气体的空气),用酒精灯加热薄铁皮,钠燃烧;
②将燃烧产物投入水中,得到0.224L(折算成标准状态)气体和1000mL溶液;
③经检验,该气体为纯净的氧气;
④从1000mL溶液中取出25.00mL溶液,加入1.00mol·L-1HCl溶液至13.50mL时恰好完全反应。
【结论】
(1)通过计算确定钠的燃烧产物中是否含有氮化钠___________ 。
(2)计算钠在空气中燃烧产物中各成分的物质的量之比___________ 。
【猜想】钠在空气中燃烧,生成过氧化钠、氧化钠,还有氮化钠。
【查阅资料】氮化钠与水反应能生成氢氧化钠和氨气。
【实验】①取11.5g钠单质放在一块薄铁皮上,上扣一玻璃罩(玻璃罩内为干燥且无酸性气体的空气),用酒精灯加热薄铁皮,钠燃烧;
②将燃烧产物投入水中,得到0.224L(折算成标准状态)气体和1000mL溶液;
③经检验,该气体为纯净的氧气;
④从1000mL溶液中取出25.00mL溶液,加入1.00mol·L-1HCl溶液至13.50mL时恰好完全反应。
【结论】
(1)通过计算确定钠的燃烧产物中是否含有氮化钠
(2)计算钠在空气中燃烧产物中各成分的物质的量之比
您最近一年使用:0次
2022-09-22更新
|
468次组卷
|
2卷引用:浙江省温州市苍南县2022年第十六届“求知杯”高一化学竞赛试题
名校
解题方法
3 . 一定条件下,将0.1LSO3、0.2LCO2、0.1LNO、0.2LNO2和0.2LNH3混合气体,然后通过分别盛有足量蒸馏水、饱和碳酸氢钠溶液和氢氧化钠溶液的三个洗气瓶(洗气瓶排列顺序不确定)。假设气体通过每个洗气瓶都能充分反应则尾气(已干燥)
| A.不可能是单一气体 |
| B.体积可能为0 |
| C.可能存在原气体中的两种气体 |
| D.成分和洗气瓶的排列顺序无关 |
您最近一年使用:0次
2022-09-22更新
|
274次组卷
|
2卷引用:浙江省温州市苍南县2022年第十六届“求知杯”高一化学竞赛试题
解题方法
4 . 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO 两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法正确的是
两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法正确的是
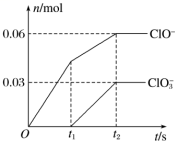
 两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法正确的是
两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法正确的是
| A.苛性钾溶液中KOH的质量是4.94g |
B.氧化性ClO-<ClO |
| C.反应中转移电子的物质的量是0.21mol |
D.ClO 的生成与温度升高无关 的生成与温度升高无关 |
您最近一年使用:0次
名校
解题方法
5 . 将一定质量的镁、铜合金加入到稀硝酸中,两者恰好完全反应,假设反应过程中还原产物全是NO,向所得溶液中加入物质的量浓度为3mol/LNaOH溶液至沉淀完全,测定生成沉淀的质量比合金的质量增加5.1克,则下列有关叙述中正确的是
| A.加入合金的质量可能是6.4克 |
| B.参加反应的硝酸的物质的量为0.1mol |
| C.沉淀完全时消耗NaOH溶液的体积为200ml |
| D.溶解合金时收集到NO气体的体积为2.24升。 |
您最近一年使用:0次
2022-09-22更新
|
348次组卷
|
3卷引用:浙江省温州市苍南县2022年第十六届“求知杯”高一化学竞赛试题
名校
解题方法
6 . 已知:2Na[Al(OH)4]+CO2→2Al(OH)3↓+Na2CO3+H2O。向含2molNaOH,1molBa(OH)2,2molNa[Al(OH)4]的混合溶液中慢慢通入CO2,则通入CO2的量和生成沉淀的量关系正确的是
| 选项 | A | B | C | D |
| n(CO2)(mol) | 2 | 3 | 4 | 6 |
| n(沉淀)(mol) | 1 | 2 | 2 | 3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-09-22更新
|
476次组卷
|
2卷引用:浙江省温州市苍南县2022年第十六届“求知杯”高一化学竞赛试题
解题方法
7 . 某混合物X由A12O3、Fe2O3、Cu、SiO2中的一种或几种物质组成。某校课外兴趣小组以两条途径分别对X进行如下实验探究。
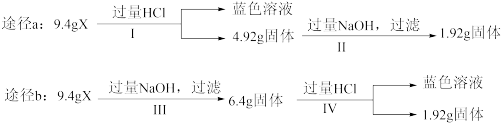
下列有关说法不正确 的是
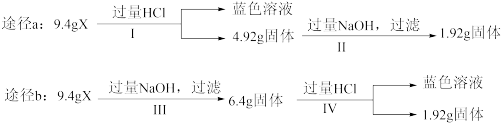
下列有关说法
| A.由Ⅰ可知X中一定存在Fe2O3、Cu |
| B.由Ⅱ和III可得出结论,混合物中无Al2O3 |
| C.6.4g固体为Fe2O3和Cu的混合物,1.92g固体为SiO2和Cu的混合物 |
| D.原混合物中m(Fe2O3)/m(Cu)的比值为1:1 |
您最近一年使用:0次
8 . 设nA为阿伏加德罗常数的数值,下列说法正确的是
①1mol。L-1CuCl2溶液含有2NA个Cl-
②1molNa与一定量O2反应,生成Na2O和Na2O2的混合物,钠失去2NA个电子
③标准状况下,2.24L酒精所含分子数为0.1NA
④常温常压下,28gCO与N2的混合气体的所含的原子数为2NA
⑤常温常压下,1.7gH2O2中含有的电子数为0.9NA
⑥标准状况下,体积相同的两种气体的分子数一定相同
①1mol。L-1CuCl2溶液含有2NA个Cl-
②1molNa与一定量O2反应,生成Na2O和Na2O2的混合物,钠失去2NA个电子
③标准状况下,2.24L酒精所含分子数为0.1NA
④常温常压下,28gCO与N2的混合气体的所含的原子数为2NA
⑤常温常压下,1.7gH2O2中含有的电子数为0.9NA
⑥标准状况下,体积相同的两种气体的分子数一定相同
| A.①③⑤ | B.④⑤⑥ | C.③④⑥ | D.①④⑥ |
您最近一年使用:0次
2022-09-22更新
|
384次组卷
|
3卷引用:浙江省温州市苍南县2022年第十六届“求知杯”高一化学竞赛试题
名校
解题方法
9 . 下列离子方程式书写正确的是
A.澄清石灰水与少量小苏打溶液混合:Ca2++2OH-+2 =CaCO3↓+ =CaCO3↓+ +2H2O +2H2O |
| B.向100mL0.1mol·L-1的FeBr2溶液中通入0.012molCl2: 10Fe2++14Br-+12Cl2=10Fe3++7Br2+24Cl- |
C.漂白粉溶液中通入少量SO2气体:Ca2++2ClO-+ +H2O=CaSO3↓+2HClO +H2O=CaSO3↓+2HClO |
D.加热条件下,向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至 刚好沉淀完全: Ba2++2OH-+ 刚好沉淀完全: Ba2++2OH-+ +H++ +H++ =BaSO4↓+NH3·H2O+H2O =BaSO4↓+NH3·H2O+H2O |
您最近一年使用:0次
2022-09-22更新
|
2073次组卷
|
8卷引用:浙江省温州市苍南县2022年第十六届“求知杯”高一化学竞赛试题
12-13高一上·黑龙江大庆·期末
名校
解题方法
10 . 将2molNaHCO3和一定量(不为0)的Na2O2固体混合,在加热条件下让其充分反应,150℃下所得气体仅含2种组分,则反应后固体的物质的量n(mol)的取值范围是
| A.n=1 | B.1<n<2 | C.2≤n<4 | D.n≥4 |
您最近一年使用:0次
2022-09-22更新
|
1091次组卷
|
6卷引用:浙江省温州市苍南县2022年第十六届“求知杯”高一化学竞赛试题



