名校
解题方法
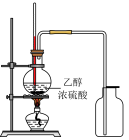
1 . 下列实验装置图正确的是
|
|
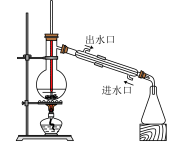
| A.实验室制乙烯 | B.石油分馏 |
|
|
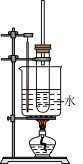
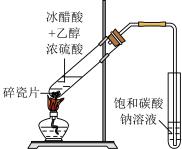
| C.实验室制硝基苯 | D.实验室制乙酸乙酯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7日内更新
|
113次组卷
|
4卷引用:吉林省辽源市田家炳高中友好学校2022-2023学年高二下学期7月期末联考化学试题
吉林省辽源市田家炳高中友好学校2022-2023学年高二下学期7月期末联考化学试题河北省唐山市遵化市第一中学2022-2023学年高二下学期第二次月考化学试题(已下线)题型05 有机实验分析-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(人教版2019)(已下线)专题06 有机实验-备战2023-2024学年高二化学下学期期末真题分类汇编(辽宁、黑龙江、吉林专用)
2 . 回答下列问题
(1)现有 醋酸钠溶液500mL(已知室温下醋酸的电离常数
醋酸钠溶液500mL(已知室温下醋酸的电离常数 )。
)。
①写出醋酸钠水解反应的离子方程式:______ 。
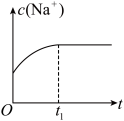
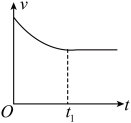
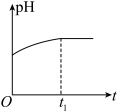
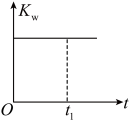
②下列图像能说明醋酸钠的水解反应达到平衡的是______ 。
③在醋酸钠溶液中加入下列少量物质,能使水解平衡右移的有______ 。
A.冰醋酸 B.纯碱固体 C.醋酸钠固体 D.氯化铵固体
④在室温下, 醋酸钠溶液的pH约为
醋酸钠溶液的pH约为______ 。
(2)如图是某温度下,将足量的 固体溶于一定量水中达到溶解平衡后,假定溶液体积不变的情况下,加入
固体溶于一定量水中达到溶解平衡后,假定溶液体积不变的情况下,加入 使
使 增大过程中,溶液中
增大过程中,溶液中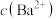 和
和 的变化曲线,根据图中的数据分析、计算。
的变化曲线,根据图中的数据分析、计算。 的
的
______ 。
⑥沉淀转化的离子方程式为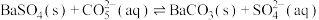 ,该反应的平衡常数
,该反应的平衡常数
______ 。
⑦向1L 溶液中加入足量
溶液中加入足量 固体,假定溶液体积不变,当溶液中
固体,假定溶液体积不变,当溶液中 的浓度为
的浓度为 时,溶解
时,溶解 的质量为
的质量为______ g。
(1)现有
 醋酸钠溶液500mL(已知室温下醋酸的电离常数
醋酸钠溶液500mL(已知室温下醋酸的电离常数 )。
)。①写出醋酸钠水解反应的离子方程式:
②下列图像能说明醋酸钠的水解反应达到平衡的是
A.溶液中 与反应时间t的关系 与反应时间t的关系 | B. 的水解速率与反应时间t的关系 的水解速率与反应时间t的关系 | C.溶液的pH与反应时间t的关系 | D. 与反应时间t的关系 与反应时间t的关系 |
|
|
|
|
A.冰醋酸 B.纯碱固体 C.醋酸钠固体 D.氯化铵固体
④在室温下,
 醋酸钠溶液的pH约为
醋酸钠溶液的pH约为(2)如图是某温度下,将足量的
 固体溶于一定量水中达到溶解平衡后,假定溶液体积不变的情况下,加入
固体溶于一定量水中达到溶解平衡后,假定溶液体积不变的情况下,加入 使
使 增大过程中,溶液中
增大过程中,溶液中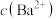 和
和 的变化曲线,根据图中的数据分析、计算。
的变化曲线,根据图中的数据分析、计算。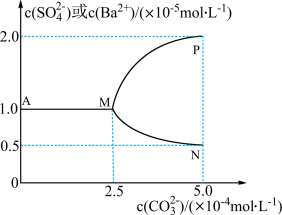
 的
的
⑥沉淀转化的离子方程式为
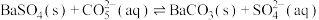 ,该反应的平衡常数
,该反应的平衡常数
⑦向1L
 溶液中加入足量
溶液中加入足量 固体,假定溶液体积不变,当溶液中
固体,假定溶液体积不变,当溶液中 的浓度为
的浓度为 时,溶解
时,溶解 的质量为
的质量为
您最近一年使用:0次
3 . 氢能是极具发展潜力的清洁能源,以氢燃料为代表的燃料电池有良好的应用前景。
(1)298K时,1g 燃烧生成
燃烧生成 放热120.9kJ,1mol
放热120.9kJ,1mol 蒸发吸热44kJ,表示
蒸发吸热44kJ,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为______ 。
(2)碱性(电解质为KOH溶液)氢氧燃料电池中负极电极反应式为______ 。
(3)工业上常用甲烷水蒸气重整制备氢气,体系中发生如下反应。
Ⅰ.
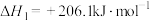
Ⅱ.

①下列措施中,不能提高 平衡转化率的是
平衡转化率的是______ (填标号)。
A.增加 用量 B.增加
用量 B.增加 用量
用量
C.恒温恒压下通入惰性气体 D.加入催化剂
②恒温恒压条件下,1mol 和1mol
和1mol 反应达平衡时,
反应达平衡时, 的转化率为
的转化率为 ,
, 的物质的量为b mol。其他条件不变,
的物质的量为b mol。其他条件不变, 起始量增加到4mol,达平衡时,
起始量增加到4mol,达平衡时,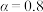 ,
,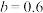 ,平衡体系中
,平衡体系中 的物质的量分数为
的物质的量分数为______ (结果保留3位有效数字,下同),该条件下,反应Ⅱ的化学平衡常数
______ 。
③“碳达峰·碳中和”是我国社会发展重大战略之一, 还原
还原 是实现“双碳”经济的有效途径之一,相关的主要反应为:
是实现“双碳”经济的有效途径之一,相关的主要反应为:

______ 。
(4)氢气还是合成氨工业的原料气,其反应为:

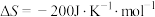 。该反应在常温下
。该反应在常温下______ (填“能”或“不能”)自发。
(1)298K时,1g
 燃烧生成
燃烧生成 放热120.9kJ,1mol
放热120.9kJ,1mol 蒸发吸热44kJ,表示
蒸发吸热44kJ,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为(2)碱性(电解质为KOH溶液)氢氧燃料电池中负极电极反应式为
(3)工业上常用甲烷水蒸气重整制备氢气,体系中发生如下反应。
Ⅰ.

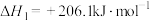
Ⅱ.


①下列措施中,不能提高
 平衡转化率的是
平衡转化率的是A.增加
 用量 B.增加
用量 B.增加 用量
用量C.恒温恒压下通入惰性气体 D.加入催化剂
②恒温恒压条件下,1mol
 和1mol
和1mol 反应达平衡时,
反应达平衡时, 的转化率为
的转化率为 ,
, 的物质的量为b mol。其他条件不变,
的物质的量为b mol。其他条件不变, 起始量增加到4mol,达平衡时,
起始量增加到4mol,达平衡时,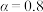 ,
,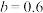 ,平衡体系中
,平衡体系中 的物质的量分数为
的物质的量分数为
③“碳达峰·碳中和”是我国社会发展重大战略之一,
 还原
还原 是实现“双碳”经济的有效途径之一,相关的主要反应为:
是实现“双碳”经济的有效途径之一,相关的主要反应为:

(4)氢气还是合成氨工业的原料气,其反应为:


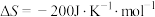 。该反应在常温下
。该反应在常温下
您最近一年使用:0次
名校
解题方法
4 . 如图甲所示,A为新型高效的甲烷燃料电池,采用铂为电极材料,两电极上分别通入 和
和 ,电解质溶液为KOH溶液,B为浸透饱和硫酸钠溶液和酚酞溶液的滤纸,滤纸中央滴有一滴
,电解质溶液为KOH溶液,B为浸透饱和硫酸钠溶液和酚酞溶液的滤纸,滤纸中央滴有一滴 ,溶液,C、D为电解槽。
,溶液,C、D为电解槽。 ,打开
,打开 ,通电后,B中的紫红色液滴向d端移动,则电源b端为
,通电后,B中的紫红色液滴向d端移动,则电源b端为______ 极,电源a端的电极反应式为______ .
(2)通电过程中滤纸c端的生成物是______ .
(3)闭合 、打开
、打开 ,若C装置中为足量的
,若C装置中为足量的 溶液,C装置中总反应的离子方程式为
溶液,C装置中总反应的离子方程式为______ ,电解结束后,为了使C装置溶液恢复原样,则可以在反应后的溶液中加入______ (填化学式)。
(4)D装置中有200mL一定浓度的NaCl与 的混合溶液,电解时两极所得气体的体积随时间变化的关系如图乙所示(气体体积已换算成标准状况下的,电解前后溶液的体积变化忽略不计),则原混合溶液中NaCl的物质的量浓度为
的混合溶液,电解时两极所得气体的体积随时间变化的关系如图乙所示(气体体积已换算成标准状况下的,电解前后溶液的体积变化忽略不计),则原混合溶液中NaCl的物质的量浓度为______  ,
, 阴极的电极反应式为
阴极的电极反应式为______ ,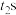 时所得溶液的
时所得溶液的
______ 。
 和
和 ,电解质溶液为KOH溶液,B为浸透饱和硫酸钠溶液和酚酞溶液的滤纸,滤纸中央滴有一滴
,电解质溶液为KOH溶液,B为浸透饱和硫酸钠溶液和酚酞溶液的滤纸,滤纸中央滴有一滴 ,溶液,C、D为电解槽。
,溶液,C、D为电解槽。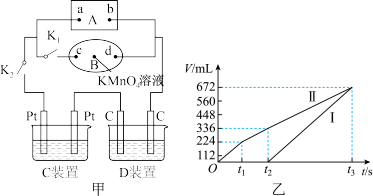
 ,打开
,打开 ,通电后,B中的紫红色液滴向d端移动,则电源b端为
,通电后,B中的紫红色液滴向d端移动,则电源b端为(2)通电过程中滤纸c端的生成物是
(3)闭合
 、打开
、打开 ,若C装置中为足量的
,若C装置中为足量的 溶液,C装置中总反应的离子方程式为
溶液,C装置中总反应的离子方程式为(4)D装置中有200mL一定浓度的NaCl与
 的混合溶液,电解时两极所得气体的体积随时间变化的关系如图乙所示(气体体积已换算成标准状况下的,电解前后溶液的体积变化忽略不计),则原混合溶液中NaCl的物质的量浓度为
的混合溶液,电解时两极所得气体的体积随时间变化的关系如图乙所示(气体体积已换算成标准状况下的,电解前后溶液的体积变化忽略不计),则原混合溶液中NaCl的物质的量浓度为 ,
, 阴极的电极反应式为
阴极的电极反应式为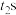 时所得溶液的
时所得溶液的
您最近一年使用:0次
5 . 前四周期元素A、B、C、D、E、F的原子序数依次增大。A元素基态原子的价电子排布式为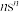 ,A与B同周期,A与C有相似的化学性质;B与D同主族,且基态B原子中p能级和s能级上的电子数相同;C与D同周期,C的基态原子有1个未成对电子:E和F是不相邻的同周期同族元素。
,A与B同周期,A与C有相似的化学性质;B与D同主族,且基态B原子中p能级和s能级上的电子数相同;C与D同周期,C的基态原子有1个未成对电子:E和F是不相邻的同周期同族元素。
(1)写出基态A原子电子排布式______ ,基态C原子价层电子轨道表示式______ 。
(2)A、B、C三种元素第一电离能由小到大的顺序是______ (用元素符号表示,下同)。
(3)五种元素中未成对电子数最多的元素是______ 。
(4)基态F原子有______ 种不同空间运动状态的电子。
(5)D的阴离子与C的阳离子在溶液中反应有白色胶状沉淀和无色气体生成,写出反应的离子方程式______ 。
(6)写出含E的高价阳离子的溶液吸收(5)中生成的气体的离子反应方程式______ 。
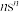 ,A与B同周期,A与C有相似的化学性质;B与D同主族,且基态B原子中p能级和s能级上的电子数相同;C与D同周期,C的基态原子有1个未成对电子:E和F是不相邻的同周期同族元素。
,A与B同周期,A与C有相似的化学性质;B与D同主族,且基态B原子中p能级和s能级上的电子数相同;C与D同周期,C的基态原子有1个未成对电子:E和F是不相邻的同周期同族元素。(1)写出基态A原子电子排布式
(2)A、B、C三种元素第一电离能由小到大的顺序是
(3)五种元素中未成对电子数最多的元素是
(4)基态F原子有
(5)D的阴离子与C的阳离子在溶液中反应有白色胶状沉淀和无色气体生成,写出反应的离子方程式
(6)写出含E的高价阳离子的溶液吸收(5)中生成的气体的离子反应方程式
您最近一年使用:0次
名校
解题方法
6 . 室温下,用 NaOH溶液滴定10.00mL
NaOH溶液滴定10.00mL HClO溶液,水的电离程度随NaOH溶液体积的变化曲线如图所示。已知室温下HClO电离常数
HClO溶液,水的电离程度随NaOH溶液体积的变化曲线如图所示。已知室温下HClO电离常数 ,下列说法不正确的是
,下列说法不正确的是
 NaOH溶液滴定10.00mL
NaOH溶液滴定10.00mL HClO溶液,水的电离程度随NaOH溶液体积的变化曲线如图所示。已知室温下HClO电离常数
HClO溶液,水的电离程度随NaOH溶液体积的变化曲线如图所示。已知室温下HClO电离常数 ,下列说法不正确的是
,下列说法不正确的是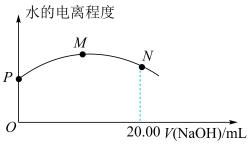
A.当滴入5.00mLNaOH溶液时,溶液中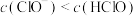 |
B.M点对应的水溶液 |
| C.M点为滴定终点 |
D.N点溶液中,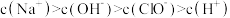 |
您最近一年使用:0次
名校
解题方法
7 . 某厂采用电化学原理回收利用工业废气中的 和
和 ,实验原理示意图如下。
,实验原理示意图如下。
 和
和 ,实验原理示意图如下。
,实验原理示意图如下。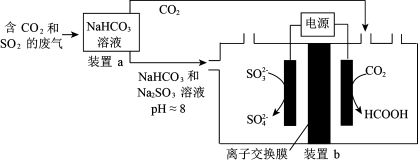
A.废气中 和 和 排放到大气中均会形成酸雨 排放到大气中均会形成酸雨 |
B.装置a中溶液的作用是吸收废气中的 和 和 |
| C.装置b中应该使用阳离子交换膜 |
| D.装置b是把化学能转化成电能的装置 |
您最近一年使用:0次
名校
解题方法
8 . 在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误的是
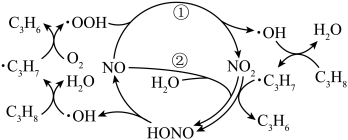
| A.上述过程既有非极性键的断裂,又有非极性键的形成 |
| B.历程①中·OOH作氧化剂 |
C.增大NO的量, 的平衡转化率不变 的平衡转化率不变 |
| D.当NO主要发生②的历程时,最终生成的水减少 |
您最近一年使用:0次
9 . 下列事实不能通过比较氟元素和氯元素的电负性进行解释的是
| A.F—F键的键能小于Cl—Cl键的键能 |
| B.氟元素无正化合价而氯元素有正化合价 |
| C.氟化氢分子的极性强于氯化氢分子的极性 |
D. 可以从熔融的氯化钠中置换出 可以从熔融的氯化钠中置换出 |
您最近一年使用:0次
名校
解题方法
10 . 用已知浓度的NaOH溶液滴定未知浓度的醋酸溶液,下列操作中会使测定结果偏低的是
| A.锥形瓶用水洗净后残留有少量水 |
| B.量取待测液后滴加几滴甲基橙作指示剂 |
| C.滴定前,滴定管尖嘴部分有气泡,滴定后气泡消失 |
| D.用滴定管量取待测液时,先平视后俯视读数 |
您最近一年使用:0次