1 . 为了探究温度对水解平衡的影响,用手持技术测定一定浓度 溶液的pH随温度变化的关系如图所示,下列说法不正确的是
溶液的pH随温度变化的关系如图所示,下列说法不正确的是
 溶液的pH随温度变化的关系如图所示,下列说法不正确的是
溶液的pH随温度变化的关系如图所示,下列说法不正确的是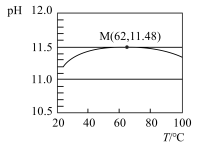
| A.该实验能证明升温促进水解 | B.点M之后 水解放热 水解放热 |
C.点M处溶液中 略大于 略大于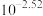 mol/L mol/L | D.点M后pH下降是因为升温对 的影响更大 的影响更大 |
您最近一年使用:0次
2 . 已知 ,甲同学将
,甲同学将 、
、 混合气体通入稍过量
混合气体通入稍过量 溶液中制备
溶液中制备 (同等条件下
(同等条件下 的氧化性强于
的氧化性强于 ),为检验制得了
),为检验制得了 ,甲进行了以下实验:
,甲进行了以下实验:
下列说法不正确的是
 ,甲同学将
,甲同学将 、
、 混合气体通入稍过量
混合气体通入稍过量 溶液中制备
溶液中制备 (同等条件下
(同等条件下 的氧化性强于
的氧化性强于 ),为检验制得了
),为检验制得了 ,甲进行了以下实验:
,甲进行了以下实验:| 实验 | 实验现象 | |
| ① | 取 制备的稀溶液,加 制备的稀溶液,加 溶液,滴加几滴淀粉溶液 溶液,滴加几滴淀粉溶液 | 不变蓝 |
| ② | 取 制备的稀溶液,滴加几滴 制备的稀溶液,滴加几滴 至 至 ,加 ,加 溶液,滴加几滴淀粉溶液 溶液,滴加几滴淀粉溶液 | |
| ③ | 取 水,滴加几滴 水,滴加几滴 至 至 ,加 ,加 溶液,滴加几滴淀粉溶液 溶液,滴加几滴淀粉溶液 | 不变蓝 |
A.实验①说明 不能氧化 不能氧化 |
| B.实验②的实验现象是溶液变蓝 |
C.实验③的目的是验证当溶液 时,稀 时,稀 不能氧化 不能氧化 |
D.上述3组实验无法证明②中一定含 ,还需补充实验 ,还需补充实验 |
您最近一年使用:0次
3 . 富硼渣中含有镁硼酸盐(2MgO·B2O3)、镁硅酸盐(2MgO·SiO2)及少量Al2O3、FeO等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸(H3BO3)晶体的一种工艺流程如下:
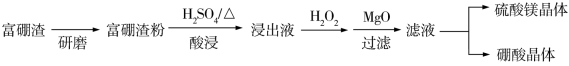
已知:生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)
(1)上述流程中能加快反应速率的措施有___________ 、___________ 等。
(2)酸浸时发生反应:2MgO·SiO2+2H2SO4=2MgSO4+SiO2+2H2O, 2MgO·B2O3+2H2SO4+H2O=2H3BO3+2MgSO4。
①上述反应体现出酸性强弱:H2SO4___________ H3BO3(填“>”或“<”)。
②酸浸时,富硼渣中所含Al2O3和FeO也同时溶解,写出相关反应的化学方程式:___________ 、___________ 。
③已知硼酸与过量NaOH溶液发生的中和反应为:H3BO3+OH− =B(OH) 。下列关于硼酸的说法正确的是
。下列关于硼酸的说法正确的是 ___________
A.硼酸是一元酸
B.硼酸的电离方程式可表示为:H3BO3+H2O B(OH)
B(OH) +H+
+H+
C.向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
(3)检验褐色浸出液中的杂质离子:取少量浸出液,___________ (填操作和现象),证明溶液中含有Fe2+。
(4)除去浸出液中的杂质离子:用MgO调节溶液的pH至___________ 以上,使杂质离子转化为___________ (填化学式)沉淀,过滤。
(5)获取晶体:ⅰ.浓缩滤液,使MgSO4和H3BO3接近饱和;ⅱ.控制温度使两种晶体分别从溶液中结晶。结合下图溶解度曲线,简述ⅱ的方法:将浓缩液加入到高压釜中,___________ (将方法补充完整)。

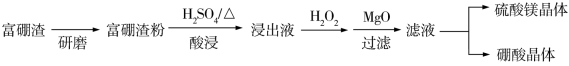
已知:生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)
| Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | |
| 开始沉淀时 | 1.9 | 3.4 | 7.0 | 9.1 |
| 完全沉淀时 | 3.2 | 4.7 | 9.0 | 11.1 |
(2)酸浸时发生反应:2MgO·SiO2+2H2SO4=2MgSO4+SiO2+2H2O, 2MgO·B2O3+2H2SO4+H2O=2H3BO3+2MgSO4。
①上述反应体现出酸性强弱:H2SO4
②酸浸时,富硼渣中所含Al2O3和FeO也同时溶解,写出相关反应的化学方程式:
③已知硼酸与过量NaOH溶液发生的中和反应为:H3BO3+OH− =B(OH)
 。下列关于硼酸的说法正确的是
。下列关于硼酸的说法正确的是 A.硼酸是一元酸
B.硼酸的电离方程式可表示为:H3BO3+H2O
 B(OH)
B(OH) +H+
+H+C.向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
(3)检验褐色浸出液中的杂质离子:取少量浸出液,
(4)除去浸出液中的杂质离子:用MgO调节溶液的pH至
(5)获取晶体:ⅰ.浓缩滤液,使MgSO4和H3BO3接近饱和;ⅱ.控制温度使两种晶体分别从溶液中结晶。结合下图溶解度曲线,简述ⅱ的方法:将浓缩液加入到高压釜中,

您最近一年使用:0次
名校
解题方法
4 . 利用Heck反应合成一种药物中间体需要经历如图反应过程。下列有关说法错误的是
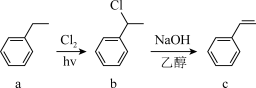

| A.a、b、c中只有a是苯的同系物 |
| B.c既可发生氧化反应,也可发生聚合反应 |
| C.a、b、c中所有碳原子均有可能共面 |
| D.向反应b→c所得混合物中滴入AgNO3溶液,可证明b中是否含有氯元素 |
您最近一年使用:0次
5 . 甲醇是一种重要的化工原料,由 制取甲醇可实现资源的循环利用。
制取甲醇可实现资源的循环利用。
Ⅰ.二氧化碳催化加氢制甲醇
(1)①已知:
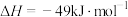 ,该反应在
,该反应在____ (填“高温”、“低温”或“任意温度”)下能自发进行。
②在恒温恒容条件下发生反应: ,下列说法能证明此反应达到平衡状态的是
,下列说法能证明此反应达到平衡状态的是____ 。
A. B.气体的平均摩尔质量不再改变
B.气体的平均摩尔质量不再改变
C.单位时间内断裂2mol C=O键同时断裂3mol H−H键 D.
(2)合成 过程起始物
过程起始物 时,在不同条件下达到平衡,设体系中
时,在不同条件下达到平衡,设体系中 的转化率为
的转化率为 ,在
,在 ℃下的
℃下的 、在
、在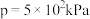 下的
下的 如图所示。已知在
如图所示。已知在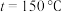 ,
,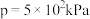 反应条件下,反应经过10s达到平衡,
反应条件下,反应经过10s达到平衡, :
:
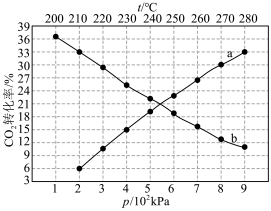
①图中对应的等温曲线是a,理由是_________ 。
② 的分压平均变化率为
的分压平均变化率为______  ,该温度下
,该温度下
______  。(保留两位有效数字)(已知:对于气相反应,可以用分压表示,分压=总压×物质的量分数)。
。(保留两位有效数字)(已知:对于气相反应,可以用分压表示,分压=总压×物质的量分数)。
(3)二氧化碳催化加氢制甲醇反应往往伴随着副反应的发生: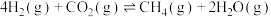 ,在一定温度和压强下,为了提高反应速率和甲醇的选择性,应当
,在一定温度和压强下,为了提高反应速率和甲醇的选择性,应当________ 。
Ⅱ.电解催化 制甲醇
制甲醇
(4)电解催化 制甲醇装置如图所示:
制甲醇装置如图所示:
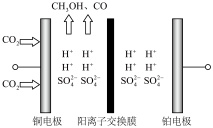
①装置中的 移动方向为
移动方向为________ 。(填“从铜极到铂电极”或“从铂电极到铜电极”)
②电解催化 制甲醇的电极反应方程式为
制甲醇的电极反应方程式为_________ 。
 制取甲醇可实现资源的循环利用。
制取甲醇可实现资源的循环利用。Ⅰ.二氧化碳催化加氢制甲醇
(1)①已知:

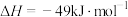 ,该反应在
,该反应在②在恒温恒容条件下发生反应:
 ,下列说法能证明此反应达到平衡状态的是
,下列说法能证明此反应达到平衡状态的是A.
 B.气体的平均摩尔质量不再改变
B.气体的平均摩尔质量不再改变C.单位时间内断裂2mol C=O键同时断裂3mol H−H键 D.

(2)合成
 过程起始物
过程起始物 时,在不同条件下达到平衡,设体系中
时,在不同条件下达到平衡,设体系中 的转化率为
的转化率为 ,在
,在 ℃下的
℃下的 、在
、在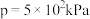 下的
下的 如图所示。已知在
如图所示。已知在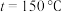 ,
,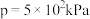 反应条件下,反应经过10s达到平衡,
反应条件下,反应经过10s达到平衡, :
:
①图中对应的等温曲线是a,理由是
②
 的分压平均变化率为
的分压平均变化率为 ,该温度下
,该温度下
 。(保留两位有效数字)(已知:对于气相反应,可以用分压表示,分压=总压×物质的量分数)。
。(保留两位有效数字)(已知:对于气相反应,可以用分压表示,分压=总压×物质的量分数)。(3)二氧化碳催化加氢制甲醇反应往往伴随着副反应的发生:
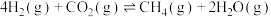 ,在一定温度和压强下,为了提高反应速率和甲醇的选择性,应当
,在一定温度和压强下,为了提高反应速率和甲醇的选择性,应当Ⅱ.电解催化
 制甲醇
制甲醇(4)电解催化
 制甲醇装置如图所示:
制甲醇装置如图所示:
①装置中的
 移动方向为
移动方向为②电解催化
 制甲醇的电极反应方程式为
制甲醇的电极反应方程式为
您最近一年使用:0次
6 . 某小组同学探究溶液中的 能否被金属钠还原,进行实验:
能否被金属钠还原,进行实验:
①在干燥试管中加入绿豆大小的金属钠,逐滴滴加 溶液,产生无色气体,溶液由紫红色变为浅绿色
溶液,产生无色气体,溶液由紫红色变为浅绿色 。
。
②向 溶液中持续通入
溶液中持续通入 ,水浴加热,溶液颜色无明显变化。
,水浴加热,溶液颜色无明显变化。
③向 溶液中加入
溶液中加入 固体,溶液由紫红色变为浅绿色。
固体,溶液由紫红色变为浅绿色。
下列说法不正确 的是
 能否被金属钠还原,进行实验:
能否被金属钠还原,进行实验:①在干燥试管中加入绿豆大小的金属钠,逐滴滴加
 溶液,产生无色气体,溶液由紫红色变为浅绿色
溶液,产生无色气体,溶液由紫红色变为浅绿色 。
。②向
 溶液中持续通入
溶液中持续通入 ,水浴加热,溶液颜色无明显变化。
,水浴加热,溶液颜色无明显变化。③向
 溶液中加入
溶液中加入 固体,溶液由紫红色变为浅绿色。
固体,溶液由紫红色变为浅绿色。下列说法
| A.实验①中还可能观察到钠块浮在溶液表面,剧烈燃烧,发出黄色火焰 |
| B.实验②中的现象说明实验①中溶液变色的原因与产生的气体无关 |
C.实验③中的现象说明实验①中可能发生的反应: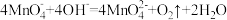 |
D.上述实验能证明溶液中的 可以被金属钠还原 可以被金属钠还原 |
您最近一年使用:0次
2023-05-07更新
|
1689次组卷
|
7卷引用:北京市海淀区2022-2023学年高三第二次模拟(下学期期末)考试化学试题
北京市海淀区2022-2023学年高三第二次模拟(下学期期末)考试化学试题(已下线)T12-化学反应及限度(已下线)第4讲 钠及其重要化合物北京师范大学附属实验中学2023-2024学年暑期高三第一次督导化学试题(已下线)选择题11-14(已下线)选择题6-10湖南省邵阳市第二中学2023-2024学年高二上学期基础知识竞赛化学试题
名校
7 . 短周期主族元素A、B、C、D的原子序数依次增大,A元素与C元素同主族,B的单质可以在A的单质中燃烧,生成一种具有强氧化性的物质,C元素与D元素相邻,D元素最高价氧化物对应的水化物和氢化物溶于水都能完全电离。下列说法错误的是
| A.元素A与元素B形成的两种化合物中,阴、阳离子个数比都是1:2 |
| B.利用D的单质和C的氢化物反应,可证明非金属性:D>C |
| C.可用酒精除去试管内壁附着的C单质 |
| D.简单离子半径:C>D>A>B |
您最近一年使用:0次
2023-05-30更新
|
385次组卷
|
3卷引用:湘豫名校联考2023届高三下学期第三次模拟考试(5月)理科综合化学试题
湘豫名校联考2023届高三下学期第三次模拟考试(5月)理科综合化学试题(已下线)考点巩固卷05 物质结构 元素周期律(2大考点50题)-2024年高考化学一轮复习考点通关卷(新高考通用)江西省宜春市宜丰中学2023-2024学年高一下学期4月期中考试化学试题
8 . 某课外学习小组在一些化学实验中都用了碳酸盐。
(1)利用图装置进行Cu与 制取氮氧化物的反应。
制取氮氧化物的反应。
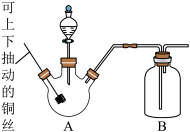
①若利用铜与浓硝酸反应制取并收集 ,为驱赶装置内的空气,可先在三颈烧瓶A中放入少量
,为驱赶装置内的空气,可先在三颈烧瓶A中放入少量___________ 粉末,再滴加浓硝酸。
②若利用该装置制取并收集NO时,则需对集气装置广口瓶B作必要的改动,改动措施是_______ 。
③针对上述实验,以下说法不正确的是___________ 。(填字母)
a.还缺少尾气吸收装置
b.不管是①还是②,每个实验,实验过程中整套装置都至少要组装两次
c.盖上滴液漏斗的玻璃塞,用水封住广口瓶B的长导管口,加热三颈烧瓶A,可以检查装置的气密性
d.在铜丝与橡皮塞之间涂抹少许凡士林,以润滑铜丝和封闭缝隙
(2) 难溶与水。难溶电解质遇到具有不同离子的可溶性强电解质溶液,会使难溶电解质溶解度增大,这种现象叫做“盐效应”。“盐效应”与离子浓度、离子所带电量有关。某小组设计实验探究
难溶与水。难溶电解质遇到具有不同离子的可溶性强电解质溶液,会使难溶电解质溶解度增大,这种现象叫做“盐效应”。“盐效应”与离子浓度、离子所带电量有关。某小组设计实验探究 是否能与
是否能与 形成络离子,分别取等量的
形成络离子,分别取等量的 进行实验,实验结果如图所示:
进行实验,实验结果如图所示:
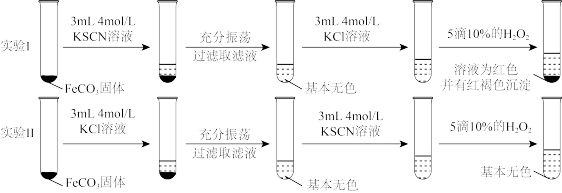
①不考虑 是否能与
是否能与 形成络离子,单就盐效应来讲,相同浓度下,KSCN溶液盐效应
形成络离子,单就盐效应来讲,相同浓度下,KSCN溶液盐效应___________ KCl溶液(填“>”、“=”、“<”)。
②滤液中+2价Fe总浓度:实验I___________ 实验II(填“>”、“=”、“<”)。
③设计实验II,对实验I的帮助作用是___________ 。
(3)常温下苯酚微溶于水,在水中形成乳浊液。苯酚是一种弱酸,常温下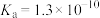 ,相同温度下碳酸
,相同温度下碳酸 ,
,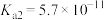 。限用两种药品或试剂(不包括蒸馏水),仪器不限,设计实验证明酸性:
。限用两种药品或试剂(不包括蒸馏水),仪器不限,设计实验证明酸性:
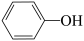 >
> 。
。
(1)利用图装置进行Cu与
 制取氮氧化物的反应。
制取氮氧化物的反应。
①若利用铜与浓硝酸反应制取并收集
 ,为驱赶装置内的空气,可先在三颈烧瓶A中放入少量
,为驱赶装置内的空气,可先在三颈烧瓶A中放入少量②若利用该装置制取并收集NO时,则需对集气装置广口瓶B作必要的改动,改动措施是
③针对上述实验,以下说法不正确的是
a.还缺少尾气吸收装置
b.不管是①还是②,每个实验,实验过程中整套装置都至少要组装两次
c.盖上滴液漏斗的玻璃塞,用水封住广口瓶B的长导管口,加热三颈烧瓶A,可以检查装置的气密性
d.在铜丝与橡皮塞之间涂抹少许凡士林,以润滑铜丝和封闭缝隙
(2)
 难溶与水。难溶电解质遇到具有不同离子的可溶性强电解质溶液,会使难溶电解质溶解度增大,这种现象叫做“盐效应”。“盐效应”与离子浓度、离子所带电量有关。某小组设计实验探究
难溶与水。难溶电解质遇到具有不同离子的可溶性强电解质溶液,会使难溶电解质溶解度增大,这种现象叫做“盐效应”。“盐效应”与离子浓度、离子所带电量有关。某小组设计实验探究 是否能与
是否能与 形成络离子,分别取等量的
形成络离子,分别取等量的 进行实验,实验结果如图所示:
进行实验,实验结果如图所示:
①不考虑
 是否能与
是否能与 形成络离子,单就盐效应来讲,相同浓度下,KSCN溶液盐效应
形成络离子,单就盐效应来讲,相同浓度下,KSCN溶液盐效应②滤液中+2价Fe总浓度:实验I
③设计实验II,对实验I的帮助作用是
(3)常温下苯酚微溶于水,在水中形成乳浊液。苯酚是一种弱酸,常温下
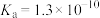 ,相同温度下碳酸
,相同温度下碳酸 ,
,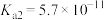 。限用两种药品或试剂(不包括蒸馏水),仪器不限,设计实验证明酸性:
。限用两种药品或试剂(不包括蒸馏水),仪器不限,设计实验证明酸性:
 >
> 。
。| 简要的实验操作 | 实验现象 | 实验结论 |
酸性:  | ||
酸性: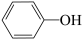 > > |
您最近一年使用:0次
解题方法
9 . 向 固体和200mL 1
固体和200mL 1
 形成的混合后的溶液中通入过量
形成的混合后的溶液中通入过量 ,可观察到有大量白色沉淀,某学习小组为进一步探究该过程中氧化
,可观察到有大量白色沉淀,某学习小组为进一步探究该过程中氧化 的微粒,设计并完成以下步骤:
的微粒,设计并完成以下步骤:
(1)向 固体、100mL 0.02
固体、100mL 0.02 盐酸和100mL 6.0
盐酸和100mL 6.0
 形成的混合液中通过量
形成的混合液中通过量 ,观察到白色沉淀。
,观察到白色沉淀。
(2)向 固体和200mL 1.0
固体和200mL 1.0
 形成的混合液中通过量
形成的混合液中通过量 ,观察到白色沉淀。
,观察到白色沉淀。
(3)取少量步骤(2)反应后的上层清液,滴入0.1
 溶液,观察到蓝色沉淀。
溶液,观察到蓝色沉淀。
已知:1.0
 溶液的pH约为2,不同浓度
溶液的pH约为2,不同浓度 被还原时产物不同,不同pH时
被还原时产物不同,不同pH时 的氧化能力也不同。
的氧化能力也不同。
下列说法不正确的是
 固体和200mL 1
固体和200mL 1
 形成的混合后的溶液中通入过量
形成的混合后的溶液中通入过量 ,可观察到有大量白色沉淀,某学习小组为进一步探究该过程中氧化
,可观察到有大量白色沉淀,某学习小组为进一步探究该过程中氧化 的微粒,设计并完成以下步骤:
的微粒,设计并完成以下步骤:(1)向
 固体、100mL 0.02
固体、100mL 0.02 盐酸和100mL 6.0
盐酸和100mL 6.0
 形成的混合液中通过量
形成的混合液中通过量 ,观察到白色沉淀。
,观察到白色沉淀。(2)向
 固体和200mL 1.0
固体和200mL 1.0
 形成的混合液中通过量
形成的混合液中通过量 ,观察到白色沉淀。
,观察到白色沉淀。(3)取少量步骤(2)反应后的上层清液,滴入0.1

 溶液,观察到蓝色沉淀。
溶液,观察到蓝色沉淀。已知:1.0

 溶液的pH约为2,不同浓度
溶液的pH约为2,不同浓度 被还原时产物不同,不同pH时
被还原时产物不同,不同pH时 的氧化能力也不同。
的氧化能力也不同。下列说法不正确的是
A.步骤(1)说明酸性条件下 能氧化 能氧化 |
B.步骤(2)反应的离子方程式: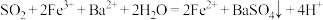 |
C.步骤(2)已证明 能氧化 能氧化 ,因此步骤(3)可舍去 ,因此步骤(3)可舍去 |
D.综合上述步骤,说明题干中 是 是 溶液的 溶液的 和酸性条件下 和酸性条件下 共同氧化的 共同氧化的 |
您最近一年使用:0次
10 . 富硼渣中含有镁硼酸盐(2MgO·B2O3)、镁硅酸盐(2MgO·SiO2)及少量Al2O3、FeO等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸(H3BO3)晶体的一种工艺流程如下:

已知生成相应氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)如下:
(1)酸浸时发生反应:2MgO·SiO2+2H2SO4=2MgSO4+SiO2+2H2O,2MgO·B2O3+2H2SO4=2H3BO3+2MgSO4。
①根据上述反应可知,酸性:H2SO4___________ (填“>”或“<”)H3BO3。
②已知硼酸与过量NaOH溶液发生中和反应的离子方程式为:H3BO3+OH-= 。下列关于硼酸的说法正确的是
。下列关于硼酸的说法正确的是___________ (填字母)
A.硼酸是一元酸
B.向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
C.硼酸的电离方程式可表示为H3BO3+H2O +H+
+H+
(2)检验褐色浸出液中的杂质离子:取少量浸出液,___________ (填操作和现象),证明溶液中含有Fe2+。
(3)除去浸出液中的杂质离子:用MgO调节溶液的pH至___________ 以上,使杂质离子转化为___________ (填化学式)沉淀,过滤。
(4)获取晶体:
ⅰ.浓缩滤液,使MgSO4溶液和H3BO3溶液接近饱和;
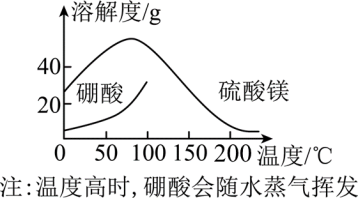
ⅱ.控制温度使两种晶体分别从溶液中结晶。结合图中溶解度曲线,简述ⅱ的方法:将浓缩液加入高压釜中升温结晶得到___________ 晶体,分离后,再将母液降温结晶,分离得到另一种物质的晶体。

已知生成相应氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)如下:
| Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | |
| 开始沉淀时 | 1.9 | 3.4 | 7.0 | 9.1 |
| 完全沉定时 | 3.2 | 4.7 | 9.0 | 11.1 |
①根据上述反应可知,酸性:H2SO4
②已知硼酸与过量NaOH溶液发生中和反应的离子方程式为:H3BO3+OH-=
 。下列关于硼酸的说法正确的是
。下列关于硼酸的说法正确的是A.硼酸是一元酸
B.向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
C.硼酸的电离方程式可表示为H3BO3+H2O
 +H+
+H+(2)检验褐色浸出液中的杂质离子:取少量浸出液,
(3)除去浸出液中的杂质离子:用MgO调节溶液的pH至
(4)获取晶体:
ⅰ.浓缩滤液,使MgSO4溶液和H3BO3溶液接近饱和;
ⅱ.控制温度使两种晶体分别从溶液中结晶。结合图中溶解度曲线,简述ⅱ的方法:将浓缩液加入高压釜中升温结晶得到

您最近一年使用:0次
2023-03-19更新
|
466次组卷
|
5卷引用:重庆市万州第二高级中学2023届高三下学期第二次质量检测化学试题
重庆市万州第二高级中学2023届高三下学期第二次质量检测化学试题(已下线)第八章 水溶液中的离子反应与平衡 第55练 无机化工流程题的解题策略(已下线)05 无机化工流程题(5) (解析)-备战2023年高考化学大题逐空突破系列(全国通用)(已下线)题型38 非金属元素相关的工艺流程山东省枣庄滕州市第二中学2021-2022学年高三上学期第一次质量检测化学试题



