名校
解题方法
1 . 在处理 废气的过程中,催化剂
废气的过程中,催化剂 会逐渐失活变为
会逐渐失活变为 。某小组为解决这一问题,实验研究
。某小组为解决这一问题,实验研究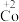 和
和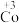 之间的相互转化。资料:
之间的相互转化。资料: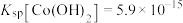 ,
,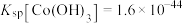
(1)探究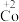 的还原性
的还原性
实验Ⅰ.粉红色的 溶液或
溶液或 溶液在空气中久置,无明显变化。
溶液在空气中久置,无明显变化。
实验Ⅱ.向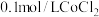 溶液中滴入2滴酸性
溶液中滴入2滴酸性 溶液,无明显变化。
溶液,无明显变化。
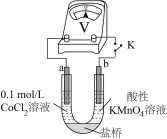
实验Ⅲ.按如图装置进行实验,观察到电压表指针偏转。
①甲同学根据实验Ⅲ得出结论: 可以被酸性
可以被酸性 溶液氧化。
溶液氧化。
乙同学补充实验Ⅳ,___________ (补全实验操作及现象),否定了该观点。
②探究碱性条件下 的还原性,进行实验。
的还原性,进行实验。
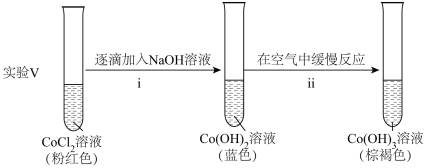
ⅱ中反应的化学方程式是___________ 。
③根据氧化还原反应规律解释:还原性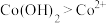 :
: 在碱性条件下,
在碱性条件下, 与
与 、
、 反应,使
反应,使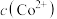 和
和 均降低,但
均降低,但___________ 降低的程度更大,还原剂的还原性增强。
(2)探究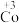 的氧化性
的氧化性
①根据实验Ⅲ和Ⅳ推测氧化性: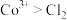 ,设计实验证明:向Ⅴ中得到的棕褐色沉淀中,
,设计实验证明:向Ⅴ中得到的棕褐色沉淀中,___________ (补全实验操作及现象),反应的离子方程式是___________ 。
②向Ⅴ中得到的棕褐色沉淀中滴加 溶液,加入催化剂,产生无色气泡,该气体是
溶液,加入催化剂,产生无色气泡,该气体是___________ 。
(3)利用“三室两膜”装置(如图)实现“电解”制备 。
。
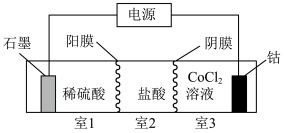
①石墨电极的电极反应式为___________
②生成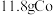 时,室1溶液质量理论上减少
时,室1溶液质量理论上减少___________ g。
 废气的过程中,催化剂
废气的过程中,催化剂 会逐渐失活变为
会逐渐失活变为 。某小组为解决这一问题,实验研究
。某小组为解决这一问题,实验研究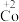 和
和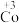 之间的相互转化。资料:
之间的相互转化。资料: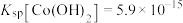 ,
,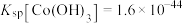
(1)探究
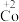 的还原性
的还原性实验Ⅰ.粉红色的
 溶液或
溶液或 溶液在空气中久置,无明显变化。
溶液在空气中久置,无明显变化。实验Ⅱ.向
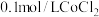 溶液中滴入2滴酸性
溶液中滴入2滴酸性 溶液,无明显变化。
溶液,无明显变化。实验Ⅲ.按如图装置进行实验,观察到电压表指针偏转。

①甲同学根据实验Ⅲ得出结论:
 可以被酸性
可以被酸性 溶液氧化。
溶液氧化。乙同学补充实验Ⅳ,
②探究碱性条件下
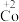 的还原性,进行实验。
的还原性,进行实验。
ⅱ中反应的化学方程式是
③根据氧化还原反应规律解释:还原性
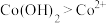 :
: 在碱性条件下,
在碱性条件下, 与
与 、
、 反应,使
反应,使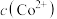 和
和 均降低,但
均降低,但(2)探究
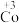 的氧化性
的氧化性①根据实验Ⅲ和Ⅳ推测氧化性:
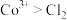 ,设计实验证明:向Ⅴ中得到的棕褐色沉淀中,
,设计实验证明:向Ⅴ中得到的棕褐色沉淀中,②向Ⅴ中得到的棕褐色沉淀中滴加
 溶液,加入催化剂,产生无色气泡,该气体是
溶液,加入催化剂,产生无色气泡,该气体是(3)利用“三室两膜”装置(如图)实现“电解”制备
 。
。
①石墨电极的电极反应式为
②生成
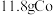 时,室1溶液质量理论上减少
时,室1溶液质量理论上减少
您最近一年使用:0次
名校
解题方法
2 . 某同学欲探究H2O2的氧化还原性:
(1)该同学从化合价的角度分析H2O2既有氧化性又有还原性,探究H2O2的氧化性可以选取的物质是:___________ (填序号)
①淀粉KI溶液(酸性) ②酸性KMnO4溶液 ③Cl2 ④HNO3溶液
任选一个你所选的物质进行实验,观察到___________ 现象,证明H2O2有氧化性,反应的离子方程式为___________ 。
(2)继续探究:
资料:Na2O2+2H2O=2NaOH+H2O2、2H2O2=2H2O+O2↑
①制备H2O2:将Na2O2溶于冰水中,产生少量气泡,得溶液A。
向A中加入过量稀H2SO4,得溶液B。
②检验H2O2:向溶液A、B中分别滴加适量KMnO4溶液。
Ⅰ.B中产生气泡,滴入的溶液紫色褪去。反应的离子方程式为___________ 。
Ⅱ.A中滴入的溶液紫色褪去,有棕褐色固体生成,产生大量气泡。推测固体可能含MnO2,对其产生的原因提出猜想:
猜想1.KMnO4,有氧化性,能被还原为MnO2
猜想2.Mn2+有___________ 性,能与H2O2反应产生MnO2
猜想3……
③探究猜想2的合理性,并分析Ⅰ中没有产生棕褐色固体的原因,设计实验如下:
iii是ii和i的对照实验。
①X是___________ 。
②a是___________ 、b是___________ 。
③取i中棕褐色固体,实验证明是MnO2。
综上所述,H2O2体现氧化性还是还原性与反应对象的性质和溶液的酸碱性有关。
(1)该同学从化合价的角度分析H2O2既有氧化性又有还原性,探究H2O2的氧化性可以选取的物质是:
①淀粉KI溶液(酸性) ②酸性KMnO4溶液 ③Cl2 ④HNO3溶液
任选一个你所选的物质进行实验,观察到
(2)继续探究:
资料:Na2O2+2H2O=2NaOH+H2O2、2H2O2=2H2O+O2↑
①制备H2O2:将Na2O2溶于冰水中,产生少量气泡,得溶液A。
向A中加入过量稀H2SO4,得溶液B。
②检验H2O2:向溶液A、B中分别滴加适量KMnO4溶液。
Ⅰ.B中产生气泡,滴入的溶液紫色褪去。反应的离子方程式为
Ⅱ.A中滴入的溶液紫色褪去,有棕褐色固体生成,产生大量气泡。推测固体可能含MnO2,对其产生的原因提出猜想:
猜想1.KMnO4,有氧化性,能被还原为MnO2
猜想2.Mn2+有
猜想3……
③探究猜想2的合理性,并分析Ⅰ中没有产生棕褐色固体的原因,设计实验如下:
| 序号 | 实验 | 试剂 | 现象 |
| i | 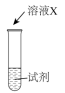 | a | 生成棕褐色固体,产生大量气泡 |
| ii | b | 有少量气泡 | |
| iii | H2O2溶液 | 有少量气泡 |
①X是
②a是
③取i中棕褐色固体,实验证明是MnO2。
综上所述,H2O2体现氧化性还是还原性与反应对象的性质和溶液的酸碱性有关。
您最近一年使用:0次
名校
解题方法
3 . 在处理NO废气的过程中,催化剂 会逐渐失活变为
会逐渐失活变为 。某小组为解决这一问题,实验研究
。某小组为解决这一问题,实验研究 和
和 之间的相互转化。
之间的相互转化。
资料:Ⅰ.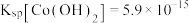

Ⅱ.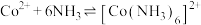
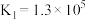
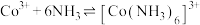
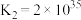
Ⅲ. 和
和 在酸性条件下均能生成
在酸性条件下均能生成
(1)探究 的还原性
的还原性
实验Ⅰ 粉红色的 溶液或
溶液或 溶液在空气中久置,无明显变化。
溶液在空气中久置,无明显变化。
实验Ⅱ 向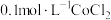 溶液中滴入2滴酸性
溶液中滴入2滴酸性 溶液,无明显变化。
溶液,无明显变化。
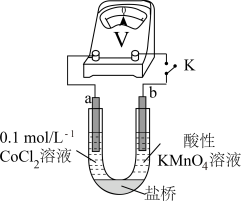
实验Ⅲ 按如图装置进行实验,观察到电压表指针偏转。
①甲同学根据实验Ⅲ得出结论: 能被酸性
能被酸性 溶液氧化。乙同学补充实验Ⅳ,
溶液氧化。乙同学补充实验Ⅳ,_______ (补全实验操作及现象),否定了该观点 。
②探究碱性条件下Co(Ⅱ)的还原性,进行实验。
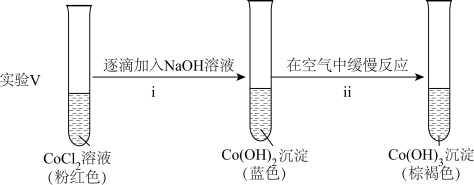
ⅱ中反应的化学方程式是_______ 。
③根据氧化还原反应规律解释还原性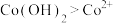 :
: 在碱性条件下,
在碱性条件下, 与
与 、
、 反应,使
反应,使 和
和 均降低,但
均降低,但_______ 降低的程度更大,还原剂的还原性增强。
(2)探究 的氧化性
的氧化性
①根据实验Ⅲ和Ⅳ推测氧化性: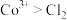 ,设计实验证明:向Ⅴ中得到的棕褐色沉淀中,
,设计实验证明:向Ⅴ中得到的棕褐色沉淀中,_______ (补全实验操作及现象),反应的离子方程式是_______ 。
②向Ⅴ中得到的棕褐色沉淀中,滴加 溶液,加入催化剂,产生无色气泡,该气体是
溶液,加入催化剂,产生无色气泡,该气体是_______ 。
 会逐渐失活变为
会逐渐失活变为 。某小组为解决这一问题,实验研究
。某小组为解决这一问题,实验研究 和
和 之间的相互转化。
之间的相互转化。资料:Ⅰ.
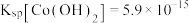

Ⅱ.
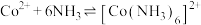
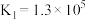
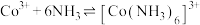
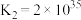
Ⅲ.
 和
和 在酸性条件下均能生成
在酸性条件下均能生成
(1)探究
 的还原性
的还原性实验Ⅰ 粉红色的
 溶液或
溶液或 溶液在空气中久置,无明显变化。
溶液在空气中久置,无明显变化。实验Ⅱ 向
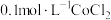 溶液中滴入2滴酸性
溶液中滴入2滴酸性 溶液,无明显变化。
溶液,无明显变化。实验Ⅲ 按如图装置进行实验,观察到电压表指针偏转。

①甲同学根据实验Ⅲ得出结论:
 能被酸性
能被酸性 溶液氧化。乙同学补充实验Ⅳ,
溶液氧化。乙同学补充实验Ⅳ,②探究碱性条件下Co(Ⅱ)的还原性,进行实验。

ⅱ中反应的化学方程式是
③根据氧化还原反应规律解释还原性
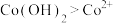 :
: 在碱性条件下,
在碱性条件下, 与
与 、
、 反应,使
反应,使 和
和 均降低,但
均降低,但(2)探究
 的氧化性
的氧化性①根据实验Ⅲ和Ⅳ推测氧化性:
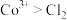 ,设计实验证明:向Ⅴ中得到的棕褐色沉淀中,
,设计实验证明:向Ⅴ中得到的棕褐色沉淀中,②向Ⅴ中得到的棕褐色沉淀中,滴加
 溶液,加入催化剂,产生无色气泡,该气体是
溶液,加入催化剂,产生无色气泡,该气体是
您最近一年使用:0次
名校
4 . 某小组探究含Cr元素的化合物间的转化,进行如下实验。
资料:
i.含Cr元素的常见粒子: (橙色)、
(橙色)、 (黄色)、CrO5(溶于水,蓝紫色,不稳定)、Cr3+(绿色)、Cr(OH)3(蓝灰色,难溶于水,可溶于强酸、强碱)、
(黄色)、CrO5(溶于水,蓝紫色,不稳定)、Cr3+(绿色)、Cr(OH)3(蓝灰色,难溶于水,可溶于强酸、强碱)、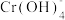 (亮绿色)。
(亮绿色)。
ii.H2O2在碱性环境中比在酸性环境中分解速率快。
iii.在碱性环境中,O2不能氧化+3价铬元素。
实验操作及现象如表:
(1)已知 (橙色)+H2O
(橙色)+H2O 2
2 (黄色)+2H+。请用化学平衡移动原理解释I中滴入稀硫酸后溶液橙色加深的原因:
(黄色)+2H+。请用化学平衡移动原理解释I中滴入稀硫酸后溶液橙色加深的原因:_____ 。
(2)I中,溶液由橙色变为绿色的总反应的离子方程式是_____ 。
(3)Ⅱ中,继续滴入NaOH溶液后,又有气泡生成的原因是_____ 。
(4)Ⅱ中,继续滴入NaOH溶液后,预测有Cr(OH)3沉淀生成,但实验时未观察到。
提出假设:在碱性环境中,+3价铬元素被H2O2氧化。
①甲同学设计实验证明假设成立:
取少量I中的绿色溶液,在滴入NaOH溶液前增加一步操作:______ 。然后滴入NaOH溶液,有蓝灰色沉淀生成,继续滴入NaOH溶液,沉淀溶解,溶液变为______ 色。
②乙同学进一步研究碱性环境对+3价铬元素的还原性或H2O2的氧化性的影响,设计如图实验。
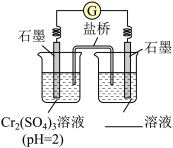
右侧烧杯的溶液中,氧化剂是_____ 。
开始时灵敏电流计指针不偏转,分别继续进行如下实验。
i.向左侧烧杯中滴入NaOH溶液,出现蓝灰色沉淀,继续缓慢滴入NaOH溶液,灵敏电流计指针向右偏转(电子从左向右运动),此时左侧的电极反应式为_____ 。
ii.向右侧烧杯中滴入NaOH溶液,有微小气泡生成,灵敏电流计指针向左偏转,左侧无明显变化。此时原电池中的总反应的化学方程式为_____ 。
(5)由上述实验, 与H2O2、
与H2O2、 与H2O2的氧化性强弱(填“>”或“<”):
与H2O2的氧化性强弱(填“>”或“<”):
酸性条件下,
_____ H2O2;碱性条件下, 
_____ H2O2。
资料:
i.含Cr元素的常见粒子:
 (橙色)、
(橙色)、 (黄色)、CrO5(溶于水,蓝紫色,不稳定)、Cr3+(绿色)、Cr(OH)3(蓝灰色,难溶于水,可溶于强酸、强碱)、
(黄色)、CrO5(溶于水,蓝紫色,不稳定)、Cr3+(绿色)、Cr(OH)3(蓝灰色,难溶于水,可溶于强酸、强碱)、 (亮绿色)。
(亮绿色)。ii.H2O2在碱性环境中比在酸性环境中分解速率快。
iii.在碱性环境中,O2不能氧化+3价铬元素。
实验操作及现象如表:
| 装置 | 步骤 | 操作 | 现象 |
 2mL0.0125mol•L-1K2Cr2O7溶液 | I | 先滴入稀硫酸至pH≈2,再滴入5滴5%H2O2溶液,振荡 | 溶液橙色加深。滴入H2O2溶液后迅速变为蓝紫色,有气泡生成。稍后,无明显气泡时,溶液由蓝紫色完全变为绿色 |
| Ⅱ | 继续缓慢滴入10滴2mol•L-1NaOH溶液,边滴,边振荡 | 又有气泡生成,溶液最终变为黄色 |
 (橙色)+H2O
(橙色)+H2O 2
2 (黄色)+2H+。请用化学平衡移动原理解释I中滴入稀硫酸后溶液橙色加深的原因:
(黄色)+2H+。请用化学平衡移动原理解释I中滴入稀硫酸后溶液橙色加深的原因:(2)I中,溶液由橙色变为绿色的总反应的离子方程式是
(3)Ⅱ中,继续滴入NaOH溶液后,又有气泡生成的原因是
(4)Ⅱ中,继续滴入NaOH溶液后,预测有Cr(OH)3沉淀生成,但实验时未观察到。
提出假设:在碱性环境中,+3价铬元素被H2O2氧化。
①甲同学设计实验证明假设成立:
取少量I中的绿色溶液,在滴入NaOH溶液前增加一步操作:
②乙同学进一步研究碱性环境对+3价铬元素的还原性或H2O2的氧化性的影响,设计如图实验。

右侧烧杯的溶液中,氧化剂是
开始时灵敏电流计指针不偏转,分别继续进行如下实验。
i.向左侧烧杯中滴入NaOH溶液,出现蓝灰色沉淀,继续缓慢滴入NaOH溶液,灵敏电流计指针向右偏转(电子从左向右运动),此时左侧的电极反应式为
ii.向右侧烧杯中滴入NaOH溶液,有微小气泡生成,灵敏电流计指针向左偏转,左侧无明显变化。此时原电池中的总反应的化学方程式为
(5)由上述实验,
 与H2O2、
与H2O2、 与H2O2的氧化性强弱(填“>”或“<”):
与H2O2的氧化性强弱(填“>”或“<”):酸性条件下,


您最近一年使用:0次
2023-01-07更新
|
425次组卷
|
4卷引用:北京市西城区2022-2023学年高二上学期1月期末考试化学试题
5 . 亚硝酸钠(NaNO2)常用作肉类食品的防腐剂。某实验小组将NO和NO2的混合气体通入Na2CO3溶液中,并经一系列操作制得NaNO2固体,然后对其性质进行探究。
【查阅资料】
①NaNO2具有较强的氧化性和较弱的还原性,其水溶液显碱性。
② 与Ag+反应,可生成AgNO2白色沉淀或无色配离子。
与Ag+反应,可生成AgNO2白色沉淀或无色配离子。
【性质探究】将制取的NaNO2固体配制成约0.1mol/L NaNO2溶液,进行实验I和实验II。
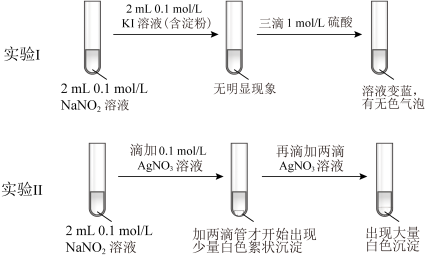
请回答下列问题:
(1)NaNO2溶液显碱性的原因是_______ (用离子方程式表示)。
(2)根据实验I,推测酸性条件下 氧化I- 的离子方程式是
氧化I- 的离子方程式是_______ 。
(3)甲同学认为依据实验I的现象可以得出结论:该条件下 能氧化I-。乙同学则认为制取的NaNO2含有副产物,仅凭实验I不能得出上述结论,还需要进行补充实验。乙同学设计实验III证明了实验I条件下氧化I- 的只有
能氧化I-。乙同学则认为制取的NaNO2含有副产物,仅凭实验I不能得出上述结论,还需要进行补充实验。乙同学设计实验III证明了实验I条件下氧化I- 的只有 。请补充完整实验III的实验方案:取2mL 0.1mol/L
。请补充完整实验III的实验方案:取2mL 0.1mol/L_______ 溶液于试管中,加入_______ ,溶液没有变蓝。
(4)①由实验II的现象得出结论:白色沉淀的生成与_______ 有关。
②仅用实验II的试剂,设计实验方案进一步证实了上述结论,实验操作及现象是_______ 。
(5)常温下AgNO2微溶于水,在沸水中可溶。除去AgNO2沉淀中的少量Ag2O杂质的方法如下:加入适量水,加热溶解,_______ ,过滤,洗涤,干燥。
【查阅资料】
①NaNO2具有较强的氧化性和较弱的还原性,其水溶液显碱性。
②
 与Ag+反应,可生成AgNO2白色沉淀或无色配离子。
与Ag+反应,可生成AgNO2白色沉淀或无色配离子。【性质探究】将制取的NaNO2固体配制成约0.1mol/L NaNO2溶液,进行实验I和实验II。

请回答下列问题:
(1)NaNO2溶液显碱性的原因是
(2)根据实验I,推测酸性条件下
 氧化I- 的离子方程式是
氧化I- 的离子方程式是(3)甲同学认为依据实验I的现象可以得出结论:该条件下
 能氧化I-。乙同学则认为制取的NaNO2含有副产物,仅凭实验I不能得出上述结论,还需要进行补充实验。乙同学设计实验III证明了实验I条件下氧化I- 的只有
能氧化I-。乙同学则认为制取的NaNO2含有副产物,仅凭实验I不能得出上述结论,还需要进行补充实验。乙同学设计实验III证明了实验I条件下氧化I- 的只有 。请补充完整实验III的实验方案:取2mL 0.1mol/L
。请补充完整实验III的实验方案:取2mL 0.1mol/L(4)①由实验II的现象得出结论:白色沉淀的生成与
②仅用实验II的试剂,设计实验方案进一步证实了上述结论,实验操作及现象是
(5)常温下AgNO2微溶于水,在沸水中可溶。除去AgNO2沉淀中的少量Ag2O杂质的方法如下:加入适量水,加热溶解,
您最近一年使用:0次
2022-10-21更新
|
204次组卷
|
2卷引用:广东省梅州市丰顺县丰顺中学2022-2023学年高三上学期1月期末考试化学试题
名校
解题方法
6 . 在处理NO废气的过程中,催化剂[Co(NH3)6]2+会逐渐失活变为[Co(NH3)6]3+。某小组为解决这一问题,实验研究 和
和 之间的相互转化。
之间的相互转化。
资料:i.Ksp[Co(OH)2]=5.9×10-15,Ksp[Co(OH)3]=1.6×10-44
ii.Co2++6NH3 [Co(NH3)6]2+K1=1.3×105
[Co(NH3)6]2+K1=1.3×105
Co3++6NH3 [Co(NH3)6]3+K2=2×1035
[Co(NH3)6]3+K2=2×1035
iii.[Co(NH3)6]2+和[Co(NH3)6]3+在酸性条件下均能生成NH
(1)探究 的还原性
的还原性
实验I.粉红色的CoCl2溶液或CoSO4溶液在空气中久置,无明显变化。
实验II.向0.1mol/LCoCl2溶液中滴入2滴酸性KMnO4溶液,无明显变化。
实验III.按如图装置进行实验,观察到电压表指针偏转。
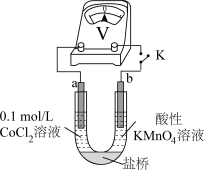
①甲同学根据实验III得出结论:Co2+可以被酸性KMnO4溶液氧化。
乙同学补充实验IV,____ (补全实验操作及现象),否定了该观点。
②探究碱性条件下 的还原性,进行实验。
的还原性,进行实验。
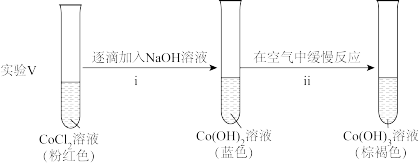
ii中反应的化学方程式是____ 。
③根据氧化还原反应规律解释:还原性Co(OH)2>Co2+:Co2+-e-=Co3+在碱性条件下,OH-与Co2+、Co3+反应,使c(Co2+)和c(Co3+)均降低,但____ 降低的程度更大,还原剂的还原性增强。
(2)探究 的氧化性
的氧化性
①根据实验III和IV推测氧化性:Co3+>Cl2,设计实验证明:向V中得到的棕褐色沉淀中,____ (补全实验操作及现象),反应的离子方程式是____ 。
②向V中得到的棕褐色沉淀中滴加H2SO4溶液,加入催化剂,产生无色气泡,该气体是____ 。
(3)催化剂[Co(NH3)6]2+的失活与再生
①结合数据解释[Co(NH3)6]2+能被氧化为[Co(NH3)6]3+而失活的原因:____ 。
②根据以上实验,设计物质转化流程图实现[Co(NH3)6]2+的再生:____ 。
示例:Co CoCl2
CoCl2 Co(OH)2
Co(OH)2
 和
和 之间的相互转化。
之间的相互转化。资料:i.Ksp[Co(OH)2]=5.9×10-15,Ksp[Co(OH)3]=1.6×10-44
ii.Co2++6NH3
 [Co(NH3)6]2+K1=1.3×105
[Co(NH3)6]2+K1=1.3×105Co3++6NH3
 [Co(NH3)6]3+K2=2×1035
[Co(NH3)6]3+K2=2×1035iii.[Co(NH3)6]2+和[Co(NH3)6]3+在酸性条件下均能生成NH

(1)探究
 的还原性
的还原性实验I.粉红色的CoCl2溶液或CoSO4溶液在空气中久置,无明显变化。
实验II.向0.1mol/LCoCl2溶液中滴入2滴酸性KMnO4溶液,无明显变化。
实验III.按如图装置进行实验,观察到电压表指针偏转。

①甲同学根据实验III得出结论:Co2+可以被酸性KMnO4溶液氧化。
乙同学补充实验IV,
②探究碱性条件下
 的还原性,进行实验。
的还原性,进行实验。
ii中反应的化学方程式是
③根据氧化还原反应规律解释:还原性Co(OH)2>Co2+:Co2+-e-=Co3+在碱性条件下,OH-与Co2+、Co3+反应,使c(Co2+)和c(Co3+)均降低,但
(2)探究
 的氧化性
的氧化性①根据实验III和IV推测氧化性:Co3+>Cl2,设计实验证明:向V中得到的棕褐色沉淀中,
②向V中得到的棕褐色沉淀中滴加H2SO4溶液,加入催化剂,产生无色气泡,该气体是
(3)催化剂[Co(NH3)6]2+的失活与再生
①结合数据解释[Co(NH3)6]2+能被氧化为[Co(NH3)6]3+而失活的原因:
②根据以上实验,设计物质转化流程图实现[Co(NH3)6]2+的再生:
示例:Co
 CoCl2
CoCl2 Co(OH)2
Co(OH)2
您最近一年使用:0次
2022-05-08更新
|
1412次组卷
|
9卷引用:热点1物质性质探究类实验
名校
7 . 化学是一门以实验为基础的学科,物质的分离提纯、检验鉴别、生产制备都可通过合适的实验方案实现。回答下列问题:
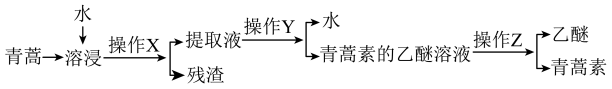
(1)乙醚是一种用途很广的有机溶剂。从青蒿中提取青蒿素的一种实验过程如下图所示,操作Y的名称为__________ 。
(2)纯净干燥的氯气与熔融金属锡反应可制备 ,某化学小组的同学设计了如下实验装置进行制备。
,某化学小组的同学设计了如下实验装置进行制备。
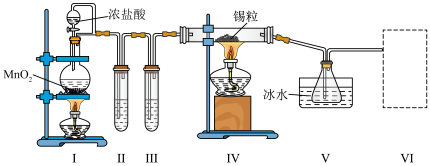
已知:i.金属锡熔点为 ,化学活泼性与铁相似;
,化学活泼性与铁相似;
ii. 的沸点为
的沸点为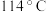 ,且易与水反应。
,且易与水反应。
请根据上图装置回答:
①装置V中发生反应的化学方程式为____________________ 。
②试管Ⅱ中的试剂是____________________ ;
装置V的作用是______________________________ 。
③装置Ⅵ最好 选用下列装置中的__________ (填标号)。
A.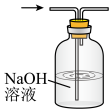 B.
B.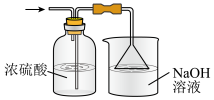 C.
C.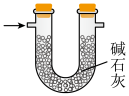
④为了顺利完成实验,点燃酒精灯的正确操作是__________ (填字母)。
A.先点燃I处酒精灯,后点燃IV处酒精灯
B.先点燃IV处酒精灯,后点燃I处酒精灯
C.同时点燃I、IV两处酒精灯
(3)某同学探究不同条件下 与二价锰化合物的反应,实验装置如下图所示:
与二价锰化合物的反应,实验装置如下图所示:
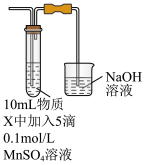
查阅资料显示:
a. 在一定条件下能被
在一定条件下能被 或
或 氧化成
氧化成 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。
b.浓碱条件下, 可被
可被 还原为
还原为 。
。
c. 的氧化性与溶液的酸碱性无关,
的氧化性与溶液的酸碱性无关, 的氧化性随碱性增强而减弱。
的氧化性随碱性增强而减弱。
①通入 前,Ⅱ、Ⅲ中白色沉淀
前,Ⅱ、Ⅲ中白色沉淀 变为棕黑色沉淀
变为棕黑色沉淀 。
。
②对比实验I、Ⅱ通入 后的实验现象,对于
后的实验现象,对于 还原性与溶液酸碱性的认识是
还原性与溶液酸碱性的认识是__________ 。
③据资料b,Ⅲ中应得到绿色溶液,而实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入 导致溶液的碱性减弱。
导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将 氧化为
氧化为 。
。
i.用化学方程式表示可能导致溶液碱性减弱的原因:____________________ 。
ii.取中放置后的 悬浊液,加入
悬浊液,加入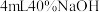 溶液,观察到溶液紫色迅速变为绿色,且有无色无味气体产生,该气体的化学式为
溶液,观察到溶液紫色迅速变为绿色,且有无色无味气体产生,该气体的化学式为__________ ;同时还可观察到溶液的绿色缓慢加深,即可证明Ⅲ的悬浊液中氧化剂过量。

(1)乙醚是一种用途很广的有机溶剂。从青蒿中提取青蒿素的一种实验过程如下图所示,操作Y的名称为
(2)纯净干燥的氯气与熔融金属锡反应可制备
 ,某化学小组的同学设计了如下实验装置进行制备。
,某化学小组的同学设计了如下实验装置进行制备。
已知:i.金属锡熔点为
 ,化学活泼性与铁相似;
,化学活泼性与铁相似;ii.
 的沸点为
的沸点为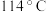 ,且易与水反应。
,且易与水反应。请根据上图装置回答:
①装置V中发生反应的化学方程式为
②试管Ⅱ中的试剂是
装置V的作用是
③装置Ⅵ
A.
 B.
B. C.
C.
④为了顺利完成实验,点燃酒精灯的正确操作是
A.先点燃I处酒精灯,后点燃IV处酒精灯
B.先点燃IV处酒精灯,后点燃I处酒精灯
C.同时点燃I、IV两处酒精灯
(3)某同学探究不同条件下
 与二价锰化合物的反应,实验装置如下图所示:
与二价锰化合物的反应,实验装置如下图所示:
查阅资料显示:
a.
 在一定条件下能被
在一定条件下能被 或
或 氧化成
氧化成 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。b.浓碱条件下,
 可被
可被 还原为
还原为 。
。c.
 的氧化性与溶液的酸碱性无关,
的氧化性与溶液的酸碱性无关, 的氧化性随碱性增强而减弱。
的氧化性随碱性增强而减弱。序号 | 物质X | C中实验现象 | |
通入 | 通入 | ||
I | 水 | 得到无色溶液 | 产生棕黑色沉淀,且放置后不发生变化 |
II |
| 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
III |
| 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
 前,Ⅱ、Ⅲ中白色沉淀
前,Ⅱ、Ⅲ中白色沉淀 变为棕黑色沉淀
变为棕黑色沉淀 。
。②对比实验I、Ⅱ通入
 后的实验现象,对于
后的实验现象,对于 还原性与溶液酸碱性的认识是
还原性与溶液酸碱性的认识是③据资料b,Ⅲ中应得到绿色溶液,而实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入
 导致溶液的碱性减弱。
导致溶液的碱性减弱。原因二:可能是氧化剂过量,氧化剂将
 氧化为
氧化为 。
。i.用化学方程式表示可能导致溶液碱性减弱的原因:
ii.取中放置后的
 悬浊液,加入
悬浊液,加入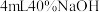 溶液,观察到溶液紫色迅速变为绿色,且有无色无味气体产生,该气体的化学式为
溶液,观察到溶液紫色迅速变为绿色,且有无色无味气体产生,该气体的化学式为
您最近一年使用:0次
名校
解题方法
8 . 某同学欲探究 的氧化还原性:
的氧化还原性:
资料: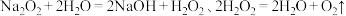
制备 :将
:将 溶于冰水中,产生少量气泡,得溶液A。将溶液A分为两份,向其中一份中加入过量稀
溶于冰水中,产生少量气泡,得溶液A。将溶液A分为两份,向其中一份中加入过量稀 ,得溶液B。
,得溶液B。
检验 :向溶液A、B中分别滴加适量
:向溶液A、B中分别滴加适量 溶液。
溶液。
I.B中产生气泡,滴入的溶液紫色褪去。
(1)反应的离子方程式为___________ 。
Ⅱ.A中滴入的溶液紫色褪去,有棕褐色固体生成,产生大量气泡。推测固体可能含 ,对其产生的原因提出猜想:
,对其产生的原因提出猜想:
(2)猜想1. 有氧化性,能被还原为
有氧化性,能被还原为
猜想2. 有
有___________ 性,能与 反应产生
反应产生
猜想3……
(3)探究猜想2的合理性,并分析Ⅰ中没有产生棕褐色固体的原因,设计实验如下:
iii是ii和i的对照实验。
①X是___________ 。
②a是___________ 、b是___________ 。
③取i中棕褐色固体,实验证明是 。
。
综上所述, 体现氧化性还是还原性与反应的对象和溶液的酸碱性有关。
体现氧化性还是还原性与反应的对象和溶液的酸碱性有关。
 的氧化还原性:
的氧化还原性:资料:
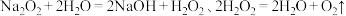
制备
 :将
:将 溶于冰水中,产生少量气泡,得溶液A。将溶液A分为两份,向其中一份中加入过量稀
溶于冰水中,产生少量气泡,得溶液A。将溶液A分为两份,向其中一份中加入过量稀 ,得溶液B。
,得溶液B。检验
 :向溶液A、B中分别滴加适量
:向溶液A、B中分别滴加适量 溶液。
溶液。I.B中产生气泡,滴入的溶液紫色褪去。
(1)反应的离子方程式为
Ⅱ.A中滴入的溶液紫色褪去,有棕褐色固体生成,产生大量气泡。推测固体可能含
 ,对其产生的原因提出猜想:
,对其产生的原因提出猜想:(2)猜想1.
 有氧化性,能被还原为
有氧化性,能被还原为
猜想2.
 有
有 反应产生
反应产生
猜想3……
(3)探究猜想2的合理性,并分析Ⅰ中没有产生棕褐色固体的原因,设计实验如下:
| 序号 | 实验 | 试剂 | 现象 |
| i |  | a | 生成棕褐色固体,产生大量气泡 |
| ii | b | 有少量气泡 | |
| iii |  溶液 溶液 | 有少量气泡 |
①X是
②a是
③取i中棕褐色固体,实验证明是
 。
。综上所述,
 体现氧化性还是还原性与反应的对象和溶液的酸碱性有关。
体现氧化性还是还原性与反应的对象和溶液的酸碱性有关。
您最近一年使用:0次
9 . 某同学欲探究H2O2的氧化还原性:
(1)该同学从化合价的角度分析H2O2既有氧化性又有还原性,其原因是___________ 。
(2)探究H2O2的氧化性可以选取的物质是:___________ (填序号)
①淀粉KI溶液 ②FeSO4溶液 ③Cl2④HNO3溶液
任选一个你所选的物质进行实验,观察到___________ 现象,证明H2O2有氧化性,反应的离子方程式为___________ 。
(3)继续探究:
资料:Na2O2+2H2O=2NaOH+H2O2、2H2O2=2H2O+O2↑
①制备H2O2:将Na2O2溶于冰水中,产生少量气泡,得溶液A。
向A中加入过量稀H2SO4,得溶液B。
②检验H2O2:向溶液A、B中分别滴加适量KMnO4溶液。
Ⅰ.B中产生气泡,滴入的溶液紫色褪去。
反应的离子方程式为___________ 。
Ⅱ.A中滴入的溶液紫色褪去,有棕褐色固体生成,产生大量气泡。推测固体可能含MnO2,对其产生的原因提出猜想:
猜想1.KMnO4,有氧化性,能被还原为MnO2
猜想2.Mn2+有___________ 性,能与H2O2反应产生MnO2
猜想3……
③探究猜想2的合理性,并分析Ⅰ中没有产生棕褐色固体的原因,设计实验如下:
iii是ii和i的对照实验。
①X是___________ 。
②a是___________ 、b是___________ 。
③取i中棕褐色固体,实验证明是MnO2。
综上所述,H2O2体现氧化性还是还原性与反应对象的性质和溶液的酸碱性有关。
(1)该同学从化合价的角度分析H2O2既有氧化性又有还原性,其原因是
(2)探究H2O2的氧化性可以选取的物质是:
①淀粉KI溶液 ②FeSO4溶液 ③Cl2④HNO3溶液
任选一个你所选的物质进行实验,观察到
(3)继续探究:
资料:Na2O2+2H2O=2NaOH+H2O2、2H2O2=2H2O+O2↑
①制备H2O2:将Na2O2溶于冰水中,产生少量气泡,得溶液A。
向A中加入过量稀H2SO4,得溶液B。
②检验H2O2:向溶液A、B中分别滴加适量KMnO4溶液。
Ⅰ.B中产生气泡,滴入的溶液紫色褪去。
反应的离子方程式为
Ⅱ.A中滴入的溶液紫色褪去,有棕褐色固体生成,产生大量气泡。推测固体可能含MnO2,对其产生的原因提出猜想:
猜想1.KMnO4,有氧化性,能被还原为MnO2
猜想2.Mn2+有
猜想3……
③探究猜想2的合理性,并分析Ⅰ中没有产生棕褐色固体的原因,设计实验如下:
| 序号 | 实验 | 试剂 | 现象 |
| i | 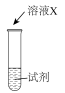 | a | 生成棕褐色固体,产生大量气泡 |
| ii | b | 有少量气泡 | |
| iii | H2O2溶液 | 有少量气泡 |
①X是
②a是
③取i中棕褐色固体,实验证明是MnO2。
综上所述,H2O2体现氧化性还是还原性与反应对象的性质和溶液的酸碱性有关。
您最近一年使用:0次
解题方法
10 . 过氧化氢水溶液是医药、卫生行业上广泛使用的消毒剂。某兴趣小组对过氧化氢(H2O2)氧化性和还原性开展如下探究。
【查阅资料】
①BaO2与稀硫酸反应可制得H2O2,反应的化学方程式为BaO2+H2SO4=BaSO4↓+H2O2。
②H2O2在常温下会缓慢分解成水和氧气,在加热或MnO2等催化剂作用下会迅速分解。
③H2O2在碱性条件下能与Mn2+反应生成棕褐色固体,产生大量气泡。
【实验探究】
(1)制备H2O2:将BaO2溶于足量的冷稀硫酸中充分反应,经_____ (填操作名称)得到含H2O2的溶液A。
(2)检验H2O2:取一定量的溶液A于试管中,加入少量MnO2,迅速产生大量气泡,检验该气体的方法是_____ 。
(3)探究H2O2的氧化性和还原性:
I.向一定量的KMnO4溶液中滴加溶液A,产生气泡,溶液紫色褪去。反应的化学方程式为2KMnO4+5H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O,其中H2O2作_____ 剂。
Ⅱ.向一定量的FeSO4溶液中滴加溶液A,溶液变为棕黄色,此反应的离子方程式为_____ ,其中H2O2作_____ 剂。
Ⅲ.该小组设计如表实验探究H2O2与Mn2+的反应。
①设计实验i的目的是_____ 。
②试剂a应选_____ 。
A.NaCl B.HCl C.NaOH D.KNO3
③取ii中生成的棕褐色固体,滴加浓盐酸,加热,产生黄绿色气体,应选用的气体发生装置是_____ (填序号)。_____ 性等因素有关。
【查阅资料】
①BaO2与稀硫酸反应可制得H2O2,反应的化学方程式为BaO2+H2SO4=BaSO4↓+H2O2。
②H2O2在常温下会缓慢分解成水和氧气,在加热或MnO2等催化剂作用下会迅速分解。
③H2O2在碱性条件下能与Mn2+反应生成棕褐色固体,产生大量气泡。
【实验探究】
(1)制备H2O2:将BaO2溶于足量的冷稀硫酸中充分反应,经
(2)检验H2O2:取一定量的溶液A于试管中,加入少量MnO2,迅速产生大量气泡,检验该气体的方法是
(3)探究H2O2的氧化性和还原性:
I.向一定量的KMnO4溶液中滴加溶液A,产生气泡,溶液紫色褪去。反应的化学方程式为2KMnO4+5H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O,其中H2O2作
Ⅱ.向一定量的FeSO4溶液中滴加溶液A,溶液变为棕黄色,此反应的离子方程式为
Ⅲ.该小组设计如表实验探究H2O2与Mn2+的反应。
| 序号 | 实验 | 溶液 | 现象 |
| i |
| H2O2 | 有少量气泡 |
| ii | H2O2+H2SO4 | 有少量气泡 | |
| iii | H2O2+a | 生成棕褐色固体,产生大量气泡 |
②试剂a应选
A.NaCl B.HCl C.NaOH D.KNO3
③取ii中生成的棕褐色固体,滴加浓盐酸,加热,产生黄绿色气体,应选用的气体发生装置是
A. B.
B.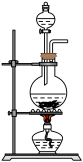 C.
C.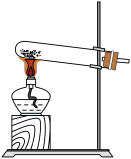 D.
D.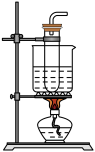
您最近一年使用:0次

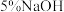 溶液
溶液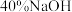 溶液
溶液