1 . 空气湿度增大,水汽凝结就易形成雾,灰尘、硫酸、硝酸、有机碳氢化合物等颗粒物的浓度增大就易形成霾。下列说法不正确的是
| A.防雾霾口罩的原理与过滤类似,防雾霾效果好的口罩往往呼吸阻力较大 |
| B.PM2.5是直径小于或等于2.5微米的污染物颗粒,属于胶体粒子的直径范围 |
| C.汽车车灯在雾霾天照出“通路”的现象属于丁达尔效应 |
| D.可通过在燃煤烟囱上加装高压静电装置除去煤灰中的固体颗粒物 |
您最近一年使用:0次
名校
2 . 已知将亚硫酸钠滴入含淀粉的碘水中,碘水中的蓝色褪为无色,溶液无沉淀生成。某无色溶液中可能含有 、
、 、
、 、
、 ,向该溶液中加入少量溴水,溶液仍呈无色,则有关该无色溶液下列判断正确的是
,向该溶液中加入少量溴水,溶液仍呈无色,则有关该无色溶液下列判断正确的是
 、
、 、
、 、
、 ,向该溶液中加入少量溴水,溶液仍呈无色,则有关该无色溶液下列判断正确的是
,向该溶液中加入少量溴水,溶液仍呈无色,则有关该无色溶液下列判断正确的是A.氧化性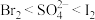 | B.一定不含有 |
C.一定含有 | D.可能含有 |
您最近一年使用:0次
名校
解题方法
3 . Mo、Co及其化合物在催化、颜料等领域有重要用途。以 为载体的钴钼废催化剂中含CoS、
为载体的钴钼废催化剂中含CoS、 及少量含Fe、Ca等元素的物质,经处理可制取
及少量含Fe、Ca等元素的物质,经处理可制取 、高纯钼,工艺流程如图所示:
、高纯钼,工艺流程如图所示:
i.“焙烧”后各元素均转化为相应氧化物,“酸浸”后钼元素转化为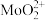 。
。
ii.常温下, ,相关物质的溶度积常数如下表:
,相关物质的溶度积常数如下表:
回答下列问题:
(1)操作2的名称为___________ 。
(2)“焙烧”过程中采用多层逆流(空气从炉底进入,固体粉末从炉顶进入)方式,该操作的优点为___________ ; 在空气中焙烧的化学方程式为
在空气中焙烧的化学方程式为___________ 。
(3)“滤渣1”的主要成分为___________ ;“调pH””的目的是沉淀铁和铝,当溶液中离子浓 时;可认为沉淀完全,若滤液中
时;可认为沉淀完全,若滤液中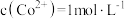 ,则“调pH”的合理范围为
,则“调pH”的合理范围为___________ (已知: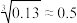 ,
, )。
)。
(4)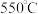 时,在还原炉中
时,在还原炉中 可将
可将 先还原为
先还原为 ,然后再将
,然后再将 还原为金属Mo,写出
还原为金属Mo,写出 还原
还原 生成
生成 的化学方程式:
的化学方程式:___________ ;在元素周期表中,Mo与Cr属于同族相邻元素,其价电子排布方式类似,写出基态Mo原子的价电子排布式:___________ 。
(5)“沉钴”过程中为防止 转化为
转化为 ,需控制溶液的酸碱度,转化过程存在平衡
,需控制溶液的酸碱度,转化过程存在平衡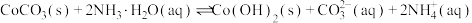 ,该反应的平衡常数
,该反应的平衡常数
___________ 。
 为载体的钴钼废催化剂中含CoS、
为载体的钴钼废催化剂中含CoS、 及少量含Fe、Ca等元素的物质,经处理可制取
及少量含Fe、Ca等元素的物质,经处理可制取 、高纯钼,工艺流程如图所示:
、高纯钼,工艺流程如图所示: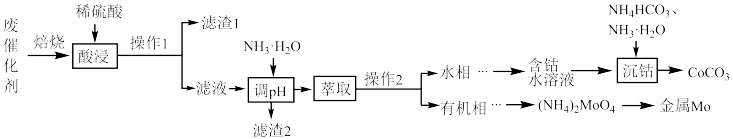
i.“焙烧”后各元素均转化为相应氧化物,“酸浸”后钼元素转化为
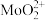 。
。ii.常温下,
 ,相关物质的溶度积常数如下表:
,相关物质的溶度积常数如下表:| 物质 |  |  |  |  |
 | 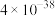 | 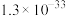 | 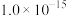 | 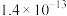 |
(1)操作2的名称为
(2)“焙烧”过程中采用多层逆流(空气从炉底进入,固体粉末从炉顶进入)方式,该操作的优点为
 在空气中焙烧的化学方程式为
在空气中焙烧的化学方程式为(3)“滤渣1”的主要成分为
 时;可认为沉淀完全,若滤液中
时;可认为沉淀完全,若滤液中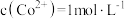 ,则“调pH”的合理范围为
,则“调pH”的合理范围为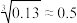 ,
, )。
)。(4)
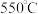 时,在还原炉中
时,在还原炉中 可将
可将 先还原为
先还原为 ,然后再将
,然后再将 还原为金属Mo,写出
还原为金属Mo,写出 还原
还原 生成
生成 的化学方程式:
的化学方程式:(5)“沉钴”过程中为防止
 转化为
转化为 ,需控制溶液的酸碱度,转化过程存在平衡
,需控制溶液的酸碱度,转化过程存在平衡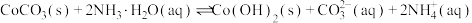 ,该反应的平衡常数
,该反应的平衡常数
您最近一年使用:0次
名校
4 . 阿伏加德罗常数的值用NA表示。下列说法中正确的是
| A.常温常压下,11.2 L SO2含有的氧原子数大于NA |
| B.0.1 mol Na2O2和Na2O的混合物中含有的离子总数等于0.3NA |
| C.10 g质量分数为98%的浓硫酸含有的氢原子数为0.2NA |
| D.一定条件下,Ca与O2反应生成7.2 g CaO2,转移电子的个数为0.4NA |
您最近一年使用:0次
名校
解题方法
5 . 对于超分子聚合物和材料的组装而言,B—N配位键的动态性质和易于调节的特性起着重要作用。某种超分子的结构如图。下列叙述错误的是
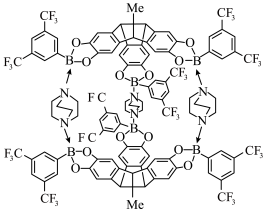
| A.该超分子中涉及的元素均为p区元素 |
| B.第一电离能:F>N>O>C>B |
| C.超分子具有分子识别和自组装的特征 |
| D.该超分子形成的B—N配位键中,N原子提供孤电子对 |
您最近一年使用:0次
名校
解题方法
6 . 某含铜催化剂的阴离子的结构如图所示。W、X、Y、Z是原子序数依次增大的短周期元素,其中X、Y、Z位于同一周期,基态X原子的价电子排布式为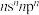 。下列说法错误的是
。下列说法错误的是
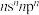 。下列说法错误的是
。下列说法错误的是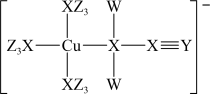
| A.电负性:Z>Y>X>W | B.X、Y、Z均位于元素周期表的p区 |
C.该阴离子中铜元素的化合价为 | D.由W和Y构成的化合物不可能为离子化合物 |
您最近一年使用:0次
名校
解题方法
7 . 铟是一种稀有贵金属,广泛应用于航空航天、太阳能电池等高科技领域。从铜烟灰酸浸渣(主要含PbO、 、
、 、
、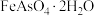 )中提取铟的工艺如图所示:
)中提取铟的工艺如图所示:
(1)铟(In)分布在元素周期表__________ 区,基态铟原子简化的核外电子排布式为__________ 。
(2)①“水浸”工艺中的滤渣除 外,还含有
外,还含有__________ 。
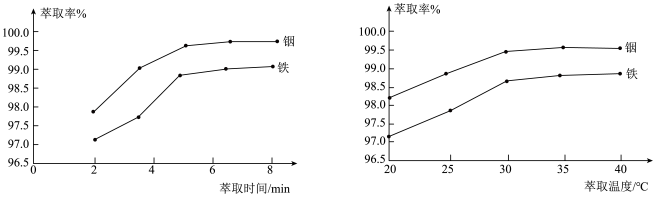
②在其他条件一定时,“水浸”铟、铁的萃取率结果如图所示,则萃取所采用的最佳条件为:萃取时间__________ ,萃取温度__________ 。__________ 。
(4)通过萃取除铁、反萃取、置换等过程,可制备金属铟。已知 能被有机萃取剂P204(简称
能被有机萃取剂P204(简称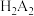 )萃取,其萃取原理可表示为
)萃取,其萃取原理可表示为 ,平衡常数为K.已知
,平衡常数为K.已知 与萃取率(E%)的关系符合公式:
与萃取率(E%)的关系符合公式: 。当pH=2.30时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=
。当pH=2.30时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=__________ ( ,忽略萃取剂浓度的变化,结果保留三位有效数字)。
,忽略萃取剂浓度的变化,结果保留三位有效数字)。
(5)一种铜铟硒晶体(化学式为 )的晶胞结构如图所示,晶胞中In和Se未标明,用A或者B代替。推断In是
)的晶胞结构如图所示,晶胞中In和Se未标明,用A或者B代替。推断In是__________ (填“A”或“B”),晶体中1mol Cu周围与它最近且等距离的A粒子的数目为__________ 。
 、
、 、
、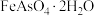 )中提取铟的工艺如图所示:
)中提取铟的工艺如图所示: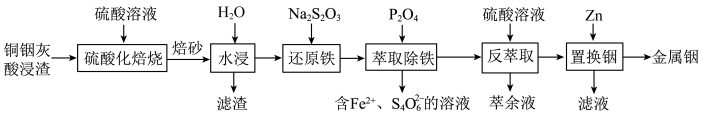
(1)铟(In)分布在元素周期表
(2)①“水浸”工艺中的滤渣除
 外,还含有
外,还含有②在其他条件一定时,“水浸”铟、铁的萃取率结果如图所示,则萃取所采用的最佳条件为:萃取时间
(4)通过萃取除铁、反萃取、置换等过程,可制备金属铟。已知
 能被有机萃取剂P204(简称
能被有机萃取剂P204(简称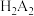 )萃取,其萃取原理可表示为
)萃取,其萃取原理可表示为 ,平衡常数为K.已知
,平衡常数为K.已知 与萃取率(E%)的关系符合公式:
与萃取率(E%)的关系符合公式: 。当pH=2.30时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=
。当pH=2.30时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH= ,忽略萃取剂浓度的变化,结果保留三位有效数字)。
,忽略萃取剂浓度的变化,结果保留三位有效数字)。(5)一种铜铟硒晶体(化学式为
 )的晶胞结构如图所示,晶胞中In和Se未标明,用A或者B代替。推断In是
)的晶胞结构如图所示,晶胞中In和Se未标明,用A或者B代替。推断In是
您最近一年使用:0次
8 . CO和NO都是有毒气体,但新的研究表明,它们都是生命体系气体信号分子,在人体内具有重要的生理作用, 是高中阶段常见的气体。
是高中阶段常见的气体。
回答下列问题:.
(1)反应
 是联合硝酸工业减少污染物排放的重要反应。该反应分为三步完成(都是双分子反应,即反应物都只有两种分子),前两步反应如下:
是联合硝酸工业减少污染物排放的重要反应。该反应分为三步完成(都是双分子反应,即反应物都只有两种分子),前两步反应如下:
第1步:
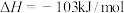
第2步:
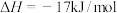
①写出第3步反应的热化学方程式:__________ 。
②基元反应 ,正反应速率
,正反应速率 。
。 的正反应速率
的正反应速率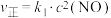 ,总反应速率
,总反应速率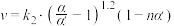 ,
, 是平衡转化率,
是平衡转化率,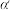 是瞬时转化率,k、
是瞬时转化率,k、 、
、 均为速率常数,受温度影响,温度升高,速率常数增大。
均为速率常数,受温度影响,温度升高,速率常数增大。
Ⅰ.复杂反应分为多步进行时,决定反应速率的是最__________ (填“快”或“慢”)的一步,3步基元反应中,活化能最高的一步是第__________ 步。
Ⅱ.温度升高,
__________ (填“变大”、“变小”或“不变”)。在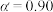 时,一系列温度下的总反应速率-时间
时,一系列温度下的总反应速率-时间 曲线如图所示,分析图中曲线先升后降的原因:
曲线如图所示,分析图中曲线先升后降的原因:__________ 。
反应Ⅰ: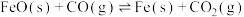
反应Ⅱ:
①将FeO和CO放入恒容密闭容器中,下列事实能说明反应Ⅰ和Ⅱ均已达到平衡状态的是__________ (填选项字母)。
A.容器内气体的密度不再发生变化 B.CO的生成速率等于消耗速率
C.容器内气体总压强不再发生变化 D.容器内CO和 的物质的量相等
的物质的量相等
②在一个体积可变的容器中,维持温度1200K不变(此时反应Ⅰ的分压平衡常数 )。压缩容器体积,达到新平衡时,CO的分压
)。压缩容器体积,达到新平衡时,CO的分压__________ (墳“变大”、“变小”或“不变”)。用压力传感器测得平衡时容器内压强为1200kPa,计算反应Ⅱ的分压平衡常数 =
=__________ kPa。
 是高中阶段常见的气体。
是高中阶段常见的气体。回答下列问题:.
(1)反应

 是联合硝酸工业减少污染物排放的重要反应。该反应分为三步完成(都是双分子反应,即反应物都只有两种分子),前两步反应如下:
是联合硝酸工业减少污染物排放的重要反应。该反应分为三步完成(都是双分子反应,即反应物都只有两种分子),前两步反应如下:第1步:

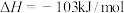
第2步:

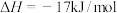
①写出第3步反应的热化学方程式:
②基元反应
 ,正反应速率
,正反应速率 。
。 的正反应速率
的正反应速率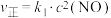 ,总反应速率
,总反应速率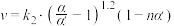 ,
, 是平衡转化率,
是平衡转化率,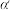 是瞬时转化率,k、
是瞬时转化率,k、 、
、 均为速率常数,受温度影响,温度升高,速率常数增大。
均为速率常数,受温度影响,温度升高,速率常数增大。Ⅰ.复杂反应分为多步进行时,决定反应速率的是最
Ⅱ.温度升高,

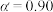 时,一系列温度下的总反应速率-时间
时,一系列温度下的总反应速率-时间 曲线如图所示,分析图中曲线先升后降的原因:
曲线如图所示,分析图中曲线先升后降的原因: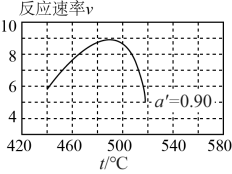
反应Ⅰ:
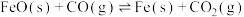
反应Ⅱ:

①将FeO和CO放入恒容密闭容器中,下列事实能说明反应Ⅰ和Ⅱ均已达到平衡状态的是
A.容器内气体的密度不再发生变化 B.CO的生成速率等于消耗速率
C.容器内气体总压强不再发生变化 D.容器内CO和
 的物质的量相等
的物质的量相等②在一个体积可变的容器中,维持温度1200K不变(此时反应Ⅰ的分压平衡常数
 )。压缩容器体积,达到新平衡时,CO的分压
)。压缩容器体积,达到新平衡时,CO的分压 =
=
您最近一年使用:0次
名校
9 . 恒温条件下,用图1所示装置研究铁的电化学腐蚀,测定结果如图2。
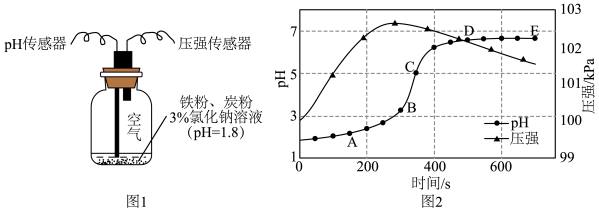
| A.AB段pH越大,析氢速率越大 |
B.AD段负极反应式为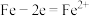 |
C.BC段正极反应式主要为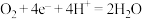 |
D.DE段溶液pH基本不变,可能的原因:相同时间内,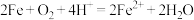 消耗 消耗 的量与 的量与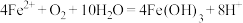 产生 产生 的量基本相同 的量基本相同 |
您最近一年使用:0次
名校
10 . 醛生成亚胺的反应机理如图,R代表烃基。下列说法错误的是
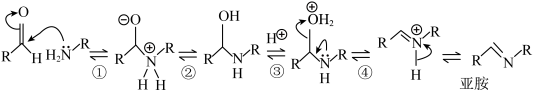
| A.反应历程中,极性键、非极性键均涉及断裂和形成 |
| B.反应历程中,N原子的杂化方式有2种 |
| C.反应历程中,氧原子始终保持8电子稳定结构 |
D.苯甲醛与羟胺( )反应的产物存在顺反异构 )反应的产物存在顺反异构 |
您最近一年使用:0次



