1 . 磷酸亚铁锂(LiFePO4)和锰酸锂(LiMn2O4)均可用作锂电池的正极材料。回答下列问题:
(1)在周期表中,与Li化学性质最相似的邻族元素是___________ (填元素符号)。基态O原子的价电子排布图为___________ 。基态P原子电子占据最高能级的电子云在空间有___________ 个伸展方向。
(2)写出H2O2的电子式___________ 。
(3)原子核外电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为___________ 。
(4)第三周期元素中,第一电离能介于A1和P之间的元素有___________ 种。
(5)Fe元素位于周期表的___________ 区。已知:I3(Mn)=3248kJ/mol,I3(Fe)=2957kJ/mol。第三电离能I3(Mn)>I3(Fe),其主要原因是___________ 。
(1)在周期表中,与Li化学性质最相似的邻族元素是
(2)写出H2O2的电子式
(3)原子核外电子有两种相反的自旋状态,分别用
 和
和 表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为(4)第三周期元素中,第一电离能介于A1和P之间的元素有
(5)Fe元素位于周期表的
您最近一年使用:0次
名校
2 . 实验室以活性炭为催化剂,由CoCl2·6H2O制备[Co(NH3)6]Cl3的流程如下。

已知:Co2+在pH=9.4时完全沉淀为Co(OH)2。
下列说法错误的是

已知:Co2+在pH=9.4时完全沉淀为Co(OH)2。
下列说法错误的是
| A.步骤①中NH4Cl可抑制NH3·H2O电离,防止生成Co(OH)2 |
B.步骤②中的反应为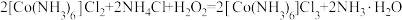 |
| C.温度越高,越有利于[Co(NH3)6]Cl3的生成 |
| D.步骤③中加入浓盐酸,降低了[Co(NH3)6]Cl3在水中的溶解度 |
您最近一年使用:0次
名校
解题方法
3 . 常温下,下列各组离子在指定溶液中一定能大量共存的是
A.加入Al放出H2的溶液中:K+、Na+、S2O 、Cl- 、Cl- |
B.中性溶液中:Fe3+、NH 、SO 、SO 、NO 、NO |
C.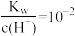 溶液中:Na+、K+、Br-、CO 溶液中:Na+、K+、Br-、CO |
| D.使甲基橙变红的溶液中:Mg2+、Fe2+、I-、CH3COO- |
您最近一年使用:0次
名校
4 .  是一种化工原料,可以制备一系列物质(如图所示)。下列说法不正确的是
是一种化工原料,可以制备一系列物质(如图所示)。下列说法不正确的是
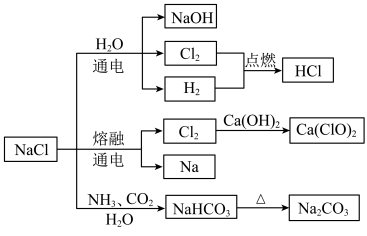
A.由氯化钠制备碳酸氢钠的过程中,发生的反应方程式为: |
| B.工业上用氯气和石灰乳反应制取漂白粉,该反应中氯气既是氧化剂又是还原剂 |
C.氢气在氯气中燃烧生成 ,有白烟产生 ,有白烟产生 |
D.25℃时, 在水中的溶解度比 在水中的溶解度比 的小 的小 |
您最近一年使用:0次
2024-03-28更新
|
72次组卷
|
2卷引用:山东省济宁市育才中学2023-2024学年高一下学期开学化学试题
名校
解题方法
5 . 下列反应的离子方程正确的是
A.钠与水反应: |
B.向 溶液中加入足量的氨水: 溶液中加入足量的氨水: |
C.铜与浓硝酸溶液反应: |
D.用小苏打治疗胃酸过多病: |
您最近一年使用:0次
2024-03-16更新
|
106次组卷
|
2卷引用:山东省烟台市莱州市第一中学2023-2024学年高一下学期开学化学试题
6 . 某无色溶液可能含有下列钠盐中的几种:
(1) A.氯化钠 B.硫化钠 C.亚硫酸钠 D.硫代硫酸钠 E.硫酸钠 F.碳酸钠。向此溶液中加入适量稀硫酸,有浅黄色的沉淀析出,同时有气体产生,此气体有臭鸡蛋气味,可使澄清的石灰水变浑浊,不能使品红试液褪色。根据上述实验现象回答下列问题。(硫代硫酸钠: ,
, )
)
①不能使品红试液褪色,说明该气体中不含_______ (填分子式)。
②此无色溶液中至少存在哪几种钠盐?请写出全部可能的情况(填写相应的字母,有几种写几种)。第一种情况是_______ ,第二种情况是_______ ,第三种情况是_______ ,第四种情况是_______ 。
(2)聚合硫酸铁(PFS)是一种性能优异的无机高分子絮凝剂,其化学式通常表示为 。某化工厂制备PFS并用其处理废水。
。某化工厂制备PFS并用其处理废水。
Ⅰ.用硫酸铜废液制备PFS

①试剂A为_______ 。
②“控温氧化”发生反应的离子方程式为_______ 。
③测定PFS样品中的 :取ag样品,溶解于
:取ag样品,溶解于 溶液中,用KF溶液掩蔽
溶液中,用KF溶液掩蔽 (使
(使 不能与
不能与 反应),再用
反应),再用 溶液反应,中和完全时消耗NaOH溶液体积为
溶液反应,中和完全时消耗NaOH溶液体积为 。agPFS样品中的
。agPFS样品中的
_______ mol。
Ⅱ.用石灰乳-PFS法处理含砷废水

已知:
i.常温下, 难溶,
难溶, 可溶;
可溶;
ii.常温下,溶液中含砷微粒的物质的量分数与pH的关系如图。

④ 溶液的pH
溶液的pH_______ 7(填“大于”、“小于”或“等于”)。
⑤“二级沉降”中,溶液的pH在8~10之间,PFS形成的 胶体粒子可以通过沉淀反应进一步减少溶液中的As含量,反应的离子方程式为
胶体粒子可以通过沉淀反应进一步减少溶液中的As含量,反应的离子方程式为_______ 。
⑥溶液的pH和m(Fe)/m(As)对As去除率的影响如图。某酸性含砷废水中As含量为20mg/L,为达到排放标准(As含量≤1mg/L),从节约成本的角度考虑,工业上选择的最佳条件是_______ (填序号)。

a.pH=8.2 m(Fe)/m(As)=5 b.pH=8.2 m(Fe)/m(As)=8
c.pH=9.0 m(Fe)/m(As)=5 d.pH=9.0 m(Fe)/m(As)=8
[m(Fe)/m(As)指PFS中Fe元素质量与对应废水中As元素质量之比]
(1) A.氯化钠 B.硫化钠 C.亚硫酸钠 D.硫代硫酸钠 E.硫酸钠 F.碳酸钠。向此溶液中加入适量稀硫酸,有浅黄色的沉淀析出,同时有气体产生,此气体有臭鸡蛋气味,可使澄清的石灰水变浑浊,不能使品红试液褪色。根据上述实验现象回答下列问题。(硫代硫酸钠:
 ,
, )
)①不能使品红试液褪色,说明该气体中不含
②此无色溶液中至少存在哪几种钠盐?请写出全部可能的情况(填写相应的字母,有几种写几种)。第一种情况是
(2)聚合硫酸铁(PFS)是一种性能优异的无机高分子絮凝剂,其化学式通常表示为
 。某化工厂制备PFS并用其处理废水。
。某化工厂制备PFS并用其处理废水。Ⅰ.用硫酸铜废液制备PFS

①试剂A为
②“控温氧化”发生反应的离子方程式为
③测定PFS样品中的
 :取ag样品,溶解于
:取ag样品,溶解于 溶液中,用KF溶液掩蔽
溶液中,用KF溶液掩蔽 (使
(使 不能与
不能与 反应),再用
反应),再用 溶液反应,中和完全时消耗NaOH溶液体积为
溶液反应,中和完全时消耗NaOH溶液体积为 。agPFS样品中的
。agPFS样品中的
Ⅱ.用石灰乳-PFS法处理含砷废水

已知:
i.常温下,
 难溶,
难溶, 可溶;
可溶;ii.常温下,溶液中含砷微粒的物质的量分数与pH的关系如图。

④
 溶液的pH
溶液的pH⑤“二级沉降”中,溶液的pH在8~10之间,PFS形成的
 胶体粒子可以通过沉淀反应进一步减少溶液中的As含量,反应的离子方程式为
胶体粒子可以通过沉淀反应进一步减少溶液中的As含量,反应的离子方程式为⑥溶液的pH和m(Fe)/m(As)对As去除率的影响如图。某酸性含砷废水中As含量为20mg/L,为达到排放标准(As含量≤1mg/L),从节约成本的角度考虑,工业上选择的最佳条件是

a.pH=8.2 m(Fe)/m(As)=5 b.pH=8.2 m(Fe)/m(As)=8
c.pH=9.0 m(Fe)/m(As)=5 d.pH=9.0 m(Fe)/m(As)=8
[m(Fe)/m(As)指PFS中Fe元素质量与对应废水中As元素质量之比]
您最近一年使用:0次
名校
7 . 亚氯酸钠 主要用于棉纺,造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下
主要用于棉纺,造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下
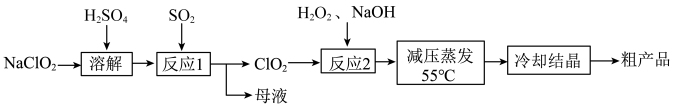
已知:①亚氯酸钠 受热易分解;②高浓度的
受热易分解;②高浓度的 易爆炸。
易爆炸。
(1) 与
与 因有强氧化性而用作常用消毒剂,消毒时均被还原为
因有强氧化性而用作常用消毒剂,消毒时均被还原为 ,则
,则 的消毒能力(转移电子的物质的量)是等质量的
的消毒能力(转移电子的物质的量)是等质量的 的
的______ 倍(保留小数点后一位)。“反应1”需要鼓入空气,空气的作用是______ 。
(2)“反应2”发生反应的化学方程式:______ 。“反应2”需要控制反应温度不能过高,温度过高可能导致______ 。
(3)从“母液”中可回收的主要物质是______ 。
(4)为探究 的氧化性,可以选择下列试剂
的氧化性,可以选择下列试剂______ 。根据选择的试剂,描述能体现 氧化性的实验现象是
氧化性的实验现象是______
A.淀粉-KI溶液 B.酸性高锰酸钾溶液 C.氯水 D. 溶液
溶液
 主要用于棉纺,造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下
主要用于棉纺,造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下
已知:①亚氯酸钠
 受热易分解;②高浓度的
受热易分解;②高浓度的 易爆炸。
易爆炸。(1)
 与
与 因有强氧化性而用作常用消毒剂,消毒时均被还原为
因有强氧化性而用作常用消毒剂,消毒时均被还原为 ,则
,则 的消毒能力(转移电子的物质的量)是等质量的
的消毒能力(转移电子的物质的量)是等质量的 的
的(2)“反应2”发生反应的化学方程式:
(3)从“母液”中可回收的主要物质是
(4)为探究
 的氧化性,可以选择下列试剂
的氧化性,可以选择下列试剂 氧化性的实验现象是
氧化性的实验现象是A.淀粉-KI溶液 B.酸性高锰酸钾溶液 C.氯水 D.
 溶液
溶液
您最近一年使用:0次
8 . 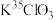 与浓
与浓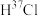 反应的化学方程式:
反应的化学方程式: 。正确的是
。正确的是
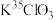 与浓
与浓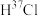 反应的化学方程式:
反应的化学方程式: 。正确的是
。正确的是| A.所得氯气的相对分子质量约为71 |
B. 中 中 |
C. 中 中 既含 既含 又含 又含 |
D. 中 中 个数比为 个数比为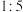 |
您最近一年使用:0次
名校
解题方法
9 . amolFeS与bmolFeO投入到VL、cmol/L的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看作是 、
、 的混合液,则反应中未被还原的硝酸可能为
的混合液,则反应中未被还原的硝酸可能为
 、
、 的混合液,则反应中未被还原的硝酸可能为
的混合液,则反应中未被还原的硝酸可能为A.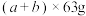 | B. | C. | D. |
您最近一年使用:0次
10 . 由一种阳离子与两种酸根离子组成的盐称为混盐。混盐 在酸性条件下可以产生氯气,下列关于混盐
在酸性条件下可以产生氯气,下列关于混盐 的有关判断不正确的是
的有关判断不正确的是
 在酸性条件下可以产生氯气,下列关于混盐
在酸性条件下可以产生氯气,下列关于混盐 的有关判断不正确的是
的有关判断不正确的是A.混盐 中两种酸根离子为 中两种酸根离子为 和 和 |
| B.该混盐具有较强的氧化性 |
| C.该混盐中氯元素的化合价为+1和-1价 |
D.该混盐与盐酸反应产生 时转移2mol电子 时转移2mol电子 |
您最近一年使用:0次



