1 . 氮和氧是构建化合物的常见元素。
(1)下列说法正确的是___________。
(2)①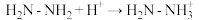 ,其中
,其中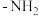 的
的 原子杂化方式为
原子杂化方式为___________ ;比较键角 中的-NH2
中的-NH2_____ H2N-NH 中的-NH
中的-NH (填“>”、“<”或“=”),请说明理由
(填“>”、“<”或“=”),请说明理由___________ 。
②将 与
与 按物质的量之比
按物质的量之比 发生化合反应生成A,测得A由2种微粒构成,其中之一是
发生化合反应生成A,测得A由2种微粒构成,其中之一是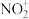 。比较氧化性强弱:NO
。比较氧化性强弱:NO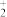
_____ HNO3(填“>”、“<”或“=”);写出A中阴离子的结构式___________ 。
已知: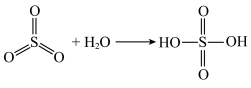
(1)下列说法正确的是___________。
A.电负性: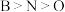 | B.离子半径: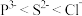 |
C.第一电离能: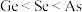 | D.基态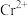 的简化电子排布式: 的简化电子排布式: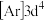 |
(2)①
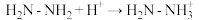 ,其中
,其中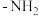 的
的 原子杂化方式为
原子杂化方式为 中的-NH2
中的-NH2 中的-NH
中的-NH (填“>”、“<”或“=”),请说明理由
(填“>”、“<”或“=”),请说明理由②将
 与
与 按物质的量之比
按物质的量之比 发生化合反应生成A,测得A由2种微粒构成,其中之一是
发生化合反应生成A,测得A由2种微粒构成,其中之一是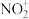 。比较氧化性强弱:NO
。比较氧化性强弱:NO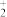
您最近一年使用:0次
2 . S8与NH3在无水条件下反应,得到一种二元化合物A,元素分析可知,A中含S元素69.60%。A进行如下反应:
(1)A、B、C、D的化学式分别为___________ 、___________ 、___________ 、___________ 。
(2)A与SnCl2的乙醇溶液反应除生成B外,还生成一种含Sn(IV)化合物,试写出A→B的化学方程式___________ 。
(3)D与一种无色液体(该液体是由常见的红棕色气体在加压下形成的)互为等电子体,但D与无色液体的几何构型完全不同,为环状结构,试画出D的最稳定的Lewis结构式___________ ,理由是___________ ,该Lewis结构式中,S原子的电子构型是___________ 。

(1)A、B、C、D的化学式分别为
(2)A与SnCl2的乙醇溶液反应除生成B外,还生成一种含Sn(IV)化合物,试写出A→B的化学方程式
(3)D与一种无色液体(该液体是由常见的红棕色气体在加压下形成的)互为等电子体,但D与无色液体的几何构型完全不同,为环状结构,试画出D的最稳定的Lewis结构式
您最近一年使用:0次
名校
3 . 亚硫酸钠和硫代硫酸钠(Na2S2O3)都是重要的含硫化合物。某化学兴趣小组进行以下有关实验,填写下列空白。
实验Ⅰ:证明Na2SO3中硫元素的价态能发生+4→+6转化
(1)实验中,不需要用到的试剂有___________ (填标号)。
a.稀硫酸 b.H2O2溶液 c.稀盐酸 d.淀粉碘化钾溶液 e.BaCl2溶液
观察到的现象是___________ 。
实验Ⅱ:制取硫代硫酸钠
利用如图所示装置进行实验___________ 。
(3)装置D的作用是___________ 。
(4)实验中,为使 缓慢通入烧瓶C,采取的操作是
缓慢通入烧瓶C,采取的操作是___________ 。
实验Ⅲ:测定某硫代硫酸钠样品的纯度(设样品中只含Na2SO3杂质)
设计如下方案,并进行实验:
①准确称取该硫代硫酸钠样品7.9g,配制成250mL待测溶液。
②移取25.00mL待测溶液于锥形瓶中,加入适量甲醛(防止Na2SO3与I2反应)和少量淀粉溶液,用0.1mol·L-1I2标准溶液滴定(发生反应:2S2O +I2=S4O
+I2=S4O +2I-),至滴定终点共消耗标准溶液23.60mL。
+2I-),至滴定终点共消耗标准溶液23.60mL。
(5)样品中Na2S2O3的百分含量为___________ (保留三位有效数字)。
实验Ⅰ:证明Na2SO3中硫元素的价态能发生+4→+6转化
(1)实验中,不需要用到的试剂有
a.稀硫酸 b.H2O2溶液 c.稀盐酸 d.淀粉碘化钾溶液 e.BaCl2溶液
观察到的现象是
实验Ⅱ:制取硫代硫酸钠
利用如图所示装置进行实验
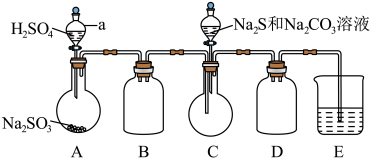
(3)装置D的作用是
(4)实验中,为使
 缓慢通入烧瓶C,采取的操作是
缓慢通入烧瓶C,采取的操作是实验Ⅲ:测定某硫代硫酸钠样品的纯度(设样品中只含Na2SO3杂质)
设计如下方案,并进行实验:
①准确称取该硫代硫酸钠样品7.9g,配制成250mL待测溶液。
②移取25.00mL待测溶液于锥形瓶中,加入适量甲醛(防止Na2SO3与I2反应)和少量淀粉溶液,用0.1mol·L-1I2标准溶液滴定(发生反应:2S2O
 +I2=S4O
+I2=S4O +2I-),至滴定终点共消耗标准溶液23.60mL。
+2I-),至滴定终点共消耗标准溶液23.60mL。(5)样品中Na2S2O3的百分含量为
您最近一年使用:0次
4 . 高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺流程如下:
(1)K2FeO4中铁元素在周期表中的位置第___________ 周期第___________ 列。
(2)在溶液I中加入KOH固体的目的是___________(填字母)。
(3)“纯化”时需加入饱和的KOH溶液,其作用是___________ 。
(4)从溶液II中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为___________ 。每制得59.4 g K2FeO4,理论上消耗氧化剂的物质的量为___________ mol。
(5)工业上用异丙醇对湿产品进行洗涤,目的是___________ 。
(6)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,写出该反应的离子方程式:___________ 。
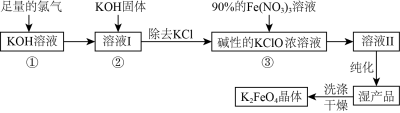
(1)K2FeO4中铁元素在周期表中的位置第
(2)在溶液I中加入KOH固体的目的是___________(填字母)。
| A.为下一步反应提供碱性的环境 |
| B.使KClO3转化为KClO |
| C.与溶液I中过量的Cl2继续反应,生成更多的KClO |
| D.KOH固体溶解时会放出较多的热量,有利于提高反应速率 |
(3)“纯化”时需加入饱和的KOH溶液,其作用是
(4)从溶液II中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为
(5)工业上用异丙醇对湿产品进行洗涤,目的是
(6)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,写出该反应的离子方程式:
您最近一年使用:0次
名校
5 . 如图是氮元素的几种价态与物质类别的对应关系。回答下列问题:
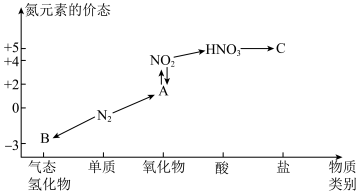
(1)B物质的电子式为:_______ 。
(2)实验室制取物质B的化学方程式为_______ 。
(3)浓硝酸与木炭在加热条件下反应的化学方程式为_______ 。
(4)将3.2g铜与60.0mL一定浓度的硝酸发生反应,铜完全溶解,产生 和NO混合气体的体积为8.96L(标况)。待产生的气体全部释放后,向溶液加入
和NO混合气体的体积为8.96L(标况)。待产生的气体全部释放后,向溶液加入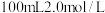 的NaOH溶液,恰好使溶液中的
的NaOH溶液,恰好使溶液中的 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为_______  。
。

(1)B物质的电子式为:
(2)实验室制取物质B的化学方程式为
(3)浓硝酸与木炭在加热条件下反应的化学方程式为
(4)将3.2g铜与60.0mL一定浓度的硝酸发生反应,铜完全溶解,产生
 和NO混合气体的体积为8.96L(标况)。待产生的气体全部释放后,向溶液加入
和NO混合气体的体积为8.96L(标况)。待产生的气体全部释放后,向溶液加入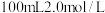 的NaOH溶液,恰好使溶液中的
的NaOH溶液,恰好使溶液中的 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为 。
。
您最近一年使用:0次
解题方法
6 . 锰是冶金工业中不可缺少的添加剂,它的作用是增加合金金属材料的硬度、韧性、耐磨性和耐腐性,应用最广泛的有不锈钢、高锰钢、锰铝合金等。位于遵义市红花岗区坪桥工业园区的遵义天磁锰业集团有限公司就是一家电解锰公司;以碳酸锰为主要原料,其中含有少量铁、铝、钙、硅的氧化物或硫化物等杂质,以下是电解锰的简化工艺流程图:

(1)粉碎的目的___________ 。
(2)写出浸出时主要的离子反应___________ ,同时会产生的有毒气体是___________ 。
(3)加双氧水的作用方程式表示出来___________ 。
(4)加入氨水的作用是___________ ,除铁的离子反应___________ 。
(5)电解制锰的电极反应___________ ,当外电路转移2mol电子时,生成的气体是___________ ,在标准状况下的体积为___________ L,阳极液中产生的___________ 可循环使用。

(1)粉碎的目的
(2)写出浸出时主要的离子反应
(3)加双氧水的作用方程式表示出来
(4)加入氨水的作用是
(5)电解制锰的电极反应
您最近一年使用:0次
7 . 钯( )是航天、航空等高科技领域以及汽车制造业不可缺少的关键材料。为节约和充分利用资源,以废钯催化剂(主要成分是钯、碳、有机物及少量
)是航天、航空等高科技领域以及汽车制造业不可缺少的关键材料。为节约和充分利用资源,以废钯催化剂(主要成分是钯、碳、有机物及少量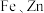 等元素)为原料通过如下工艺流程回收钯。
等元素)为原料通过如下工艺流程回收钯。
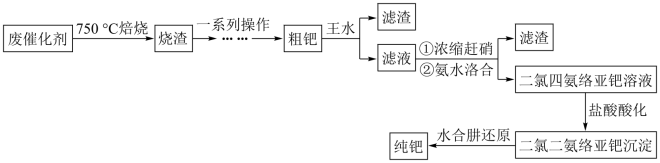
回答下列问题:
(1)“焙烧”时通入的空气一定要足量,目的是_______ 。
(2)“一系列操作”包括向烧渣中加入 ,目的是将
,目的是将 还原得到粗钯,写出反应的化学方程式:
还原得到粗钯,写出反应的化学方程式:___________ 。
(3)得到粗钯后,用王水在一定温度下充分浸取钯,得到氯亚钯酸( )和一种有毒的无色气体
)和一种有毒的无色气体 ,该气体遇空气变为红棕色,该反应中消耗的
,该气体遇空气变为红棕色,该反应中消耗的 与
与 的物质的量之比为
的物质的量之比为_______ 。钯的浸出率与反应的时间、温度的关系如图所示,则最佳的浸取时间和温度为_______ 。
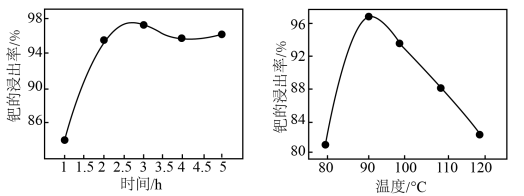
(4)“氨水络合”时需要控制好溶液的 ,已知常温下,
,已知常温下, ,
, ,要使得溶液中的杂质金属离子沉淀完全(即金属离子浓度低于
,要使得溶液中的杂质金属离子沉淀完全(即金属离子浓度低于 ),
), 至少调节为
至少调节为______ (保留三位有效数字)。(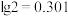 )
)
(5)海绵状金属钯密度为 ,具有优良的吸氢功能,标准状况下,其吸附的氢气是其体积的840倍,则此条件下海绵钯的吸附容量
,具有优良的吸氢功能,标准状况下,其吸附的氢气是其体积的840倍,则此条件下海绵钯的吸附容量
______ 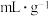 ,氢气的浓度
,氢气的浓度
______ (保留小数点后两位)。(吸附容量 即
即 钯吸附氢气的体积;氢气的浓度
钯吸附氢气的体积;氢气的浓度 为
为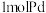 吸附标准状况下氢气的物质的量)
吸附标准状况下氢气的物质的量)
 )是航天、航空等高科技领域以及汽车制造业不可缺少的关键材料。为节约和充分利用资源,以废钯催化剂(主要成分是钯、碳、有机物及少量
)是航天、航空等高科技领域以及汽车制造业不可缺少的关键材料。为节约和充分利用资源,以废钯催化剂(主要成分是钯、碳、有机物及少量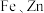 等元素)为原料通过如下工艺流程回收钯。
等元素)为原料通过如下工艺流程回收钯。
回答下列问题:
(1)“焙烧”时通入的空气一定要足量,目的是
(2)“一系列操作”包括向烧渣中加入
 ,目的是将
,目的是将 还原得到粗钯,写出反应的化学方程式:
还原得到粗钯,写出反应的化学方程式:(3)得到粗钯后,用王水在一定温度下充分浸取钯,得到氯亚钯酸(
 )和一种有毒的无色气体
)和一种有毒的无色气体 ,该气体遇空气变为红棕色,该反应中消耗的
,该气体遇空气变为红棕色,该反应中消耗的 与
与 的物质的量之比为
的物质的量之比为
(4)“氨水络合”时需要控制好溶液的
 ,已知常温下,
,已知常温下, ,
, ,要使得溶液中的杂质金属离子沉淀完全(即金属离子浓度低于
,要使得溶液中的杂质金属离子沉淀完全(即金属离子浓度低于 ),
), 至少调节为
至少调节为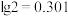 )
)(5)海绵状金属钯密度为
 ,具有优良的吸氢功能,标准状况下,其吸附的氢气是其体积的840倍,则此条件下海绵钯的吸附容量
,具有优良的吸氢功能,标准状况下,其吸附的氢气是其体积的840倍,则此条件下海绵钯的吸附容量
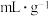 ,氢气的浓度
,氢气的浓度
 即
即 钯吸附氢气的体积;氢气的浓度
钯吸附氢气的体积;氢气的浓度 为
为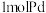 吸附标准状况下氢气的物质的量)
吸附标准状况下氢气的物质的量)
您最近一年使用:0次
解题方法
8 . 除了上面的金属钠之外,白风还发现了以前一位学弟留下的实验报告。
只是,这实验报告怎么看着这么像数学题……?
“看来这个学弟很喜欢5啊……”
一定条件下将一定量氯气通入KOH溶液中,生成 m mol氯酸钾、n mol次氯酸钾以及其他常见物质。用NA代表阿伏加德罗常数的值:
(1)若m + n = 5,则反应中转移的电子的物质的量最大为___________ 。
(2)若m - n = 5,则反应中被还原的氯原子和被氧化的氯原子物质的量的比值的最大值为___________ 。
(3)若mn = 5,则反应中转移的电子数量最小为___________ 。
(4)若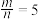 ,则反应中被还原的氯原子和被氧化的氯原子数目之比为
,则反应中被还原的氯原子和被氧化的氯原子数目之比为___________ 。
(5)我们可以用一个转化系数α来近似描述混合液的漂白性,其中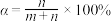 ,白风根据实验报告选用不同的温度测定了对应时刻的α,并绘制出了T-α图像:
,白风根据实验报告选用不同的温度测定了对应时刻的α,并绘制出了T-α图像:
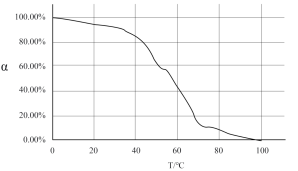
Ⅰ.由图像我们可以得出的结论是:______________________ 。
Ⅱ.试推测为什么图像会有这种趋势:______________________ 。
只是,这实验报告怎么看着这么像数学题……?
“看来这个学弟很喜欢5啊……”
一定条件下将一定量氯气通入KOH溶液中,生成 m mol氯酸钾、n mol次氯酸钾以及其他常见物质。用NA代表阿伏加德罗常数的值:
(1)若m + n = 5,则反应中转移的电子的物质的量最大为
(2)若m - n = 5,则反应中被还原的氯原子和被氧化的氯原子物质的量的比值的最大值为
(3)若mn = 5,则反应中转移的电子数量最小为
(4)若
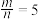 ,则反应中被还原的氯原子和被氧化的氯原子数目之比为
,则反应中被还原的氯原子和被氧化的氯原子数目之比为(5)我们可以用一个转化系数α来近似描述混合液的漂白性,其中
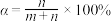 ,白风根据实验报告选用不同的温度测定了对应时刻的α,并绘制出了T-α图像:
,白风根据实验报告选用不同的温度测定了对应时刻的α,并绘制出了T-α图像:
Ⅰ.由图像我们可以得出的结论是:
Ⅱ.试推测为什么图像会有这种趋势:
您最近一年使用:0次
9 . “说起来,你知道传统文化里有多少化学知识喵~”
(1)《天工开物》中曾经记载过灰吹法冶炼白银的方法:灰吹法(cuppelation)是一种古代金银共生分离和银铅分离出银的方法。 银多与其它有色金属共生,而且银的含量行为往往偏少,故需要加以分离和提纯。灰吹法主要利用银铅互熔,使矿石中的银溶于铅中,通入空气,使铅氧化沉积,成为密陀僧(Lithargyrum),使银铅得以分离,且银得到提纯。
Ⅰ.密陀僧的主要成分的化学式为___________ 。
Ⅱ.铅在步骤中被采用的原因是:___________ ;___________ 。
Ⅲ.该过程中涉及到以下哪些步骤?___________
A.萃取 B.蒸馏 C.分液 D.溶解 E.以上都没有
(2)徽墨制作技艺,安徽省绩溪县、歙县、黄山市屯溪区地方传统手工技艺,国家级非物质文化遗产之一、徽墨是中国特有传统制墨技艺中的珍品,也是闻名中外的“文房四宝”之一、2006年5月,徽墨制作技艺经国务院批准列入第一批国家级非物质文化遗产名录。
【本题以桐烟徽墨为例】
Ⅰ.“一盏油灯燃烧一天一夜,才能收集大约10克烟灰。”这里烟灰俗名为___________ 。
Ⅱ.中国古代没有墨水只有墨锭,每当用时再加水研磨。如何让烟灰既能均匀分布在水中,又能坚固成型?古人最终决定将徽墨制作成___________ (填一种分散系),这是利用了这种分散系的___________ 和___________ 这两个性质。
(3)“纸香弥漫处,徽墨已半干。提笔风流起,落笔淡雅生。” 富阳土纸是古代劳动人民采用当年生的嫩毛竹作原料,靠手工操造而成的毛笔书写用纸。土纸是浙江省富阳市的特产。富阳土纸薄如蝉衣,韧力似纺绸,品多质优,张面光洁,色泽白净,不受虫蛀,不会变色。写字作画滋润而悦目。在制浆过程中,用石灰乳,草木灰水作蒸煮剂浸透,目的在于脱去原料中的色素,除去污质、蜡质、松解原料中残留的胶质及其它填充物。其中石灰乳和草木灰的化学式分别是:___________ ;___________ 。
(1)《天工开物》中曾经记载过灰吹法冶炼白银的方法:灰吹法(cuppelation)是一种古代金银共生分离和银铅分离出银的方法。 银多与其它有色金属共生,而且银的含量行为往往偏少,故需要加以分离和提纯。灰吹法主要利用银铅互熔,使矿石中的银溶于铅中,通入空气,使铅氧化沉积,成为密陀僧(Lithargyrum),使银铅得以分离,且银得到提纯。
Ⅰ.密陀僧的主要成分的化学式为
Ⅱ.铅在步骤中被采用的原因是:
Ⅲ.该过程中涉及到以下哪些步骤?
A.萃取 B.蒸馏 C.分液 D.溶解 E.以上都没有
(2)徽墨制作技艺,安徽省绩溪县、歙县、黄山市屯溪区地方传统手工技艺,国家级非物质文化遗产之一、徽墨是中国特有传统制墨技艺中的珍品,也是闻名中外的“文房四宝”之一、2006年5月,徽墨制作技艺经国务院批准列入第一批国家级非物质文化遗产名录。
【本题以桐烟徽墨为例】
Ⅰ.“一盏油灯燃烧一天一夜,才能收集大约10克烟灰。”这里烟灰俗名为
Ⅱ.中国古代没有墨水只有墨锭,每当用时再加水研磨。如何让烟灰既能均匀分布在水中,又能坚固成型?古人最终决定将徽墨制作成
(3)“纸香弥漫处,徽墨已半干。提笔风流起,落笔淡雅生。” 富阳土纸是古代劳动人民采用当年生的嫩毛竹作原料,靠手工操造而成的毛笔书写用纸。土纸是浙江省富阳市的特产。富阳土纸薄如蝉衣,韧力似纺绸,品多质优,张面光洁,色泽白净,不受虫蛀,不会变色。写字作画滋润而悦目。在制浆过程中,用石灰乳,草木灰水作蒸煮剂浸透,目的在于脱去原料中的色素,除去污质、蜡质、松解原料中残留的胶质及其它填充物。其中石灰乳和草木灰的化学式分别是:
您最近一年使用:0次
解题方法
10 . 磷酸亚铁锂( )为近来新开发的锂离子电池电极材料,主要用于动力锂离子电池,
)为近来新开发的锂离子电池电极材料,主要用于动力锂离子电池, 废料中(含Al、石墨),其中磷、铁、锂的综合回收工艺流程图如下:
废料中(含Al、石墨),其中磷、铁、锂的综合回收工艺流程图如下: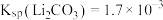
②LiOH、 的溶解度与温度的关系如下表:
的溶解度与温度的关系如下表:
(1)过程I“碱浸”的目的是___________ 。
(2)若浸出液中存在大量 离子,则反应的离子方程式为
离子,则反应的离子方程式为___________ 。
(3)①过程III得到“沉淀Y”的离子方程式为___________ 。
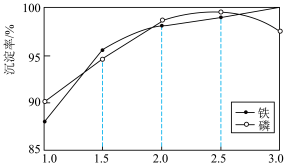
②一定条件下,探究了pH对磷酸铁沉淀的影响,结果如下图所示。由图可知,过程III应选取的最佳沉淀时的pH为___________ 。随pH的增加,磷的沉淀率开始下降,而铁沉淀率未下降,分析原因为___________ 。___________ 。
A.NaOH20-40℃ B.NaOH80-100℃
C. 20-40℃ D.
20-40℃ D. 60-80℃
60-80℃
②常温下,测得滤液1中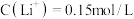 ,某同学取该100ml滤液进行“沉锂”反应。加入50mlX溶液却未见沉淀,若不考虑液体混合时的体积变化,则该同学加入的X溶液最大浓度为
,某同学取该100ml滤液进行“沉锂”反应。加入50mlX溶液却未见沉淀,若不考虑液体混合时的体积变化,则该同学加入的X溶液最大浓度为
___________  。
。
 )为近来新开发的锂离子电池电极材料,主要用于动力锂离子电池,
)为近来新开发的锂离子电池电极材料,主要用于动力锂离子电池, 废料中(含Al、石墨),其中磷、铁、锂的综合回收工艺流程图如下:
废料中(含Al、石墨),其中磷、铁、锂的综合回收工艺流程图如下: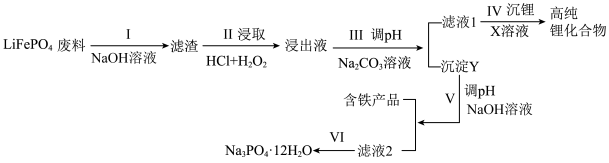
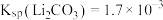
②LiOH、
 的溶解度与温度的关系如下表:
的溶解度与温度的关系如下表:| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | LiOH | 11.9 | 12.4 | 13.2 | 14.6 | 16.6 | 19.1 |
 | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 | |
(1)过程I“碱浸”的目的是
(2)若浸出液中存在大量
 离子,则反应的离子方程式为
离子,则反应的离子方程式为(3)①过程III得到“沉淀Y”的离子方程式为
②一定条件下,探究了pH对磷酸铁沉淀的影响,结果如下图所示。由图可知,过程III应选取的最佳沉淀时的pH为
A.NaOH20-40℃ B.NaOH80-100℃
C.
 20-40℃ D.
20-40℃ D. 60-80℃
60-80℃②常温下,测得滤液1中
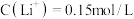 ,某同学取该100ml滤液进行“沉锂”反应。加入50mlX溶液却未见沉淀,若不考虑液体混合时的体积变化,则该同学加入的X溶液最大浓度为
,某同学取该100ml滤液进行“沉锂”反应。加入50mlX溶液却未见沉淀,若不考虑液体混合时的体积变化,则该同学加入的X溶液最大浓度为
 。
。
您最近一年使用:0次
2023-12-05更新
|
385次组卷
|
3卷引用:湖南省湘西州吉首市2024届高三上学期第二届中小学生教师解题大赛化学试题
湖南省湘西州吉首市2024届高三上学期第二届中小学生教师解题大赛化学试题山西运城新康国际中学2023-2024学年高三上学期一轮复习检测化学试卷(已下线)大题01 化工流程综合题(逐空突破)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)



