1 . 中国科学家首次成功制得大面积单晶石墨炔,是碳材料科学的一大进步。
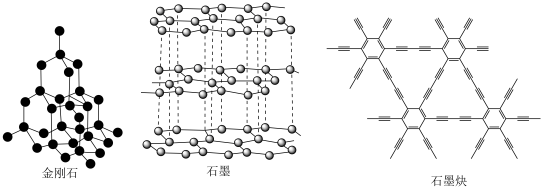
| A.三种物质均是碳单质 | B.三种物质的化学性质相同 |
| C.三种物质的晶体类型相同 | D.三种物质均能导电 |
您最近一年使用:0次
解题方法
2 . 某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是______ 。为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离子方程式______ 。
(2)“滤液②”中含有的金属离子是______ 。
(3)若工艺流程改为先“调pH”后“转化”,即,“滤液③”中可能含有的杂质离子为______ 。
(4)如果“转化”后的溶液中Ni2+浓度为1.0mol·L-1,则“调pH”应控制的pH范围是______ 。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式______ 。
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是______ 。
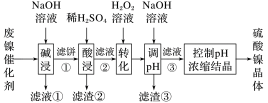

| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀时 (c=0.01mol·L-1)的pH | 7.2 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时 (c=1.0×10-5mol·L-1)的pH | 8.7 | 4.7 | 3.2 | 9.0 |
(1)“碱浸”中NaOH的两个作用分别是
(2)“滤液②”中含有的金属离子是
(3)若工艺流程改为先“调pH”后“转化”,即,“滤液③”中可能含有的杂质离子为
(4)如果“转化”后的溶液中Ni2+浓度为1.0mol·L-1,则“调pH”应控制的pH范围是
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是
您最近一年使用:0次
解题方法
3 . 下列物质的分类不正确的是
| A.烧碱、纯碱、熟石灰都属于碱 |
B. 、 、 、 、 都属于酸 都属于酸 |
C. 、 、 和干冰都属于氧化物 和干冰都属于氧化物 |
D. 、 、 和 和 都属于盐 都属于盐 |
您最近一年使用:0次
名校
4 . 反应 应用于石油开采。下列说法正确的是
应用于石油开采。下列说法正确的是
 应用于石油开采。下列说法正确的是
应用于石油开采。下列说法正确的是A. 的电子式为 的电子式为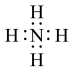 | B. 中N原子采用 中N原子采用 杂化 杂化 |
C. 晶体属于离子晶体 晶体属于离子晶体 | D. 为含极性键的非极性分子 为含极性键的非极性分子 |
您最近一年使用:0次
名校
5 . 下列化学用语描述正确的是
A. 的空间结构: 的空间结构: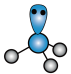 (三角锥形) (三角锥形) |
B.二氧化碳的空间填充模型: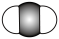 |
C. 的结构示意图: 的结构示意图: |
D.磷基态原子价层电子排布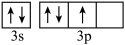 违背了泡利原理 违背了泡利原理 |
您最近一年使用:0次
解题方法
6 . (I).请按要求写出下列反应的离子方程式。
(1)铝和烧碱溶液反应___________ 。
(2)向 溶液中滴加过量浓氨水
溶液中滴加过量浓氨水___________ 。
(II).氧气是支持生命活动的一种重要物质,回答下列问题:
(3)氧气的摩尔质量为___________ 。
(4)现有0.5molO2,含氧原子物质的量为___________ ,含氧分子数为___________ 个,其体积(标准状况)为___________ ,其质量为___________ 。
(5)氧气与炭在一定条件下发生反应可以生成 CO和CO2.在标准状况下18.8 g CO与CO2的混合气体,体积为11.2 L。则:CO2和CO的物质的量之比是___________ 。
(1)铝和烧碱溶液反应
(2)向
 溶液中滴加过量浓氨水
溶液中滴加过量浓氨水(II).氧气是支持生命活动的一种重要物质,回答下列问题:
(3)氧气的摩尔质量为
(4)现有0.5molO2,含氧原子物质的量为
(5)氧气与炭在一定条件下发生反应可以生成 CO和CO2.在标准状况下18.8 g CO与CO2的混合气体,体积为11.2 L。则:CO2和CO的物质的量之比是
您最近一年使用:0次
7 . 氯化钠(NaCl)是一种常见的电解质,下列关于氯化钠的电离的说法正确的是
| A.氯化钠的电离需要通电 |
| B.氯化钠是一种离子化合物 |
| C.家用食盐是一种纯净物 |
| D.高温条件下氯化钠固体会熔化生成钠原子与氯原子 |
您最近一年使用:0次
名校
解题方法
8 . 下列反应既是氧化还原反应,又是吸热反应的是
| A.碳和二氧化碳在高温下的反应 | B.碳酸钙高温分解 |
| C.氢氧化钠和盐酸的反应 | D.铝片和稀硫酸反应 |
您最近一年使用:0次
9 . 回答下列问题。
(1)双氧水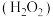 和水都是极弱电解质,若把
和水都是极弱电解质,若把 看成是二元弱酸,请写出在水中的电离方程式:
看成是二元弱酸,请写出在水中的电离方程式:___________ 。鉴于 显弱酸性,它能同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出
显弱酸性,它能同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出 与
与 作用形成盐的两个化学方程式:
作用形成盐的两个化学方程式:___________ 。
(2)如图是向 的盐酸中逐渐加入
的盐酸中逐渐加入 溶液时,溶液的
溶液时,溶液的 变化图像。
变化图像。___________  。
。
②X的值为___________ 。
(3)已知 的高碘酸
的高碘酸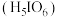 溶液与
溶液与 的
的 溶液等体积混合,所得混合溶液呈酸性,
溶液等体积混合,所得混合溶液呈酸性, 的碘酸
的碘酸 或高锰酸
或高锰酸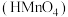 溶液与
溶液与 的
的 溶液等体积混合,所得溶液呈中性,高碘酸是
溶液等体积混合,所得溶液呈中性,高碘酸是___________ (填“强酸”或“弱酸”),理由是___________ 。
(4) 时,在一定体积
时,在一定体积 的
的 溶液中,逐滴加入一定物质的量浓度的
溶液中,逐滴加入一定物质的量浓度的 溶液,当溶液中的
溶液,当溶液中的 恰好完全沉淀时,溶液
恰好完全沉淀时,溶液 ,忽略溶液体积变化,则
,忽略溶液体积变化,则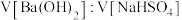 为
为___________ 。
(1)双氧水
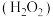 和水都是极弱电解质,若把
和水都是极弱电解质,若把 看成是二元弱酸,请写出在水中的电离方程式:
看成是二元弱酸,请写出在水中的电离方程式: 显弱酸性,它能同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出
显弱酸性,它能同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出 与
与 作用形成盐的两个化学方程式:
作用形成盐的两个化学方程式:(2)如图是向
 的盐酸中逐渐加入
的盐酸中逐渐加入 溶液时,溶液的
溶液时,溶液的 变化图像。
变化图像。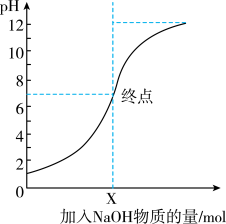
 。
。②X的值为
(3)已知
 的高碘酸
的高碘酸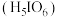 溶液与
溶液与 的
的 溶液等体积混合,所得混合溶液呈酸性,
溶液等体积混合,所得混合溶液呈酸性, 的碘酸
的碘酸 或高锰酸
或高锰酸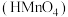 溶液与
溶液与 的
的 溶液等体积混合,所得溶液呈中性,高碘酸是
溶液等体积混合,所得溶液呈中性,高碘酸是(4)
 时,在一定体积
时,在一定体积 的
的 溶液中,逐滴加入一定物质的量浓度的
溶液中,逐滴加入一定物质的量浓度的 溶液,当溶液中的
溶液,当溶液中的 恰好完全沉淀时,溶液
恰好完全沉淀时,溶液 ,忽略溶液体积变化,则
,忽略溶液体积变化,则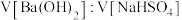 为
为
您最近一年使用:0次
10 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下,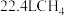 与 与 充分反应,生成的 充分反应,生成的 分子数为 分子数为 |
B. 与 与 的混合气体中含有的质子数为 的混合气体中含有的质子数为 |
C. 正丁烷和 正丁烷和 异丁烷的混合物中共价键数目为 异丁烷的混合物中共价键数目为 |
D.向密闭容器中充入 和 和 ,充分反应时转移电子 ,充分反应时转移电子 |
您最近一年使用:0次



