1 . 下图是部分短周期元素的常见化合价与原子序数的关系图: 在周期表中的位置是
在周期表中的位置是______________________ 。
(2)用电子式表示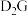 的形成过程为
的形成过程为_________________ 。
(3)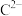 ,
,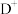 ,
,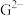 离子半径由大到小的顺序是
离子半径由大到小的顺序是______ (用离子符号表示)。
(4)某同学利用上图装置设计实验证明 ,
, ,
, 的非金属性强弱关系(已知硅酸难溶于水)。
的非金属性强弱关系(已知硅酸难溶于水)。______ (填化学式);溶液ⅲ为______ (填选项字母)。
a.饱和碳酸钠溶液 b.饱和碳酸氢钠溶液
c.饱和氢氧化钠溶液 d.饱和硅酸钠溶液
②装置丙中发生反应的离子方程式为_______________ 。
(5)将 投入
投入 的最高价氧化物对应的水化物中,其离子方程式为
的最高价氧化物对应的水化物中,其离子方程式为____________ 。

 在周期表中的位置是
在周期表中的位置是(2)用电子式表示
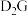 的形成过程为
的形成过程为(3)
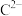 ,
,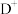 ,
,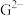 离子半径由大到小的顺序是
离子半径由大到小的顺序是(4)某同学利用上图装置设计实验证明
 ,
, ,
, 的非金属性强弱关系(已知硅酸难溶于水)。
的非金属性强弱关系(已知硅酸难溶于水)。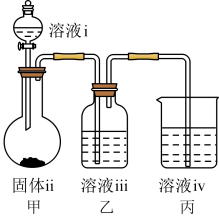
a.饱和碳酸钠溶液 b.饱和碳酸氢钠溶液
c.饱和氢氧化钠溶液 d.饱和硅酸钠溶液
②装置丙中发生反应的离子方程式为
(5)将
 投入
投入 的最高价氧化物对应的水化物中,其离子方程式为
的最高价氧化物对应的水化物中,其离子方程式为
您最近半年使用:0次
解题方法
2 . 某溶液呈酸性,可能含有: 、
、 、
、 、
、 、
、 、
、 中的若干种。对其进行如下实验:
中的若干种。对其进行如下实验:
Ⅰ.取少量溶液,向其中加入过量 ,生成白色沉淀
,生成白色沉淀 和无色气体
和无色气体 ,该无色气体在空气中变为红棕色。
,该无色气体在空气中变为红棕色。
Ⅱ.将Ⅰ中所得溶液滤去沉淀后,加入过量浓 溶液,生成无色气体,最终得到红棕色沉淀
溶液,生成无色气体,最终得到红棕色沉淀 。
。
(1)上述6种离子中,该溶液肯定存在的为____________ ,肯定不存在 的为______ ,不能 确定是否存在的为______ 。
(2)请设计实验检验原溶液中是否存在 ,写出操作方法、现象及结论
,写出操作方法、现象及结论___________ 。
(3)生成无色气体 的离子方程式为
的离子方程式为____________ 。
(4)步骤Ⅱ中发生反应的离子方程式为___________________ 。
 、
、 、
、 、
、 、
、 、
、 中的若干种。对其进行如下实验:
中的若干种。对其进行如下实验:Ⅰ.取少量溶液,向其中加入过量
 ,生成白色沉淀
,生成白色沉淀 和无色气体
和无色气体 ,该无色气体在空气中变为红棕色。
,该无色气体在空气中变为红棕色。Ⅱ.将Ⅰ中所得溶液滤去沉淀后,加入过量浓
 溶液,生成无色气体,最终得到红棕色沉淀
溶液,生成无色气体,最终得到红棕色沉淀 。
。(1)上述6种离子中,该溶液肯定存在的为
(2)请设计实验检验原溶液中是否存在
 ,写出操作方法、现象及结论
,写出操作方法、现象及结论(3)生成无色气体
 的离子方程式为
的离子方程式为(4)步骤Ⅱ中发生反应的离子方程式为
您最近半年使用:0次
3 . 将一定量的锌与 浓硫酸充分反应后,锌完全溶解,同时生成气体
浓硫酸充分反应后,锌完全溶解,同时生成气体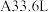 (标准状况)。将反应后的溶液稀释至
(标准状况)。将反应后的溶液稀释至 ,测得溶液的
,测得溶液的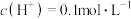 ,则下列叙述中正确的是
,则下列叙述中正确的是
 浓硫酸充分反应后,锌完全溶解,同时生成气体
浓硫酸充分反应后,锌完全溶解,同时生成气体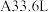 (标准状况)。将反应后的溶液稀释至
(标准状况)。将反应后的溶液稀释至 ,测得溶液的
,测得溶液的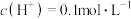 ,则下列叙述中正确的是
,则下列叙述中正确的是A.气体 为 为 |
B.稀释后所得溶液中硫酸根的浓度为 |
| C.该反应若不加热,锌会被钝化 |
D.反应中共转移 电子 电子 |
您最近半年使用:0次
4 . 从元素化合价和物质类别两个角度学习,研究物质的性质,是一种行之有效的方法。下图为氮元素的价类二维图。下列说法错误 的是

A. 的浓溶液与 的浓溶液与 的浓溶液靠近会产生白烟 的浓溶液靠近会产生白烟 |
B. 在一定条件下与氧气反应可直接生成 在一定条件下与氧气反应可直接生成 |
C. 与氧气按一定比例混合溶于水能得到 与氧气按一定比例混合溶于水能得到 |
D.若 为 为 ,碱性条件下由 ,碱性条件下由 、 、 制备 制备 的反应中氧化剂与还原剂的物质的量之比为 的反应中氧化剂与还原剂的物质的量之比为 |
您最近半年使用:0次
5 . 在无氧环境下,将 通入足量
通入足量 稀溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,并有气体产生。关于上述变化,下列说法
稀溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,并有气体产生。关于上述变化,下列说法错误 的是
 通入足量
通入足量 稀溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,并有气体产生。关于上述变化,下列说法
稀溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,并有气体产生。关于上述变化,下列说法A.最终被还原的是 |
B.氧化性: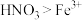 |
C.最终所得溶液中不存在 |
D.同温、同压下, 和逸出气体的体积比为 和逸出气体的体积比为 |
您最近半年使用:0次
解题方法
6 . 下列离子方程式书写正确的是
A.氧化亚铁溶于稀硝酸: |
B.铜和稀硝酸反应: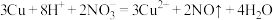 |
C.向 溶液中通入少量的 溶液中通入少量的 : :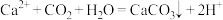 |
D.向碳酸氢铵溶液中加入过量氢氧化钠溶液: |
您最近半年使用:0次
7 . 下列溶液中能大量共存的离子组是
A.无色透明的溶液: 、 、 、 、 、 、 |
B.能使紫色石蕊溶液变红的溶液: 、 、 、 、 、 、 |
C.含有 的溶液: 的溶液: 、 、 、 、 、 、 |
D.能使酚酞溶液变红的溶液: 、 、 、 、 、 、 |
您最近半年使用:0次
8 .  代表阿伏加德罗常数的值。下列叙述正确的是
代表阿伏加德罗常数的值。下列叙述正确的是
 代表阿伏加德罗常数的值。下列叙述正确的是
代表阿伏加德罗常数的值。下列叙述正确的是A.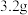 氧气和臭氧的混合气体中所含原子总数为 氧气和臭氧的混合气体中所含原子总数为 |
B.标准状况下, 水中含有的质子数为 水中含有的质子数为 |
C.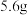 铁粉溶于稀硝酸后转移电子数为 铁粉溶于稀硝酸后转移电子数为 |
D.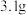 白磷( 白磷(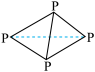 )中所含共价键数为 )中所含共价键数为 |
您最近半年使用:0次
名校
解题方法
9 . FeO(OH)在高档涂料、油墨等领域有着广泛的应用。以铁泥(主要含Fe2O3,以及少量的 、
、 、SiO2)为原料制备FeO(OH)的流程如图所示。
、SiO2)为原料制备FeO(OH)的流程如图所示。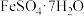 溶于水,不溶于乙醇。回答下列问题:
溶于水,不溶于乙醇。回答下列问题:
(1)滤液①的溶质为H2SO4和_______ 、_______ (填化学式)。
(2)“提纯”步骤中所有可能的反应的离子方程式为_______ 、__________ 。
(3)加入乙醇的目的是_______ 。
(4)“氧化”步骤中主要反应的化学方程式为_______ 。
(5)按照以上流程回收处理1 kg铁泥(含Fe元素的质量分数为56%),得到890 g纯度为95%的产品,Fe元素的回收率为_______ 。
(6)镍铁电池放电时也可产生FeO(OH),其工作原理如图所示。 放电生成FeO(OH)2后,继续放电时,电极上的FeO(OH)2可转化为FeO(OH),写出该过程的电极反应式
放电生成FeO(OH)2后,继续放电时,电极上的FeO(OH)2可转化为FeO(OH),写出该过程的电极反应式_______ 。
 、
、 、SiO2)为原料制备FeO(OH)的流程如图所示。
、SiO2)为原料制备FeO(OH)的流程如图所示。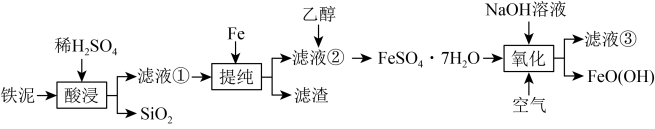
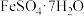 溶于水,不溶于乙醇。回答下列问题:
溶于水,不溶于乙醇。回答下列问题:(1)滤液①的溶质为H2SO4和
(2)“提纯”步骤中所有可能的反应的离子方程式为
(3)加入乙醇的目的是
(4)“氧化”步骤中主要反应的化学方程式为
(5)按照以上流程回收处理1 kg铁泥(含Fe元素的质量分数为56%),得到890 g纯度为95%的产品,Fe元素的回收率为
(6)镍铁电池放电时也可产生FeO(OH),其工作原理如图所示。
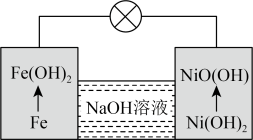
 放电生成FeO(OH)2后,继续放电时,电极上的FeO(OH)2可转化为FeO(OH),写出该过程的电极反应式
放电生成FeO(OH)2后,继续放电时,电极上的FeO(OH)2可转化为FeO(OH),写出该过程的电极反应式
您最近半年使用:0次
10 . 草酸是一种二元弱酸,可用作还原剂、沉淀剂等。某校课外小组的同学设计利用C2H2气体制取H2C2O4·2H2O。回答下列问题:
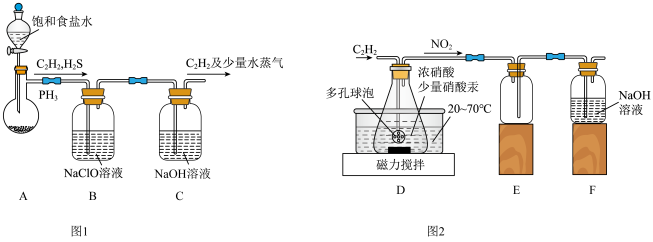
(1)甲组的同学以电石(主要成分CaC2,少量CaS及Ca3P2杂质等)为原料,并用下图1装置制取C2H2。___________ (写一种即可)。
②装置B中,NaClO将H2S、PH3 氧化为硫酸及磷酸,本身被还原为NaCl,其中PH3被氧化的离子方程式为___________ 。该过程中,可能产生新的杂质气体Cl2,其原因是:___________ (用离子方程式回答)。
(2)乙组的同学根据文献资料,用Hg(NO3)2作催化剂,浓硝酸氧化C2H2制取H2C2O4·2H2O。制备装置如上图2所示:
①装置D中多孔球泡的作用是___________ 。
②装置D中生成H2C2O4的化学方程式为___________ 。
③从装置D中得到产品,还需经过___________ (填操作名称)、过滤、洗涤及干燥。
(3)丙组设计了测定乙组产品中H2C2O4·2H2O的质量分数实验。他们的实验步骤如下:准确称取m g产品于锥形瓶中,加入适量的蒸馏水溶解,再加入少量稀硫酸,然后用c mol·L-1酸性KMnO4标准溶液进行滴定至终点,共消耗标准溶液V mL。
①滴定终点的现象是___________ 。
②产品中H2C2O4·2H2O的质量分数为___________ (列出含 m、c、V 的表达式)。
(1)甲组的同学以电石(主要成分CaC2,少量CaS及Ca3P2杂质等)为原料,并用下图1装置制取C2H2。
②装置B中,NaClO将H2S、PH3 氧化为硫酸及磷酸,本身被还原为NaCl,其中PH3被氧化的离子方程式为
(2)乙组的同学根据文献资料,用Hg(NO3)2作催化剂,浓硝酸氧化C2H2制取H2C2O4·2H2O。制备装置如上图2所示:
①装置D中多孔球泡的作用是
②装置D中生成H2C2O4的化学方程式为
③从装置D中得到产品,还需经过
(3)丙组设计了测定乙组产品中H2C2O4·2H2O的质量分数实验。他们的实验步骤如下:准确称取m g产品于锥形瓶中,加入适量的蒸馏水溶解,再加入少量稀硫酸,然后用c mol·L-1酸性KMnO4标准溶液进行滴定至终点,共消耗标准溶液V mL。
①滴定终点的现象是
②产品中H2C2O4·2H2O的质量分数为
您最近半年使用:0次



