1 . 科学探究要实事求是、严谨细致。某化学兴趣小组设计实验进行有关氯化物的探究实验,回答下列问题:
Ⅰ.FeCl3在工业生产中应用广泛,某化学研究性学习小组模拟工业流程制备无水FeCl3。经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了以Fe粉和Cl2为原料制备无水FeCl3的实验方案,装置示意图如下:___________ 。
(2)装置A中设计g管的作用是___________ 。
(3)装置A中发生反应的离子方程式为___________ 。
Ⅱ.利用惰性电极电解0.1mol/LFeCl2溶液,探究外界条件对电极反应(离子放电顺序)的影响。
实验数据如表所示:
(4)由实验1、2现象可以得出结论:增大pH,___________ 优先于___________ 放电;
Ⅲ.为了探究外界条件对氯化铵水解平衡的影响,兴趣小组设计了如下实验方案:
(5)该实验限选药品和仪器:恒温水浴、pH传感器、烧杯、0.1mol/L硝酸银溶液、蒸馏水和各种浓度的NH4Cl溶液。
①实验中,“待测物理量X”是___________ ;
②为了探究浓度对氯化铵水解平衡的影响,实验6可与实验___________ 作对照实验;
③实验目的ii是___________ ;
④氯化铵在生产生活中有很多实用的用途,请写出一种应用:___________ 。
Ⅰ.FeCl3在工业生产中应用广泛,某化学研究性学习小组模拟工业流程制备无水FeCl3。经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了以Fe粉和Cl2为原料制备无水FeCl3的实验方案,装置示意图如下:
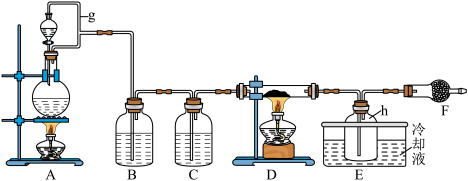
(2)装置A中设计g管的作用是
(3)装置A中发生反应的离子方程式为
Ⅱ.利用惰性电极电解0.1mol/LFeCl2溶液,探究外界条件对电极反应(离子放电顺序)的影响。
实验数据如表所示:
| 实验编号 | 电压/V | pH | 阳极现象 | 阴极现象 |
| 1 | 1.5 | 1.00 | 无气泡,滴加KSCN显红色 | 较多气泡,极少量金属析出 |
| 2 | 1.5 | 5.52 | 无气泡,滴加KSCN显红色 | 无气泡,银白色金属析出 |
| 3 | 3.0 | 5.52 | 少量气泡,滴加KSCN显红色 | 无气泡,银白色金属析出 |
| 4 | 4.5 | 5.52 | 大量气泡,滴加KSCN显红色 | 较多气泡,极少量金属析出 |
(4)由实验1、2现象可以得出结论:增大pH,
Ⅲ.为了探究外界条件对氯化铵水解平衡的影响,兴趣小组设计了如下实验方案:
| 实验编号 | c(NH4Cl)/mol·L-1 | 温度/℃ | 待测物理量X | 实验目的 |
| 5 | 0.5 | 30 | a | ___________ |
| 6 | 1.5 | i | b | 探究浓度对氯化铵水解平衡的影响 |
| 7 | 1.5 | 35 | c | ii |
| 8 | 2.0 | 40 | d | 探究温度、浓度同时对氯化铵化解平衡的影响 |
(5)该实验限选药品和仪器:恒温水浴、pH传感器、烧杯、0.1mol/L硝酸银溶液、蒸馏水和各种浓度的NH4Cl溶液。
①实验中,“待测物理量X”是
②为了探究浓度对氯化铵水解平衡的影响,实验6可与实验
③实验目的ii是
④氯化铵在生产生活中有很多实用的用途,请写出一种应用:
您最近一年使用:0次
名校
2 . 氧化亚铜和溴化亚铜均是常见的一价铜化合物,氧化亚铜在强酸性溶液中易发生歧化反应,溴化亚铜常用作有机合成原料和反应催化剂。
(1)可利用葡萄糖还原CuSO4溶液制备氧化亚铜。
①配制490mL0.1mol·L-1CuSO4溶液,需要称取胆矾晶体的质量为___________ g。
②某同学为检验CuO样品中是否含有Cu2O,可向样品中加入足量稀硫酸,若观察到___________ ,则说明样品中含有Cu2O杂质。
(2)向CuSO4和NaBr的混合溶液中通入足量的二氧化硫可得到溴化亚铜沉淀。完成该反应的离子方程式:___________ 。
_______Cu2++_______Br-+_______SO2+_______H2O=______CuBr↓+_____ +_________。
+_________。
该反应完毕的现象标志是___________ ,洗涤CuBr沉淀时采用二氧化硫的水溶液而不采用蒸馏水的目的是___________ 。
(3)某小组同学取含有少量CuO杂质的Cu2O样品进行如下实验,以测定氧化亚铜的纯度。
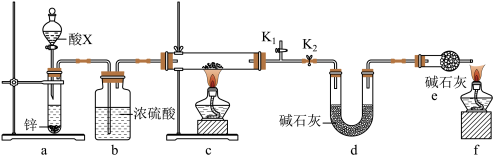
①装置a中所加的酸X是___________ (填化学式)。
②通过测定下列物理量,能达到实验目的的是___________ (填字母)。
A.反应前后装置a的质量 B.充分反应后装置c所得固体的质量
C.反应前后装置d的质量 D.反应前后装置e的质量
③点燃酒精灯前涉及的部分操作如下,正确的顺序是___________ 。
①打开K2:关闭K1②检查装置的气密性③连接仪器④关闭K2,打开K1,通氢气一段时间。
(1)可利用葡萄糖还原CuSO4溶液制备氧化亚铜。
①配制490mL0.1mol·L-1CuSO4溶液,需要称取胆矾晶体的质量为
②某同学为检验CuO样品中是否含有Cu2O,可向样品中加入足量稀硫酸,若观察到
(2)向CuSO4和NaBr的混合溶液中通入足量的二氧化硫可得到溴化亚铜沉淀。完成该反应的离子方程式:
_______Cu2++_______Br-+_______SO2+_______H2O=______CuBr↓+_____
 +_________。
+_________。该反应完毕的现象标志是
(3)某小组同学取含有少量CuO杂质的Cu2O样品进行如下实验,以测定氧化亚铜的纯度。

①装置a中所加的酸X是
②通过测定下列物理量,能达到实验目的的是
A.反应前后装置a的质量 B.充分反应后装置c所得固体的质量
C.反应前后装置d的质量 D.反应前后装置e的质量
③点燃酒精灯前涉及的部分操作如下,正确的顺序是
①打开K2:关闭K1②检查装置的气密性③连接仪器④关闭K2,打开K1,通氢气一段时间。
您最近一年使用:0次
3 . 根据下列实验操作和现象能推出相应结论或目的的是
| 选项 | 实验操作和现象 | 实验目的或结论 |
| A | 向 溶液中滴加 溶液中滴加 溶液,产生白色沉淀 溶液,产生白色沉淀 |  和 和 发生了相互促进的水解反应 发生了相互促进的水解反应 |
| B | 向 溶液中加入 溶液中加入 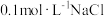 溶液,出现白色沉淀,再加入几滴 溶液,出现白色沉淀,再加入几滴 的 的 溶液,有黑色沉淀生成 溶液,有黑色沉淀生成 | 证明 的溶解度大于 的溶解度大于 的溶解度 的溶解度 |
| C | 向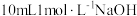 溶液中滴加饱和 溶液中滴加饱和 溶液,有红褐色物质产生 溶液,有红褐色物质产生 | 制备 胶体 胶体 |
| D | 向 溶液中通入 溶液中通入 气体,产生黑色沉淀 气体,产生黑色沉淀 | 氢硫酸为强酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-07更新
|
547次组卷
|
6卷引用:福建省莆田市2022-2023学年高三毕业班第四次教学质量检测化学试题
名校
解题方法
4 . 某化学研究性学习小组设计实验探究铜的常见化学性质,过程设计如下所示:
【提出猜想】
问题1:在周期表中,铜与铝的位置很靠近,铜不如铝活泼,氢氧化铝具有两性。那么,氢氧化铜也具有两性吗?
问题2:铁和铜都有变价,一般情况下,正二价铁的稳定性小于正三价铁的稳定性。那么,正一价铜的稳定性也小于正二价铜的稳定性吗?
问题3:氧化铜具有氧化性,能被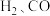 还原。那么,氧化铜也能被氮的某种气态氢化物还原吗?
还原。那么,氧化铜也能被氮的某种气态氢化物还原吗?
【实验探究】
Ⅰ.解决问题1
(1)需用到的药品除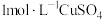 溶液、稀硫酸外,还需
溶液、稀硫酸外,还需____________ (填试剂的化学式)溶液。
(2)为达到本实验目的,你认为应进行的相关实验是(填实验内容):
①__________________ ;②__________________ 。
Ⅱ.解决问题2
取一定量制得的氢氧化铜固体,于坩埚中灼烧,当温度达到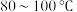 时得到黑色固体粉末;继续加热至
时得到黑色固体粉末;继续加热至 以上,黑色粉末全部变成红色粉末氧化亚铜;取适量红色氧化亚铜粉末于洁浄试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液,同时观察到试管底部还有红色固体存在。根据以上实验现象回答问题:
以上,黑色粉末全部变成红色粉末氧化亚铜;取适量红色氧化亚铜粉末于洁浄试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液,同时观察到试管底部还有红色固体存在。根据以上实验现象回答问题:
(3)写出氧化亚铜与稀硫酸(或盐酸)反应的离子方程式:______________________________ 。
(4)从实验Ⅱ可得出的结论是:__________________________________________ 。
(5)往蓝色溶液中逐滴加入过量的氨水,发生反应的离子方程式为:______________ 、______________ 。
Ⅲ.解决问题3
设计如图装置(夹持装置未画出):

当氮的某种气态氢化物(X)缓缓通过灼热的氧化铜时,观察到氧化铜由黑色变成了红色,无水 变成了蓝色,生成物中还有一种无污染的单质气体Y;将X通入灼热的
变成了蓝色,生成物中还有一种无污染的单质气体Y;将X通入灼热的 燃烧管完全反应后,消耗
燃烧管完全反应后,消耗 ,测得B装置增重
,测得B装置增重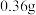 ,并收集到
,并收集到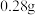 单质气体Y。
单质气体Y。
(6)C装置中发生反应的化学方程式为________________________________ 。
【提出猜想】
问题1:在周期表中,铜与铝的位置很靠近,铜不如铝活泼,氢氧化铝具有两性。那么,氢氧化铜也具有两性吗?
问题2:铁和铜都有变价,一般情况下,正二价铁的稳定性小于正三价铁的稳定性。那么,正一价铜的稳定性也小于正二价铜的稳定性吗?
问题3:氧化铜具有氧化性,能被
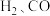 还原。那么,氧化铜也能被氮的某种气态氢化物还原吗?
还原。那么,氧化铜也能被氮的某种气态氢化物还原吗?【实验探究】
Ⅰ.解决问题1
(1)需用到的药品除
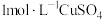 溶液、稀硫酸外,还需
溶液、稀硫酸外,还需(2)为达到本实验目的,你认为应进行的相关实验是(填实验内容):
①
Ⅱ.解决问题2
取一定量制得的氢氧化铜固体,于坩埚中灼烧,当温度达到
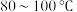 时得到黑色固体粉末;继续加热至
时得到黑色固体粉末;继续加热至 以上,黑色粉末全部变成红色粉末氧化亚铜;取适量红色氧化亚铜粉末于洁浄试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液,同时观察到试管底部还有红色固体存在。根据以上实验现象回答问题:
以上,黑色粉末全部变成红色粉末氧化亚铜;取适量红色氧化亚铜粉末于洁浄试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液,同时观察到试管底部还有红色固体存在。根据以上实验现象回答问题:(3)写出氧化亚铜与稀硫酸(或盐酸)反应的离子方程式:
(4)从实验Ⅱ可得出的结论是:
(5)往蓝色溶液中逐滴加入过量的氨水,发生反应的离子方程式为:
Ⅲ.解决问题3
设计如图装置(夹持装置未画出):

当氮的某种气态氢化物(X)缓缓通过灼热的氧化铜时,观察到氧化铜由黑色变成了红色,无水
 变成了蓝色,生成物中还有一种无污染的单质气体Y;将X通入灼热的
变成了蓝色,生成物中还有一种无污染的单质气体Y;将X通入灼热的 燃烧管完全反应后,消耗
燃烧管完全反应后,消耗 ,测得B装置增重
,测得B装置增重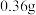 ,并收集到
,并收集到 单质气体Y。
单质气体Y。(6)C装置中发生反应的化学方程式为
您最近一年使用:0次
名校
解题方法
5 . 下列实验装置或操作能达到实验目的的是
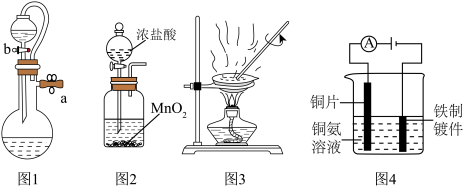
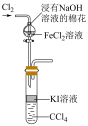
| A.图1,关闭a、打开b,检查装置气密性 | B.图2,制备氯气 |
C.图3,蒸干 溶液制 溶液制 | D.图4,铁件镀铜 |
您最近一年使用:0次
2024-03-21更新
|
596次组卷
|
3卷引用:福建省永春一中2023-2024学年高三化学最后一卷试卷
福建省永春一中2023-2024学年高三化学最后一卷试卷山东省淄博市2024届高三一模化学试题(已下线)压轴题09?微型化学实验设计与评价(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
名校
6 . 下列实验操作正确且能达到实验目的的是
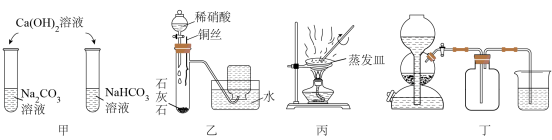

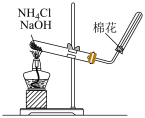
A.用甲装置鉴别 溶液和 溶液和 溶液 溶液 |
| B.用乙装置验证稀硝酸的还原产物为NO |
C.用丙装置除去NaCl固体中的 |
D.利用 固体和浓硫酸制备 固体和浓硫酸制备 气体 气体 |
您最近一年使用:0次
名校
7 . 下列实验方案中能达到实验目的的是
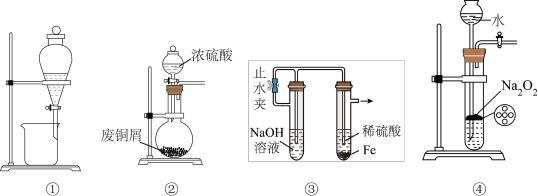

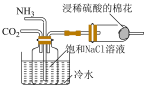
| A.用装置①分离饱和Na2CO3溶液和CH3COOC2H5 |
| B.用装置②制取SO2 |
| C.用装置③制备氢氧化亚铁沉淀 |
| D.用装置④制备O2 |
您最近一年使用:0次
名校
解题方法
8 . 下列装置正确并能达到实验目的的是
|
|
|
|
| 甲 | 乙 | 丙 | 丁 |
| A.图甲装置可用于实验室制取并收集NH3 |
| B.图乙装置可用于制备NaHCO3,其中CO2分子为直线形 |
| C.图丙装置可用于比较碳、硅元素非金属性大小 |
| D.图丁装置试管下层出现紫红色,可证明氧化性:Cl2>Fe3+>I2 |
您最近一年使用:0次
2023-10-05更新
|
69次组卷
|
2卷引用:福建省厦门第一中学2024届高三上学期10 月月考化学试题
名校
解题方法
9 . 利用下列装置(夹持装置略)进行实验,能达到实验目的的是
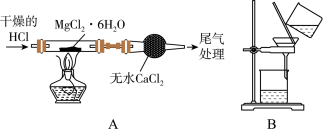
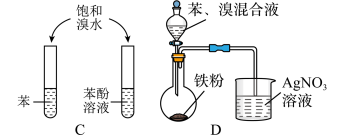


| A.制备无水MgCl2 |
| B.除去 Fe(OH)3胶体中的 NaCl 溶液 |
| C.证明苯环使羟基活化 |
| D.制备溴苯并验证有 HBr 产生 |
您最近一年使用:0次
名校
解题方法
10 . 下列实验方案能达到实验目的的是
| 选项 | A | B | C | D |
| 目的 | 装置可以干燥 气体 气体 | 证明温度对平衡的影响 | 实验室快速制备 | 制备氢氧化铁胶体 |
| 实验方案 |  | 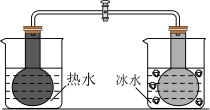 | 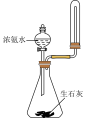 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-11-18更新
|
183次组卷
|
2卷引用:福建省厦门市松柏中学2023-2024学年高三上学期第三次月考化学试卷