解题方法
1 . 下列化学实验事实及其结论中正确的是
| A.将稀盐酸滴入硅酸钠溶液中,充分振荡,有白色沉淀产生,证明非金属性:Cl>Si |
| B.向SO2水溶液中滴加盐酸和Ba(NO3)2溶液,有白色沉淀生成,证明BaSO3难溶于酸 |
| C.向2.0mL浓度均为0.1mol·L-1的KCl、KI混合溶液中滴加1~2滴0.01mol·L-1 AgNO3溶液,振荡后沉淀呈黄色,证明Ksp(AgCl)>Ksp(AgI) |
| D.将漂白粉样品溶于水,加入盐酸和KI溶液,再加入CCl4振荡,静置,下层液体呈紫红色,证明样品未变质 |
您最近一年使用:0次
2 . 氯气(Cl2)是一种能溶于水的有毒气体,它能与水发生反应生成盐酸(HCl)和次氯酸(HClO),次氯酸(HClO) 具有漂白性,能使品红等有色物质褪色。
(1)向含有酚酞的NaOH溶液中逐滴滴入饱和氯水(氯气的水溶液),发现溶液会由红色褪成无色,请根据以上信息猜想溶液变成无色的两个可能原因(用简要文字说明);
①___________ ;
②___________ 。
(2)请设计一个简单的实验,验证(1) 中猜想:___________ 。
(3)工业制取漂白粉的原理为2Cl2+2Ca (OH)2 =CaCl2+Ca (C1O)2+2H2O, 漂白粉的有效成分是次氯酸钙Ca (ClO)2 ,它能与酸发生复分解反应生成HClO。在空气中容易吸收水和CO2发生反应:Ca (ClO) 2+CO2+H2O=CaCO3 ↓+2HClO, HClO是一种酸性比盐酸弱的酸,不稳定、易分解。
①HClO在常温下分解,发生反应:2HClO=2HCl+O2↑。某瓶HClO溶液放置一段时间后,溶液的pH会___________ (填 “增大”或“减小”或“不变”)。
②实验室有一包长时间放置的漂白粉,某同学设计了下列实验探究该漂白粉是否变质。
[提出问题]长时间放置的漂白粉是否变质?
[作出猜想]猜想1:该漂白粉未未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为___________ ;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3。
[实验探究]
[反思评价]I.有同学认为无需进行操作步骤②,只需在步骤①反应后的溶液中滴加适量品红,观察品红是否褪色即可,理由是___________ (用化学方程式表示)。
II.漂白粉在保存时一定要注意___________ 。
(1)向含有酚酞的NaOH溶液中逐滴滴入饱和氯水(氯气的水溶液),发现溶液会由红色褪成无色,请根据以上信息猜想溶液变成无色的两个可能原因(用简要文字说明);
①
②
(2)请设计一个简单的实验,验证(1) 中猜想:
(3)工业制取漂白粉的原理为2Cl2+2Ca (OH)2 =CaCl2+Ca (C1O)2+2H2O, 漂白粉的有效成分是次氯酸钙Ca (ClO)2 ,它能与酸发生复分解反应生成HClO。在空气中容易吸收水和CO2发生反应:Ca (ClO) 2+CO2+H2O=CaCO3 ↓+2HClO, HClO是一种酸性比盐酸弱的酸,不稳定、易分解。
①HClO在常温下分解,发生反应:2HClO=2HCl+O2↑。某瓶HClO溶液放置一段时间后,溶液的pH会
②实验室有一包长时间放置的漂白粉,某同学设计了下列实验探究该漂白粉是否变质。
[提出问题]长时间放置的漂白粉是否变质?
[作出猜想]猜想1:该漂白粉未未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3。
[实验探究]
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,加入适量 | 有气体产生,气体使石灰水变浑浊。 | 猜想2成立 |
| ②把少量样品加入水中,通入足量的CO2气体后,再滴入适量的品红溶液 |
II.漂白粉在保存时一定要注意
您最近一年使用:0次
名校
解题方法
3 .  俗称大苏打、海波,易溶于水,在中性或碱性环境中能稳定存在,食品工业用作螯合剂、抗氧化剂,医药工业用作洗涤剂、消毒剂。下列说法中根据实验目的、实验操作或现象得到的相关离子方程式正确的是
俗称大苏打、海波,易溶于水,在中性或碱性环境中能稳定存在,食品工业用作螯合剂、抗氧化剂,医药工业用作洗涤剂、消毒剂。下列说法中根据实验目的、实验操作或现象得到的相关离子方程式正确的是
 俗称大苏打、海波,易溶于水,在中性或碱性环境中能稳定存在,食品工业用作螯合剂、抗氧化剂,医药工业用作洗涤剂、消毒剂。下列说法中根据实验目的、实验操作或现象得到的相关离子方程式正确的是
俗称大苏打、海波,易溶于水,在中性或碱性环境中能稳定存在,食品工业用作螯合剂、抗氧化剂,医药工业用作洗涤剂、消毒剂。下列说法中根据实验目的、实验操作或现象得到的相关离子方程式正确的是| 选项 | 实验目的 | 实验操作或现象 | 相关离子方程式 |
| A | 制备 | 实验室用 通入 通入 和 和 的混合溶液中来制备 的混合溶液中来制备 | 4SO2+2S2-+CO =3S2O =3S2O +CO2 +CO2 |
| B | 检验硫代硫酸钠氧化变质可能混有的 | 取少量样品溶于水,先加入过量稀盐酸,再滴加 溶液,有沉淀生成 溶液,有沉淀生成 | SO +Ba2+=BaSO4↓ +Ba2+=BaSO4↓ |
| C | 探究温度对硫代硫酸钠与硫酸反应速率的影响 | 分别将两种反应溶液先混合,再水浴加热至反应要求温度,测得该温度下的反应速率 | 2S2O +2H+=S↓+SO +2H+=S↓+SO +2H2O +2H2O |
| D | 用过量硫代硫酸钠除去水中溶解的氯气 | 黄绿色褪去 | S2O +4Cl2+5H2O=2SO +4Cl2+5H2O=2SO +8Cl-+10H+ +8Cl-+10H+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-11更新
|
2451次组卷
|
7卷引用:湖南省四大名校名师团队2022-2023学年高三下学期2月模拟冲刺卷(1)化学试题
湖南省四大名校名师团队2022-2023学年高三下学期2月模拟冲刺卷(1)化学试题(已下线)素养卷09 微型原理验证方案设计-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)专题04 离子反应湖南省部分学校2022-2023学年高三下学期开学考试化学试题湖南省衡阳市第八中学2023-2024学年高三上学期开学(暑假检测)化学试题江苏省靖江高级中学、华罗庚中学2023-2024学年高三上学期第一次阶段考试化学试题江西省新余市第一中学2023-2024学年高三上学期开学考试化学试题
名校
解题方法
4 .  和焦亚硫酸钠
和焦亚硫酸钠 可用作食品添加剂。回答下列问题:
可用作食品添加剂。回答下列问题:
(1)实验室用 和
和 制取
制取 的化学方程式为
的化学方程式为_______ 。欲净化与收集 ,选择必要装置,按气流方向连接顺序为
,选择必要装置,按气流方向连接顺序为_______ (填仪器接口的字母编号)。
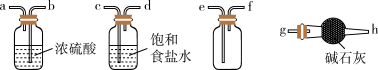
(2)①焦亚硫酸钠易被氧化而变质,选用下列试剂设计实验方案,检验焦亚硫酸钠样品氧化变质的程度。已知: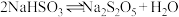 。
。
试剂:稀盐酸、稀 、稀
、稀 、
、 溶液、酸性
溶液、酸性 溶液、
溶液、 溶液
溶液
② 是常用的食品添加剂,常用于葡萄酒、果脯、拉面等食品中。为检验某白葡萄酒中是否含有
是常用的食品添加剂,常用于葡萄酒、果脯、拉面等食品中。为检验某白葡萄酒中是否含有 能否用酸性
能否用酸性 溶液检验?作出判断并说明理由
溶液检验?作出判断并说明理由_______ 。
(3)某小组利用下列装置测定空气中 的含量。
的含量。
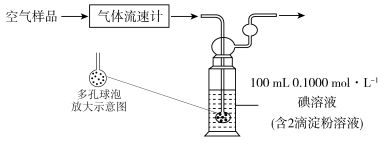
通空气样品的导管末端是带许多小孔的玻璃球泡,其主要作用是_______ ;该装置中发生的离子方程式为:_______ 。若空气流速为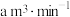 ,当观察到
,当观察到_______ 时,结束计时,测定耗时t min。假定样品中的 可被溶液充分吸收,该空气样品中
可被溶液充分吸收,该空气样品中 的含量是
的含量是_______ 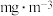 。
。
 和焦亚硫酸钠
和焦亚硫酸钠 可用作食品添加剂。回答下列问题:
可用作食品添加剂。回答下列问题:(1)实验室用
 和
和 制取
制取 的化学方程式为
的化学方程式为 ,选择必要装置,按气流方向连接顺序为
,选择必要装置,按气流方向连接顺序为
(2)①焦亚硫酸钠易被氧化而变质,选用下列试剂设计实验方案,检验焦亚硫酸钠样品氧化变质的程度。已知:
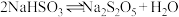 。
。试剂:稀盐酸、稀
 、稀
、稀 、
、 溶液、酸性
溶液、酸性 溶液、
溶液、 溶液
溶液| 实验编号 | 实验步骤 | 现象 | 结论 |
| Ⅰ | 取少量样品,加入除氧蒸馏水 | 固体完全溶解得到无色溶液 | / |
| Ⅱ | 取实验Ⅰ的溶液, | 样品已氧化变质 | |
| Ⅲ | 另取实验Ⅰ的溶液,加入酸性KMnO4溶液 | 溶液褪色 | 样品未完全氧化变质 |
 是常用的食品添加剂,常用于葡萄酒、果脯、拉面等食品中。为检验某白葡萄酒中是否含有
是常用的食品添加剂,常用于葡萄酒、果脯、拉面等食品中。为检验某白葡萄酒中是否含有 能否用酸性
能否用酸性 溶液检验?作出判断并说明理由
溶液检验?作出判断并说明理由(3)某小组利用下列装置测定空气中
 的含量。
的含量。
通空气样品的导管末端是带许多小孔的玻璃球泡,其主要作用是
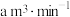 ,当观察到
,当观察到 可被溶液充分吸收,该空气样品中
可被溶液充分吸收,该空气样品中 的含量是
的含量是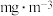 。
。
您最近一年使用:0次
2022-05-23更新
|
452次组卷
|
4卷引用:天津市滨海新区2022届普通高考模拟试卷化学试题
天津市滨海新区2022届普通高考模拟试卷化学试题天津市高三九校2022届高三第二次模拟考试化学试题湖南省娄底市新化县第一中学2021-2022学年高三下学期模拟考试化学试题(已下线)专题16 化学实验综合题-2022年高考真题模拟题分项汇编
5 . 氯化亚铜(CuCl)广泛用于冶金、电镀、医药等行业。已知CuCl难溶于水和乙醇,在潮湿空气中易变质。学习小组开展了与CuCl相关的系列实验,回答下列问题:
I.利用废铜屑制备CuCl2,实验装置如图所示。
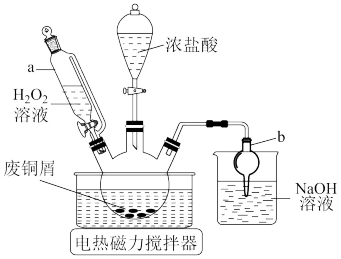
(1)仪器a的名称为___ 。仪器b的作用是___ 。
(2)三颈烧瓶中制备CuCl2的化学方程式为___ 。
II.制备氯化亚铜,制备流程如图所示:
CuCl2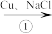 Na[CuCl2]
Na[CuCl2]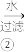 CuCl粗产品
CuCl粗产品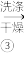 CuCl
CuCl
(3)反应①中氧化剂为___ (填化学式)。
(4)Na[CuCl2]溶液中存在的平衡是___ (用离子方程式表示)。
(5)析出的CuCl粗产品不用盐酸而用水、乙醇分别洗涤的目的依次是___ 、___ 。
(6)测定产品中CuCl的质量分数。准确称取制备的CuCl产品0.40g,加入足量的氯化铁溶液,待样品全部溶解后,加入适量稀硫酸,用0.15 mol·L-1的Ce(SO4)2标准溶液滴定至终点,消耗Ce(SO4)2溶液24.00 mL,反应中Ce4+被还原为Ce3+。硫酸铈标准溶液应盛放在___ (填“酸式”或“碱式”)滴定管中。产品中CuCl的质量分数为___ 。
I.利用废铜屑制备CuCl2,实验装置如图所示。

(1)仪器a的名称为
(2)三颈烧瓶中制备CuCl2的化学方程式为
II.制备氯化亚铜,制备流程如图所示:
CuCl2
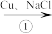 Na[CuCl2]
Na[CuCl2]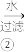 CuCl粗产品
CuCl粗产品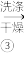 CuCl
CuCl(3)反应①中氧化剂为
(4)Na[CuCl2]溶液中存在的平衡是
(5)析出的CuCl粗产品不用盐酸而用水、乙醇分别洗涤的目的依次是
(6)测定产品中CuCl的质量分数。准确称取制备的CuCl产品0.40g,加入足量的氯化铁溶液,待样品全部溶解后,加入适量稀硫酸,用0.15 mol·L-1的Ce(SO4)2标准溶液滴定至终点,消耗Ce(SO4)2溶液24.00 mL,反应中Ce4+被还原为Ce3+。硫酸铈标准溶液应盛放在
您最近一年使用:0次
2022-01-08更新
|
274次组卷
|
3卷引用:河北省名校联盟2021-2022学年高三上学期一轮复习考试化学试题
6 . 下列方案设计、现象和结论都正确的是
| 选项 | 目的 | 方案设计 | 现象和结论 |
| A | 探究金属钠在氧气中燃烧所得固体粉末的成分 | 取少量固体粉末,加入2~3mL蒸馏水 | 若无气体生成,则固体粉末为Na2O;若有气体生成,则固体粉末为Na2O2 |
| B | 探究Ag+与Fe3+氧化性的强弱 | 向FeCl2和KSCN的混合溶液中滴入酸化的AgNO3溶液 | 溶液变红,说明氧化性Ag+> Fe3+ |
| C | 探究乙醇消去反应的产物 | 取4mL乙醇,加入12mL浓硫酸、少量沸石,迅速升温至140℃,将产生的气体通入2mL溴水中 | 若溴水褪色,则乙醇消去反应的产物为乙烯 |
| D | 探究Na2SO3固体样品是否变质 | 取少量待测液样品溶于蒸馏水中,加入足量稀盐酸,再加入足量BaCl2溶液 | 若有白色沉淀产生,则样品已经变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . 盐酸和氢氧化钠是工业上重要的化工原料,也是实验室里常见的试剂。
I.欲使用0.30mol/L的 溶液950mL,现拟用36.5%(
溶液950mL,现拟用36.5%(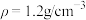 )的浓盐酸来配制,请回答下列问题:
)的浓盐酸来配制,请回答下列问题:
(1)配制溶液所用36.5%的盐酸的体积为_______ 。
(2)该实验需要使用到的玻璃仪器有:烧杯、玻璃棒、胶头滴管、_______ 。
(3)下列操作会使所配溶液浓度小于0.30mol/L的是:_______ 。(填对应的序号)
a、容量瓶用蒸馏水洗净后没有烘干,瓶内有少量残留的蒸馏水;
b、在操作中没有用蒸馏水洗涤烧杯和玻璃棒;
c、定容时视线俯视刻度线;
d、定容时加蒸馏水超过了刻度线,倒出一些溶液,再重新加蒸馏水定容到刻度线;
e、将配制好的溶液转入试剂瓶的过程中不慎洒出了少许溶液;
f、用量筒量取浓盐酸时视线仰视刻度线。
II.酸碱中和滴定
(4)某学生用盐酸标准液测定氢氧化钠待测液时,选择酚酞作指示剂。达到滴定终点的现象是_______ 。滴定时不必用到的仪器是_______ 。
A.酸式滴定管 B.容量瓶 C.锥形瓶 D.铁架台
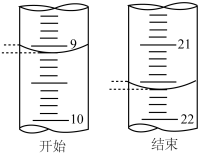
(5)若滴定开始和结束时,酸式滴定管中的液面如图所示,此时消耗盐酸的体积为_______ mL。已知用 的盐酸标定25mL的氢氧化钠溶液,则测得
的盐酸标定25mL的氢氧化钠溶液,则测得 为
为_______  。
。
III.为了测定摩尔盐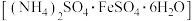 产品的纯度,称取ag样品溶于水,配制成500mL溶液,用浓度为
产品的纯度,称取ag样品溶于水,配制成500mL溶液,用浓度为 的酸性
的酸性 溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
(6)滴定过程中发生反应的离子方程式为_______ 。
(7)通过实验数据计算该产品的纯度:_______ (用含字母a、c的式子表示,用M表示摩尔盐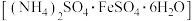 的摩尔质量)。上表第一次实验中记录的数据明显大于后两次,其原因可能是
的摩尔质量)。上表第一次实验中记录的数据明显大于后两次,其原因可能是_______ 。
A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低
I.欲使用0.30mol/L的
 溶液950mL,现拟用36.5%(
溶液950mL,现拟用36.5%(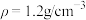 )的浓盐酸来配制,请回答下列问题:
)的浓盐酸来配制,请回答下列问题:(1)配制溶液所用36.5%的盐酸的体积为
(2)该实验需要使用到的玻璃仪器有:烧杯、玻璃棒、胶头滴管、
(3)下列操作会使所配溶液浓度小于0.30mol/L的是:
a、容量瓶用蒸馏水洗净后没有烘干,瓶内有少量残留的蒸馏水;
b、在操作中没有用蒸馏水洗涤烧杯和玻璃棒;
c、定容时视线俯视刻度线;
d、定容时加蒸馏水超过了刻度线,倒出一些溶液,再重新加蒸馏水定容到刻度线;
e、将配制好的溶液转入试剂瓶的过程中不慎洒出了少许溶液;
f、用量筒量取浓盐酸时视线仰视刻度线。
II.酸碱中和滴定
(4)某学生用盐酸标准液测定氢氧化钠待测液时,选择酚酞作指示剂。达到滴定终点的现象是
A.酸式滴定管 B.容量瓶 C.锥形瓶 D.铁架台
(5)若滴定开始和结束时,酸式滴定管中的液面如图所示,此时消耗盐酸的体积为
 的盐酸标定25mL的氢氧化钠溶液,则测得
的盐酸标定25mL的氢氧化钠溶液,则测得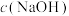 为
为 。
。
III.为了测定摩尔盐
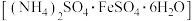 产品的纯度,称取ag样品溶于水,配制成500mL溶液,用浓度为
产品的纯度,称取ag样品溶于水,配制成500mL溶液,用浓度为 的酸性
的酸性 溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗高锰酸钾溶液体积/mL | 25.52 | 25.02 | 24.98 |
(7)通过实验数据计算该产品的纯度:
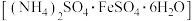 的摩尔质量)。上表第一次实验中记录的数据明显大于后两次,其原因可能是
的摩尔质量)。上表第一次实验中记录的数据明显大于后两次,其原因可能是A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低
您最近一年使用:0次
8 . 亚硫酸钠(Na2SO3)是印染工业中常用的脱氧剂和漂白剂。回答下列问题:
(1)实验室用H2SO4和NaHSO3制取SO2的化学方程式为:___________
(2)SO2可以与H2S反应,请写出其化学方程式:___________ 。
(3)亚硫酸钠易被氧化而变质为Na2SO4,选用下列试剂设计实验方案,检验亚硫酸钠样品氧化变质的程度。仅供选择的试剂:稀盐酸、稀H2SO4、稀HNO3、BaCl2溶液、酸性KMnO4溶液、H2O2溶液
(4)(Ga)与A1同主族,化学性质相似,是制造半导体材料氮化镓的重要原料,其中电解NaGaO2是获得Ga单质的重要方法,如图所示,则阴极的电极反应为:___________ 。若电解获得1molGa,则阳极产生的气体在标准状况下的体积至少为 ___________ L。

(1)实验室用H2SO4和NaHSO3制取SO2的化学方程式为:
(2)SO2可以与H2S反应,请写出其化学方程式:
(3)亚硫酸钠易被氧化而变质为Na2SO4,选用下列试剂设计实验方案,检验亚硫酸钠样品氧化变质的程度。仅供选择的试剂:稀盐酸、稀H2SO4、稀HNO3、BaCl2溶液、酸性KMnO4溶液、H2O2溶液
| 实验编号 | 实验步骤 | 现象 | 结论 |
| I | 取少量样品,加入除氧蒸馏水 | 固体完全溶解,得到无色溶液 | / |
| II | 取实验I的溶液, | 样品存在氧化变质 | |
| III | 另取实验I的溶液, | 样品并未完全氧化变质 |

您最近一年使用:0次
名校
解题方法
9 . 过氧化钠(Na2O2)常用作漂白剂、杀菌剂、供氧剂,能与水和二氧化碳等物质发生反应,保存不当时容易变质。某实验小组以过氧化钠为研究对象进行了如下实验。
(1)探究 Na2O2样品是否已经变质:Na2O2在空气中久置易变质生成_______ ,现取少量样品加水溶解,加入_______ 溶液,充分振荡后有白色沉淀,证明Na2O2已经变质。
(2)该实验小组为了粗略测定这包Na2O2样品的质量分数,称取了m g样品,并设计如图所示装置来测定过氧化钠的质量分数。
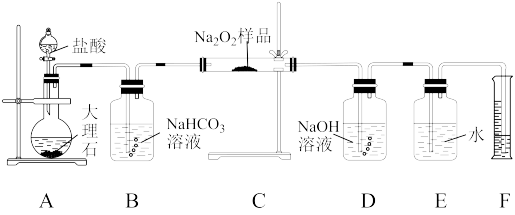
已知:饱和NaHCO3溶液的作用是除去CO2中的HCl气体,E和F是排水集气装置。
①写出装置C中发生的主要反应的化学方程式:_______ 。
②装置D的作用是_______ 。
③反应结束,待冷却后读出量筒内水的体积,将其折算成O2的质量为n g,则样品中过氧化钠的质量分数为_______ ×100%(用含m、n的最简式表示)。
(1)探究 Na2O2样品是否已经变质:Na2O2在空气中久置易变质生成
(2)该实验小组为了粗略测定这包Na2O2样品的质量分数,称取了m g样品,并设计如图所示装置来测定过氧化钠的质量分数。

已知:饱和NaHCO3溶液的作用是除去CO2中的HCl气体,E和F是排水集气装置。
①写出装置C中发生的主要反应的化学方程式:
②装置D的作用是
③反应结束,待冷却后读出量筒内水的体积,将其折算成O2的质量为n g,则样品中过氧化钠的质量分数为
您最近一年使用:0次
解题方法
10 . 过氧化钠常用作漂白剂、杀菌消毒剂,能与水和二氧化碳等物质发生反应,保存不当容易变质。某兴趣小组以过氧化钠为对象进行如下探究:
探究一: “干燥的CO2不能与Na2O2反应”和“CO2在有水存在时才能与Na2O2反应”,设计如下实验装置:
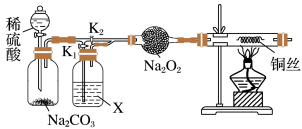
(1)连接装置,检查气密性。在干燥管中装入Na2O2后,打开活塞加入稀硫酸,生成CO2。打开K1,关闭K2,一段时间后再加热铜丝。其中,X中应加入试剂_________ (填名称)。先通一段时间CO2的目的是_________ ,实验观察到铜丝未变化,则得出结论“干燥的CO2不能与Na2O2反应”。
(2)若打开K2,关闭K1,出现_________ 现象,可证明“有水时CO2与Na2O2反应”产生了O2。
探究二: Na2O2是否已经变质并粗略测定该样品中Na2O2的质量分数
(3)甲同学取少量Na2O2样品,将其溶于水,加入_________ 溶液,充分振荡后有白色沉淀,证明Na2O2样品已经与空气中的CO2反应变质。
(4)乙同学为粗略测定该样品中Na2O2的质量分数,称取m g样品,设计如下装置进行实验:
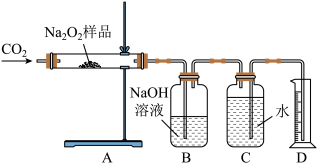
实验开始后,A中发生反应的化学方程式为:_________ ;利用装置B除去混合气体未反应的CO2;调整装置C、D内液面高度相同,读出量筒D中水的体积,并将其折算成氧气的质量为n g。则该样品中Na2O2的质量分数为: _________ 。
探究一: “干燥的CO2不能与Na2O2反应”和“CO2在有水存在时才能与Na2O2反应”,设计如下实验装置:

(1)连接装置,检查气密性。在干燥管中装入Na2O2后,打开活塞加入稀硫酸,生成CO2。打开K1,关闭K2,一段时间后再加热铜丝。其中,X中应加入试剂
(2)若打开K2,关闭K1,出现
探究二: Na2O2是否已经变质并粗略测定该样品中Na2O2的质量分数
(3)甲同学取少量Na2O2样品,将其溶于水,加入
(4)乙同学为粗略测定该样品中Na2O2的质量分数,称取m g样品,设计如下装置进行实验:

实验开始后,A中发生反应的化学方程式为:
您最近一年使用:0次



