名校
1 . 过氧化钠是重要的化工原料,具有杀菌、消毒等多种用途,请回答下列问题:
(1) 在空气中易变质,写出
在空气中易变质,写出 与
与 反应的化学方程式:
反应的化学方程式:______
(2)若将 投入到含有下列离子的溶液中:
投入到含有下列离子的溶液中: 、
、 、
、 、
、 、
、 、
、 ,反应完毕后,溶液中上述离子数目几乎不变的有
,反应完毕后,溶液中上述离子数目几乎不变的有______ (填离子符号)。
(3) 因保存不当易吸收空气中的
因保存不当易吸收空气中的 ,实验小组取样品m g,设计如图实验装置测定样品中
,实验小组取样品m g,设计如图实验装置测定样品中 的质量分数;
的质量分数;
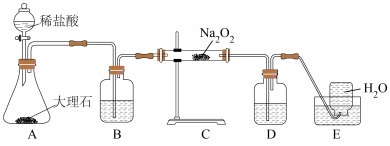
①将实验装置组装好后,必须进行的第一步操作是______ ;装置D中的试剂:______ ;
②反应结束后,测得生成气体的体积为V L(已折算为标准状况下的体积),则样品中 的质量分数为
的质量分数为______ 。
(1)
 在空气中易变质,写出
在空气中易变质,写出 与
与 反应的化学方程式:
反应的化学方程式:(2)若将
 投入到含有下列离子的溶液中:
投入到含有下列离子的溶液中: 、
、 、
、 、
、 、
、 、
、 ,反应完毕后,溶液中上述离子数目几乎不变的有
,反应完毕后,溶液中上述离子数目几乎不变的有(3)
 因保存不当易吸收空气中的
因保存不当易吸收空气中的 ,实验小组取样品m g,设计如图实验装置测定样品中
,实验小组取样品m g,设计如图实验装置测定样品中 的质量分数;
的质量分数;
①将实验装置组装好后,必须进行的第一步操作是
②反应结束后,测得生成气体的体积为V L(已折算为标准状况下的体积),则样品中
 的质量分数为
的质量分数为
您最近一年使用:0次
2023-12-01更新
|
82次组卷
|
2卷引用:山东省聊城市2023-2024学年高一上学期11月期中化学试题
名校
2 . 过氧化钠常作漂白剂、杀菌剂、消毒剂。过氧化钠保存不当容易吸收空气中 而变质。为了测定过氧化钠的纯度,称取ag样品并设计如图装置来测定过氧化钠的质量分数。
而变质。为了测定过氧化钠的纯度,称取ag样品并设计如图装置来测定过氧化钠的质量分数。
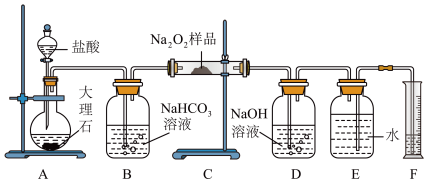
(1)将仪器连接好以后,必须进行的第一步操作是___________ 。
(2)装置C中发生反应的化学方程式为___________ 、___________ 。
(3)D中NaOH溶液的作用为___________ 。
(4)实验结束时,读取实验中生成气体的体积时,不合理的是___________ 。
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.读取量筒中水的体积时,应使视线与凹液面的最低点相平
(5)读出量筒内水的体积后,折算成标准状况下氧气的体积为 ,则样品中过氧化钠的质量分数为
,则样品中过氧化钠的质量分数为___________ 。
 而变质。为了测定过氧化钠的纯度,称取ag样品并设计如图装置来测定过氧化钠的质量分数。
而变质。为了测定过氧化钠的纯度,称取ag样品并设计如图装置来测定过氧化钠的质量分数。
(1)将仪器连接好以后,必须进行的第一步操作是
(2)装置C中发生反应的化学方程式为
(3)D中NaOH溶液的作用为
(4)实验结束时,读取实验中生成气体的体积时,不合理的是
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.读取量筒中水的体积时,应使视线与凹液面的最低点相平
(5)读出量筒内水的体积后,折算成标准状况下氧气的体积为
 ,则样品中过氧化钠的质量分数为
,则样品中过氧化钠的质量分数为
您最近一年使用:0次
名校
3 . 某烧碱样品因部分变质含 ,某化学课外小组的同学测定该烧碱样品中NaOH的质量分数。
,某化学课外小组的同学测定该烧碱样品中NaOH的质量分数。
实验步骤:
Ⅰ.迅速地称取烧碱样品0.50g,溶解后配制成100mL溶液,备用。
Ⅱ.取20.00mL样品溶液于锥形瓶中,加入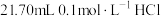 标准溶液,此时溶质为NaCl和
标准溶液,此时溶质为NaCl和 。
。
Ⅲ.继续加入 标准溶液,此时溶质为NaCl。
标准溶液,此时溶质为NaCl。
(1)步骤Ⅰ中所需的玻璃仪器有烧杯、玻璃棒、胶头滴管和___________ 。
(2)步骤Ⅱ、步骤Ⅲ中发生反应的离子方程式为___________ 、___________ 、___________ 。
(3)样品中NaOH的质量分数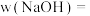
___________ %。(计算结果保留小数点后1位)
(4)下列操作会导致测得的NaOH质量分数偏高的是___________ (填字母序号)。
a.步骤Ⅰ,定容时俯视刻度线
b.步骤Ⅱ,加入HCl标准溶液时锥形瓶中有气泡产生
c.步骤Ⅲ,加入HCl标准溶液的过程中,锥形瓶中有少许液体溅出
 ,某化学课外小组的同学测定该烧碱样品中NaOH的质量分数。
,某化学课外小组的同学测定该烧碱样品中NaOH的质量分数。实验步骤:
Ⅰ.迅速地称取烧碱样品0.50g,溶解后配制成100mL溶液,备用。
Ⅱ.取20.00mL样品溶液于锥形瓶中,加入
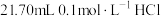 标准溶液,此时溶质为NaCl和
标准溶液,此时溶质为NaCl和 。
。Ⅲ.继续加入
 标准溶液,此时溶质为NaCl。
标准溶液,此时溶质为NaCl。(1)步骤Ⅰ中所需的玻璃仪器有烧杯、玻璃棒、胶头滴管和
(2)步骤Ⅱ、步骤Ⅲ中发生反应的离子方程式为
(3)样品中NaOH的质量分数
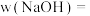
(4)下列操作会导致测得的NaOH质量分数偏高的是
a.步骤Ⅰ,定容时俯视刻度线
b.步骤Ⅱ,加入HCl标准溶液时锥形瓶中有气泡产生
c.步骤Ⅲ,加入HCl标准溶液的过程中,锥形瓶中有少许液体溅出
您最近一年使用:0次
4 . 通过下列实验进行物质性质或成分的探究。
实验1:向某溶液中加入澄清石灰水,观察到有白色沉淀产生
实验2:取久置的过氧化钠样品少许于试管中,加入2~3mL蒸馏水,有无色无味的气体生成
实验3:将盛满氯气的试管倒扣在水槽中,静置一段时间,观察到试管中液面明显上升
实验4:用洁净的铂丝蘸取某碱性溶液进行焰色试验,观察到火焰的颜色呈黄色
下列说法正确的是
实验1:向某溶液中加入澄清石灰水,观察到有白色沉淀产生
实验2:取久置的过氧化钠样品少许于试管中,加入2~3mL蒸馏水,有无色无味的气体生成
实验3:将盛满氯气的试管倒扣在水槽中,静置一段时间,观察到试管中液面明显上升
实验4:用洁净的铂丝蘸取某碱性溶液进行焰色试验,观察到火焰的颜色呈黄色
下列说法正确的是
A.实验1说明溶液中含有 或 或 |
| B.实验2可知过氧化钠没有变质 |
| C.实验3说明氯气能溶于水 |
D.实验4说明溶液中的溶质为 |
您最近一年使用:0次
名校
5 . 过氧化钠常做漂白剂、杀菌剂、消毒剂,其保存不当容易吸收空气中的CO2而变质。
(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入___________ 溶液,充分震荡后有白色沉淀,证明Na2O2已经变质。
(2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取a g样品,并设计用下图装置来测定过氧化钠的质量分数。
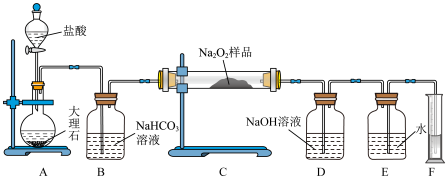
①将仪器连接好以后,必须进行的第一步操作是___________ 。
②B装置出来的气体是否需要干燥___________ 。(填“是”或“否”)
③写出装置C中发生的所有反应的化学方程式___________ ,___________ 。
④D中NaOH溶液的作用是___________ 。
⑤实验结束时,读取实验中生成气体的体积时,合理的是___________ (填字母序号)。
a.直接读取气体体积,不需要冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中的水的体积
⑥读取量筒内水的体积后,折算成标准状况下氧气的体积为V mL,则样品中过氧化钠的质量分数为___________ 。
(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入
(2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取a g样品,并设计用下图装置来测定过氧化钠的质量分数。

①将仪器连接好以后,必须进行的第一步操作是
②B装置出来的气体是否需要干燥
③写出装置C中发生的所有反应的化学方程式
④D中NaOH溶液的作用是
⑤实验结束时,读取实验中生成气体的体积时,合理的是
a.直接读取气体体积,不需要冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中的水的体积
⑥读取量筒内水的体积后,折算成标准状况下氧气的体积为V mL,则样品中过氧化钠的质量分数为
您最近一年使用:0次
6 . 对于某些离子或物质成分的检验及推断正确的是
| A.用洁净的铂丝蘸取溶液在酒精灯火焰上灼烧,火焰呈黄色,说明原溶液中有Na+,可能有K+ |
| B.加入碳酸钾溶液产生白色沉淀,再加盐酸白色沉淀消失,推断溶液中含有Ca2+ |
| C.将Na2O2样品中加入稀盐酸,有气体产生,可推断Na2O2已变质 |
D.加入盐酸后有气体逸出,此气体能使澄清石灰水变浑浊,可判定溶液中只含有CO |
您最近一年使用:0次
名校
解题方法
7 . 过氧化钠常用作漂白剂、杀菌剂、消毒剂,能与水和二氧化碳等物质发生反应,保存不当时容易变质。某实验小组以过氧化钠为研究对象进行了如下实验。
(1)探究一包Na2O2样品是否已经变质:取少量样品,加水将其溶解,加入___________ 溶液(填化学式),充分振荡后有白色沉淀,证明Na2O2已经变质。
(2)该实验小组为了粗略测定过氧化钠的质量分数,称取了mg样品,并设计用下图装置来测定过氧化钠的质量分数。
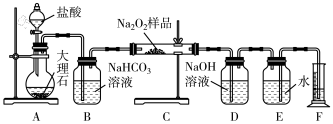
①装置中盛放盐酸的仪器的名称是___________ ,有同学提出该实验装置A、C装置之间没必要增加盛有饱和NaHCO3溶液的洗气瓶,该同学想法是否有道理?并说明理由:___________ 。
②将仪器连接好以后,必须进行的第一步操作是___________ 。
③写出装置C中发生的主要反应的化学方程式:___________ 。
④装置D的作用是___________ ;若无装置D,样品中Na2O2的质量分数___________ (填“偏高”“偏低”或“无影响”)。
⑤实验结束后,装置F中水的体积为VmL,已知氧气的密度为ρg·mL-1,样品中Na2O2质量分数为___________ (用含ρ、m、V的代数式表示)。
(3)压强不变时在一个密闭容器中放入足量过氧化钠固体,然后充入等分子数的CH4和O2,电火花引燃后充分反应,恢复至原温度,余下气体的分子数为原分子总数的___________ 。
(1)探究一包Na2O2样品是否已经变质:取少量样品,加水将其溶解,加入
(2)该实验小组为了粗略测定过氧化钠的质量分数,称取了mg样品,并设计用下图装置来测定过氧化钠的质量分数。

①装置中盛放盐酸的仪器的名称是
②将仪器连接好以后,必须进行的第一步操作是
③写出装置C中发生的主要反应的化学方程式:
④装置D的作用是
⑤实验结束后,装置F中水的体积为VmL,已知氧气的密度为ρg·mL-1,样品中Na2O2质量分数为
(3)压强不变时在一个密闭容器中放入足量过氧化钠固体,然后充入等分子数的CH4和O2,电火花引燃后充分反应,恢复至原温度,余下气体的分子数为原分子总数的
您最近一年使用:0次
2023-11-04更新
|
394次组卷
|
2卷引用:湖北省荆州市沙市中学2023-2024学年高一上学期11月期中考试化学试题
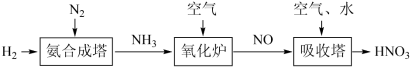
8 . I.空气中的氮氧化物主要来源:化石燃料燃烧、工业制硝酸尾气、汽车尾气。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:________ 。
(2)用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。在酸性NaClO溶液中,HClO氧化NO生成 和
和 ,其离子方程式为
,其离子方程式为_______ 。
II.铁器时代是人类发展史中一个极为重要的时代,铁及其化合物在人类的生产、生活中都起了巨大的作用。
(3)长期放置的FeSO4溶液易被氧化而变质,实验室用绿矾FeSO4·xH2O配制FeSO4溶液时为了防止FeSO4溶液变质,经常向其中加入铁粉,其原因是_______ (用离子方程式表示)。
(4)利用部分变质的FeSO4溶液制备Fe2O3:
部分变质的FeSO4溶液 溶液I
溶液I  沉淀II
沉淀II  Fe2O3
Fe2O3
①H2O2溶液的作用是______ 。
②写出由“溶液I”到“沉淀II”反应的离子方程式:______ 。
③“操作III”的名称为_______ 。
(5)为测定某绿矾FeSO4·xH2O中结晶水的含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g;将该绿矾FeSO4·xH2O样品装入石英玻璃管中,再次将装置A称重,记为m2g,按图示连接好装置进行实验。______ (填标号);重复上述操作步骤,直至装置A恒重,记为m3 g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2 d.打开K1和K2,缓缓通入N2 e.称量装置A f.冷却至室温
②根据实验记录,计算绿矾FeSO4·xH2O化学式中结晶水的数目x=_____ (列出计算式即可)。
(2)用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。在酸性NaClO溶液中,HClO氧化NO生成
 和
和 ,其离子方程式为
,其离子方程式为II.铁器时代是人类发展史中一个极为重要的时代,铁及其化合物在人类的生产、生活中都起了巨大的作用。
(3)长期放置的FeSO4溶液易被氧化而变质,实验室用绿矾FeSO4·xH2O配制FeSO4溶液时为了防止FeSO4溶液变质,经常向其中加入铁粉,其原因是
(4)利用部分变质的FeSO4溶液制备Fe2O3:
部分变质的FeSO4溶液
 溶液I
溶液I  沉淀II
沉淀II  Fe2O3
Fe2O3①H2O2溶液的作用是
②写出由“溶液I”到“沉淀II”反应的离子方程式:
③“操作III”的名称为
(5)为测定某绿矾FeSO4·xH2O中结晶水的含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g;将该绿矾FeSO4·xH2O样品装入石英玻璃管中,再次将装置A称重,记为m2g,按图示连接好装置进行实验。
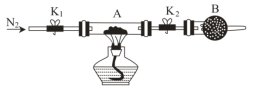
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2 d.打开K1和K2,缓缓通入N2 e.称量装置A f.冷却至室温
②根据实验记录,计算绿矾FeSO4·xH2O化学式中结晶水的数目x=
您最近一年使用:0次
名校
9 . 硫元素广泛存在于自然界中,是动植物生长不可缺少的元素。
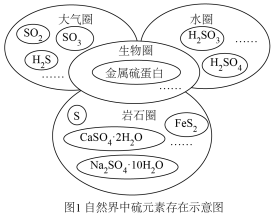
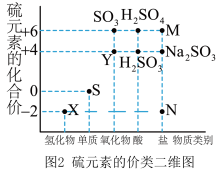
I.图1是自然界中硫元素的存在示意图,图2是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。___________ 。
(2)工业上常以黄铁矿为原料来制备硫酸,通入空气焙烧黄铁矿的化学方程式为___________ 。
(3) 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的基本操作是
溶液是否变质的基本操作是___________ 。
II.小组同学利用图3装置测定空气中 的含量。
的含量。___________ ,该装置中发生反应的离子方程式为___________ 。
(5)若空气流速为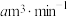 ,当观察到装置内
,当观察到装置内___________ 时,结束计时,测定耗时tmin,假定空气中的 可被溶液充分吸收,该空气样品中
可被溶液充分吸收,该空气样品中 的含量是
的含量是___________  。
。
I.图1是自然界中硫元素的存在示意图,图2是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。
(2)工业上常以黄铁矿为原料来制备硫酸,通入空气焙烧黄铁矿的化学方程式为
(3)
 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的基本操作是
溶液是否变质的基本操作是II.小组同学利用图3装置测定空气中
 的含量。
的含量。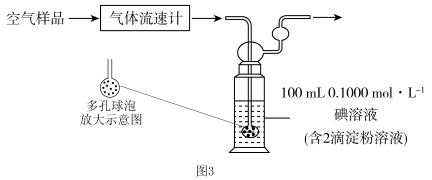
(5)若空气流速为
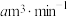 ,当观察到装置内
,当观察到装置内 可被溶液充分吸收,该空气样品中
可被溶液充分吸收,该空气样品中 的含量是
的含量是 。
。
您最近一年使用:0次
10 . 下列由相关实验现象所推出的结论不正确的是
A.取一定量 样品,溶解后加入 样品,溶解后加入 溶液,产生白色沉淀,加入稀硝酸,仍有沉淀,由此可知此样品已变质 溶液,产生白色沉淀,加入稀硝酸,仍有沉淀,由此可知此样品已变质 |
B.向某溶液滴加稀硝酸酸化的 溶液,产生白色沉淀,该溶液中含 溶液,产生白色沉淀,该溶液中含 |
C.向某溶液中加入浓氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,则待测溶液中一定含有 |
| D.将气体通过无水硫酸铜粉末,粉末变蓝,表明原气体中一定含有水蒸气 |
您最近一年使用:0次



