名校
解题方法
1 . 短周期元素X、Y、Z、W的原子序数依次增大。用表中信息判断下列说法不正确的是
| 元素 | X | Y | Z | W | |
| 最高价氧化物的水化物 | 分子式 | H3ZO4 | |||
| 25℃时,0.1mol·L-1溶液对应的pH | 1.00 | 13.00 | 1.57 | 0.70 | |
| A.YX3用于汽车防撞气囊,是离子晶体 |
B.简单氢化物分子内的键角: |
| C.足量的锌与W最高价氧化物的水化物的浓溶液充分反应,还原产物有2种 |
| D.31gZ4分子中含有1.5molσ键 |
您最近一年使用:0次
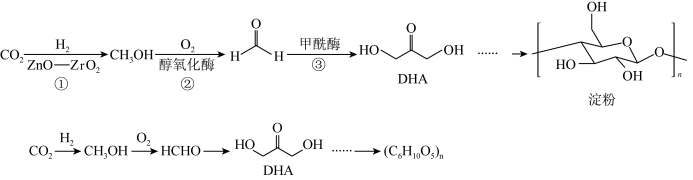
2 . 中国科学家在国际上首次实现从 到淀粉的实验室人工合成,其部分合成路线如图所示。设
到淀粉的实验室人工合成,其部分合成路线如图所示。设 表示阿伏加德罗常数的值,下列有关说法正确的是
表示阿伏加德罗常数的值,下列有关说法正确的是
 到淀粉的实验室人工合成,其部分合成路线如图所示。设
到淀粉的实验室人工合成,其部分合成路线如图所示。设 表示阿伏加德罗常数的值,下列有关说法正确的是
表示阿伏加德罗常数的值,下列有关说法正确的是
| A.反应①中转化属于化合反应 |
| B.升高温度一定会加快反应②的反应速率 |
C.3.0g 与DHA的混合物中含碳原子数为0.1 与DHA的混合物中含碳原子数为0.1 |
| D.DHA和淀粉中碳原子的成键方式完全相同 |
您最近一年使用:0次
解题方法
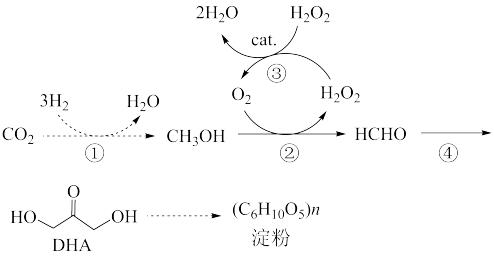
3 . 中科院天津工业生物技术研究所在淀粉的人工合成方面取得重大突破性进展,在国际上首次实现了二氧化碳到淀粉的从头合成,其中部分核心反应如图所示。设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
A.反应①消耗44g ,转移电子数为6 ,转移电子数为6 |
B.反应③中 为催化剂,实验室常用 为催化剂,实验室常用 催化该反应 催化该反应 |
C.30g 与DHA的混合物中含氧原子数目为2 与DHA的混合物中含氧原子数目为2 |
| D.淀粉与纤维素的分子式相同,但二者不互为同分异构体 |
您最近一年使用:0次
4 . 设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A.常温常压下,7.0g乙烯与丙烯的混合物中含有氢原子的数目为 |
B.11g由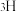 和 和 组成的超重水中,中子数和电子数之和为11 组成的超重水中,中子数和电子数之和为11 |
C.用1L1  溶液充分反应制备氢氧化铁胶体,该体系中含氢氧化铁胶体粒子的数目小于 溶液充分反应制备氢氧化铁胶体,该体系中含氢氧化铁胶体粒子的数目小于 |
D.向 溶液中通入适量 溶液中通入适量 ,当有1 ,当有1  被氧化时,共转移的电子数为3 被氧化时,共转移的电子数为3 |
您最近一年使用:0次
5 . 设 为阿伏加德罗常数的值。工业上制备高纯度硅的反应有:
为阿伏加德罗常数的值。工业上制备高纯度硅的反应有:
①
②
③
已知:H、Si的电负性依次为2.1、1.8.下列有关说法正确的是
 为阿伏加德罗常数的值。工业上制备高纯度硅的反应有:
为阿伏加德罗常数的值。工业上制备高纯度硅的反应有:①

②

③

已知:H、Si的电负性依次为2.1、1.8.下列有关说法正确的是
A.①中,30g氧化剂含极性键数目为 | B.②中,生成1g 时转移电子数为 时转移电子数为 |
| C.②和③互为可逆反应 | D.②和③的目的是除去粗硅中的杂质 |
您最近一年使用:0次
6 . 设 是阿伏加德罗常数的值。下列说法中正确的是
是阿伏加德罗常数的值。下列说法中正确的是
 是阿伏加德罗常数的值。下列说法中正确的是
是阿伏加德罗常数的值。下列说法中正确的是A.标准状况下,22.4LNO2所含质子数为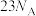 |
B.1mol 与足量 与足量 反应时,转移电子数为 反应时,转移电子数为 |
C.50mL 12mol/L的盐酸与足量 共热,生成水分子的数目为 共热,生成水分子的数目为 |
D.铅酸蓄电池的正极质量增加3.2g时,电路中通过的电子数目为 |
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
7 . NA是阿伏加德罗常数的值,下列说法不正确的是
| A.等物质的量的甲基(-CH3)和羟基(-OH)所含电子数相等 |
| B.22.4L(标准状况)氩气含有的质子数为36NA |
| C.1mol固体NaHSO4含有阴阳离子总数为2NA |
| D.2g由H218O和2H2O组成的物质中含有的质子数为NA |
您最近一年使用:0次
8 . NA为阿伏加德罗常数的值,下列说法不正确的是
| A.0.1 mol·L-1的NH4HCO3溶液与NaOH溶液等体积混合并加热,产生的氨气标况下2.24L |
| B.标况下,1molN2 和O2的混合气体总体积约为22.4L |
| C.常温常压下,2.8gCO和C2H4的混合气体中含有的分子数目为0.1 NA |
| D.39.0gNa2O2 与足量水完全反应,转移的电子数为0.5 NA |
您最近一年使用:0次
9 .  是阿伏加德罗常数的值,下列说法中合理的是
是阿伏加德罗常数的值,下列说法中合理的是
 是阿伏加德罗常数的值,下列说法中合理的是
是阿伏加德罗常数的值,下列说法中合理的是A.0.1 mol  与0.1 mol 与0.1 mol  于密闭容器中充分反应后HI分子总数为 于密闭容器中充分反应后HI分子总数为 |
B.18 g重水中含有质子数为 |
C.3 g  含有中子数为 含有中子数为 |
D.25℃,101 kPa下,28 L氢气的中电子数目为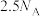 |
您最近一年使用:0次
解题方法
10 . 氟与碱的反应不同于其他卤素与碱的反应,例如F2与NaOH稀溶液可发生反应:2F2(g)+2NaOH(aq)=2NaF(aq)+OF2(g)+H2O(l)。设NA为阿伏加德罗常数的值。下列说法错误的是
| A.NaF溶液显酸性 |
| B.H2O分子中O的价层电子对数为4 |
| C.含0.1molNaOH的溶液中,Na+的数目为0.1NA |
| D.OF2分子中每个原子均达到8电子稳定结构 |
您最近一年使用:0次
2023-03-16更新
|
640次组卷
|
4卷引用:专题03 阿伏伽德罗常数的应用



