名校
1 .  为阿伏加德罗常数的值,下列说法
为阿伏加德罗常数的值,下列说法不正确 的是
 为阿伏加德罗常数的值,下列说法
为阿伏加德罗常数的值,下列说法A.铁与水蒸气反应后,固体质量增加了3.2g,则电子转移的数目为 |
B.1L0.1mol/L 溶液中, 溶液中, 的数目为 的数目为 |
C.10g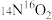 和 和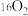 混合气体中含有的质子数为 混合气体中含有的质子数为 |
D.3.2g 中含有的共价键的数目为 中含有的共价键的数目为 |
您最近一年使用:0次
2023-05-04更新
|
452次组卷
|
4卷引用:专题03 阿伏加德罗常数与化学计算 -2023年高考化学真题题源解密(新高考专用)
(已下线)专题03 阿伏加德罗常数与化学计算 -2023年高考化学真题题源解密(新高考专用)浙江省浙南名校联盟2023届高三第二次联考(一模)化学试题(已下线)第03练 阿伏加德罗常数(NA)及其应用-2023年【暑假分层作业】高二化学(2024届一轮复习通用)山西省晋城市第一中学校2023-2024学年高二上学期第五次调研考试化学试题
2024高三下·浙江·专题练习
2 . KNO3具有强氧化性,可发生反应:2KNO3+2NH4Cl 2KCl+2N2↑+O2↑+4H2O。下列说法
2KCl+2N2↑+O2↑+4H2O。下列说法不正确 的是(NA为阿伏加德罗常数的值)
 2KCl+2N2↑+O2↑+4H2O。下列说法
2KCl+2N2↑+O2↑+4H2O。下列说法| A.N2既是氧化产物,又是还原产物 |
| B.KNO3仅作氧化剂 |
| C.生成1molN2转移电子的数目为5NA |
| D.实验室不可用加热NH4NO3固体的方法制备NH3 |
您最近一年使用:0次
3 . 设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A.50g质量分数为64%的甲醇水溶液中含有σ键数目为5 |
B.一定条件下,5.6g Fe与0.1mol  充分反应,转移的电子数为0.2 充分反应,转移的电子数为0.2 |
C.浓硝酸热分解生成 、 、 共69g时,转移电子数为1.5 共69g时,转移电子数为1.5 |
D.常温下,1L pH=2的稀盐酸中含有的H+数目为0.01 |
您最近一年使用:0次
名校
4 . NA为阿伏加德罗常数的值。下列说法中,正确的是
| A.标准状况下,22.4 L己烷的氢原子数约为14 NA |
| B.密闭容器中23 g NO2与N2O4的混合气体中氮原子数为0.5 NA |
| C.过氧化钠与水反应时,生成0.1 mol O2转移的电子数为0.4 NA |
D.1 L 0.1 mol·L−1的NaHCO3溶液中HCO 和CO 和CO 离子数之和为0.1 NA 离子数之和为0.1 NA |
您最近一年使用:0次
名校
解题方法
5 . 六方硫化锌的结构是S原子作六方最密堆积,其晶胞如图所示,图中A点分数坐标为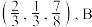 点分数坐标为
点分数坐标为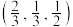 ;底
;底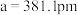 ,高
,高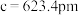 。设
。设 为阿伏加德罗常数的值。下列说法
为阿伏加德罗常数的值。下列说法错误 的是
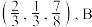 点分数坐标为
点分数坐标为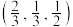 ;底
;底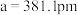 ,高
,高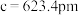 。设
。设 为阿伏加德罗常数的值。下列说法
为阿伏加德罗常数的值。下列说法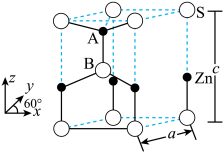
A.晶胞中, 填充空隙类型为正四面体空隙 填充空隙类型为正四面体空隙 | B.图中S原子的配位数为6 |
C.图中 的核间距约为 的核间距约为 | D.该晶体的化学式为 |
您最近一年使用:0次
2024-05-06更新
|
735次组卷
|
5卷引用:题型5 物质结构与性质 有机物的结构与性质(25题)-2024年高考化学常考点必杀300题(新高考通用)
(已下线)题型5 物质结构与性质 有机物的结构与性质(25题)-2024年高考化学常考点必杀300题(新高考通用)贵州省贵阳市第六中学2024届高三下学期一模考试化学试题浙江省舟山中学2023-2024学年高二下学期4月月考化学试题河南省焦作市博爱县第一中2023-2024学年高二下学期4月期中考试化学试题湖南省衡阳县第四中学2023-2024学年高三下学期4月月考化学试题
解题方法
6 . “84”消毒液和双氧水混合时发生反应: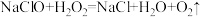 。已知NA为阿伏加德罗常数的值,若生成标准状况下33.6LO2,下列说法不正确的是
。已知NA为阿伏加德罗常数的值,若生成标准状况下33.6LO2,下列说法不正确的是
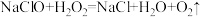 。已知NA为阿伏加德罗常数的值,若生成标准状况下33.6LO2,下列说法不正确的是
。已知NA为阿伏加德罗常数的值,若生成标准状况下33.6LO2,下列说法不正确的是| A.消耗的H2O2含有共用电子对数为3NA |
| B.生成NaCl的质量为87.75g |
| C.转移的电子数为3NA |
| D.1L1mol·L-1NaClO溶液中含有ClO-数小于NA |
您最近一年使用:0次
名校
解题方法
7 .  具有强氧化性,可发生反应:
具有强氧化性,可发生反应: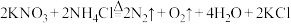 。下列说法
。下列说法不正确 的是( 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
 具有强氧化性,可发生反应:
具有强氧化性,可发生反应: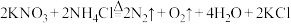 。下列说法
。下列说法 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)A. 既是氧化产物,又是还原产物 既是氧化产物,又是还原产物 | B. 仅作氧化剂 仅作氧化剂 |
C.生成1mol 转移电子的数目为 转移电子的数目为 | D.实验室不可用加热 固体的方法制备 固体的方法制备 |
您最近一年使用:0次
解题方法
8 . 氟与碱的反应不同于其他卤素与碱的反应,例如F2与NaOH稀溶液可发生反应:2F2(g)+2NaOH(aq)=2NaF(aq)+OF2(g)+H2O(l)。设NA为阿伏加德罗常数的值。下列说法错误的是
| A.NaF溶液显酸性 |
| B.H2O分子中O的价层电子对数为4 |
| C.含0.1molNaOH的溶液中,Na+的数目为0.1NA |
| D.OF2分子中每个原子均达到8电子稳定结构 |
您最近一年使用:0次
2023-03-16更新
|
640次组卷
|
4卷引用:专题03 阿伏伽德罗常数的应用
名校
解题方法
9 . 微观探析是认识物质的一种途径。设 为阿伏加德罗常数,下列有关说法正确的是
为阿伏加德罗常数,下列有关说法正确的是
 为阿伏加德罗常数,下列有关说法正确的是
为阿伏加德罗常数,下列有关说法正确的是A.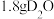 中含有的中子数目为 中含有的中子数目为 |
B.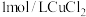 溶液中含有 溶液中含有 的数目小于 的数目小于 |
C. 与 与 的混合物中含有的分子数为 的混合物中含有的分子数为 |
D.25℃,101kPa, 与NaOH溶液完全反应,转移电子数目为 与NaOH溶液完全反应,转移电子数目为 |
您最近一年使用:0次
2024-03-06更新
|
902次组卷
|
4卷引用:选择题11-16
2023高三·全国·专题练习
10 . 已知Na2SO3具有强还原性,能够被Cl2氧化。某化工厂排出的废水中含0.014mol·L-1 Cl2、0.001mol·L-1 H+,废水排出的速度为10.0mL·s-1,为了除去此废水中的游离氯分子,并使废水变为中性,有人提出如下建议:在废水排出管A和B处分别注入一定流量的Na2SO3溶液(0.10mol·L-1)和烧碱溶液(0.10mol·L-1)。下列说法错误的是
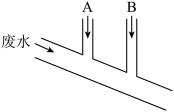

A.排出管A处发生的反应为 +Cl2+H2O= +Cl2+H2O= +2Cl-+2H+ +2Cl-+2H+ |
| B.废水排出管B处发生的反应为Cl2+2OH-=Cl-+ClO-+H2O |
| C.A处溶液的流量为1.4mL·s-1 |
| D.B处溶液的流量为2.8mL·s-1 |
您最近一年使用:0次



