1 . 下列由实验操作及现象所得的结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向0.5mL溴乙烷中加入约2mL2%AgNO3溶液,振荡 | 溶液分层,上层出现浑浊 | 溴乙烷是电解质,能电离出Br- |
| B | 向苯酚钠溶液中通入足量CO2气体 | 溶液变浑浊 | 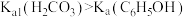 |
| C | 光洁的铜丝灼烧后,趁热插入2mL乙醇中 | 铜丝由黑色变为红色 | 乙醇具有氧化性 |
| D | 向CH3COOH溶液中加入CH3CCONH4固体,测量溶液pH变化 | pH变大 | CH3COONH4溶液呈碱性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 硼氢化钠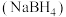 在化工等领域具有重要的应用价值,工业上可用硼镁矿(生要成分为
在化工等领域具有重要的应用价值,工业上可用硼镁矿(生要成分为 ,含少量杂质
,含少量杂质 )制取
)制取 ,其工艺流程如下:
,其工艺流程如下:

已知:硼氢化钠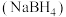 常温下能与水反应,易溶于异丙胺(沸点为
常温下能与水反应,易溶于异丙胺(沸点为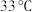 )。
)。
(1) 和
和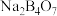 都是硼酸盐,请写出一元弱酸硼酸
都是硼酸盐,请写出一元弱酸硼酸 在水中的电离方程式
在水中的电离方程式_______ 。
(2)粉碎的目的是_______ ;滤渣的成分是_______ (写化学式、下同)。
(3)操作1的步骤是____ 、冷却结晶;操作2、操作3的名称分别为_____ 、_______ 。
(4)高温合成过程中,加料之前需先在反应器中通入氩气,该操作的目的是_______ 。
(5)流程中可循环利用的物质是_______ 。写出副产物硅酸钠的一种用途_______ 。
(6) 被称为万能还原剂,“有效氢含量”可用来衡量含氢还原剂的还原能力,其定义是:每克含氢还原剂的还原能力相当于多少克
被称为万能还原剂,“有效氢含量”可用来衡量含氢还原剂的还原能力,其定义是:每克含氢还原剂的还原能力相当于多少克 的还原能力。
的还原能力。 的有效氢含量为
的有效氢含量为_____ (保留两位小数)。
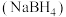 在化工等领域具有重要的应用价值,工业上可用硼镁矿(生要成分为
在化工等领域具有重要的应用价值,工业上可用硼镁矿(生要成分为 ,含少量杂质
,含少量杂质 )制取
)制取 ,其工艺流程如下:
,其工艺流程如下:
已知:硼氢化钠
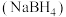 常温下能与水反应,易溶于异丙胺(沸点为
常温下能与水反应,易溶于异丙胺(沸点为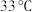 )。
)。(1)
 和
和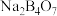 都是硼酸盐,请写出一元弱酸硼酸
都是硼酸盐,请写出一元弱酸硼酸 在水中的电离方程式
在水中的电离方程式(2)粉碎的目的是
(3)操作1的步骤是
(4)高温合成过程中,加料之前需先在反应器中通入氩气,该操作的目的是
(5)流程中可循环利用的物质是
(6)
 被称为万能还原剂,“有效氢含量”可用来衡量含氢还原剂的还原能力,其定义是:每克含氢还原剂的还原能力相当于多少克
被称为万能还原剂,“有效氢含量”可用来衡量含氢还原剂的还原能力,其定义是:每克含氢还原剂的还原能力相当于多少克 的还原能力。
的还原能力。 的有效氢含量为
的有效氢含量为
您最近一年使用:0次
3 . 高纯度的氢氟酸是制造芯片的重要原料之一。
(1)已知:HF(aq)⇌H+(aq)+F-(aq) ΔH=-10.4kJ/mol
H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol
则:HF(aq)+NaOH(aq)=NaF(aq)+H2O(l)的ΔH=_______ 。
(2)HF无论是气态还是在水溶液中均可二聚形成(HF)2。HF能二聚的原因是_______ ,写出(HF)2发生第二步电离的电离方程式_______ 。
(3)如图为恒温、带有可自由移动隔板的刚性容器。当两边分别充入4g氦气和20g单分子态的HF气体时,隔板位于“5”处,隔板两边容器内的压强均为100kPa。

若固定隔板于“5”处,当右侧容器内反应2HF(g)⇌(HF)2(g)达到平衡状态时,右侧容器内压强为P1;松开隔板,隔板移至“6”处并达到新的平衡,此时右侧容器内压强为P2,则P1_______ P2(填“大于”“小于”或“等于”)。该温度下,2HF(g)⇌(HF)2(g)反应的平衡常数KP=_______ kPa-1(KP为以分压表示的平衡常数,计算结果保留2位有效数字)。
(4)若将上述容器改为绝热容器,固定隔板在“5”处,下列不能说明右侧容器内反应已达平衡状态的是_______ 。
A.容器右侧气体的密度不再改变
B.容器右侧的温度不再改变
C.容器右侧气体的压强不再改变
D.容器右侧气体的平均相对分子质量不再改变
E.
(5)某温度下,将分析浓度(总浓度)相同的HCl、HF和CH3COOH三种溶液,分别加水稀释时,溶液pH变化如图所示。

图中,氢氟酸溶液在稀释初期的pH上升特别快,据此判断,(HF)2与HF的酸性相比,较强的是_______ 。
(6)NaF和HF的混合溶液具有一定的缓冲能力,即加入少量的酸或碱时,溶液的pH基本保持不变。试结合方程式和必要的文字解释之______ 。
(1)已知:HF(aq)⇌H+(aq)+F-(aq) ΔH=-10.4kJ/mol
H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol
则:HF(aq)+NaOH(aq)=NaF(aq)+H2O(l)的ΔH=
(2)HF无论是气态还是在水溶液中均可二聚形成(HF)2。HF能二聚的原因是
(3)如图为恒温、带有可自由移动隔板的刚性容器。当两边分别充入4g氦气和20g单分子态的HF气体时,隔板位于“5”处,隔板两边容器内的压强均为100kPa。

若固定隔板于“5”处,当右侧容器内反应2HF(g)⇌(HF)2(g)达到平衡状态时,右侧容器内压强为P1;松开隔板,隔板移至“6”处并达到新的平衡,此时右侧容器内压强为P2,则P1
(4)若将上述容器改为绝热容器,固定隔板在“5”处,下列不能说明右侧容器内反应已达平衡状态的是
A.容器右侧气体的密度不再改变
B.容器右侧的温度不再改变
C.容器右侧气体的压强不再改变
D.容器右侧气体的平均相对分子质量不再改变
E.

(5)某温度下,将分析浓度(总浓度)相同的HCl、HF和CH3COOH三种溶液,分别加水稀释时,溶液pH变化如图所示。

图中,氢氟酸溶液在稀释初期的pH上升特别快,据此判断,(HF)2与HF的酸性相比,较强的是
(6)NaF和HF的混合溶液具有一定的缓冲能力,即加入少量的酸或碱时,溶液的pH基本保持不变。试结合方程式和必要的文字解释之
您最近一年使用:0次
2021-03-12更新
|
485次组卷
|
3卷引用:安徽省马鞍山市2021届高三第一次模拟理综化学试题
安徽省马鞍山市2021届高三第一次模拟理综化学试题(已下线)重点9 化学反应原理的综合应用-2021年高考化学【热点·重点·难点】专练(山东专用)河北省石家庄市第二中学2021-2022学年高三上学期10月第二次考试化学试题
4 . 常温下,向10 mL 0.1 mol·L–1的HA溶液中逐滴加入0.1 mol·L–1的氨水,溶液的pH及导电能力变化趋势如图。下列说法正确的是( )
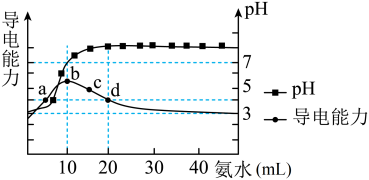

| A.b点溶液中,水的电离程度最小 |
| B.溶液中的阴离子浓度总和关系是:b>c>a |
| C.常温下,HA的电离平衡常数的数量级为10–6 |
| D.d点溶液中:c(A–)+c(HA)=2c(NH3·H2O) |
您最近一年使用:0次
解题方法
5 . 某分子的结构如图所示(-R 为烃基),其中 A、B、D 三种元素位于元素周期表中同一族的三个相邻的周期,A 的非金属性大于 B。D 与 G 形成的 DG3在工业上可用于漂白和杀菌消毒。A 与 G 形成的 AG3可完全水解,其水解的产物之一 H3AO3常用作塑料件镀金属的还原剂。

(1)具有未成对电子的原子或分子具有磁性。D 的某种氧化物 D2O4的磁性大小与温度呈正相关关系,即磁性是温度的增函数。则 D2O4 2DO2,ΔH
2DO2,ΔH______ 0(填“>”“<”或“=”)。
(2)DG3用于杀菌消毒与 HGO 相比,DG3可大大延长杀菌消毒的时间,试从反应速率理论和平衡移动理论两者中选择一个,解释其原因____________________________ 。
(3)无机含氧酸中的非羟基氢不能发生电离。H3AO3分子中 A 原子最外层的电子都参与了共价键的形成,试用方程式表示 H3AO3的正盐溶液呈碱性的原因_____ 。
(4)液氨中因存在2NH3(1) NH4++NH2-可导电,液态 D2O4中也存在 D2O4
NH4++NH2-可导电,液态 D2O4中也存在 D2O4 DO++DO3-,上述两个过程的本质区别为
DO++DO3-,上述两个过程的本质区别为___________ 。
(5)T℃时,在一体积为 VL 的密闭容器中放入一定量的 ACl5固体,按下式发生反应:ACl5(s) ACl3(g)+Cl2(g),ΔH>0。测得容器内气体的压强变化如下表:
ACl3(g)+Cl2(g),ΔH>0。测得容器内气体的压强变化如下表:
上述条件下,以分压表示的平衡常数 Kp=_____ (kPa)2(计算结果保留两位小数); 若保持温度不变,30s 时给容器加压,达新平衡后,容器内的总压将_____ (填“升高”、“降低”或“不变”);若将容器换成绝热容器,加压后容器内的总压将_____ (填“升高”、“降低”或“不变”)。

(1)具有未成对电子的原子或分子具有磁性。D 的某种氧化物 D2O4的磁性大小与温度呈正相关关系,即磁性是温度的增函数。则 D2O4
 2DO2,ΔH
2DO2,ΔH(2)DG3用于杀菌消毒与 HGO 相比,DG3可大大延长杀菌消毒的时间,试从反应速率理论和平衡移动理论两者中选择一个,解释其原因
(3)无机含氧酸中的非羟基氢不能发生电离。H3AO3分子中 A 原子最外层的电子都参与了共价键的形成,试用方程式表示 H3AO3的正盐溶液呈碱性的原因
(4)液氨中因存在2NH3(1)
 NH4++NH2-可导电,液态 D2O4中也存在 D2O4
NH4++NH2-可导电,液态 D2O4中也存在 D2O4 DO++DO3-,上述两个过程的本质区别为
DO++DO3-,上述两个过程的本质区别为(5)T℃时,在一体积为 VL 的密闭容器中放入一定量的 ACl5固体,按下式发生反应:ACl5(s)
 ACl3(g)+Cl2(g),ΔH>0。测得容器内气体的压强变化如下表:
ACl3(g)+Cl2(g),ΔH>0。测得容器内气体的压强变化如下表:| 时间 t/s | 0 | 5 | 10 | 15 | 20 | 25 | 30 | ∞ |
| 总压 P/kPa | 0 | 1.0 | 2.0 | 3.0 | 4.0 | 5.0 | 5.0 | 5.0 |
您最近一年使用:0次
名校
6 . 下列物质属于弱电解质的是
| A.酒精 | B.水 | C.盐酸 | D.食盐 |
您最近一年使用:0次
2019-08-22更新
|
159次组卷
|
2卷引用:安徽省安庆市第七中学2021-2022学年高三下学期第一次模拟考试化学试题
名校
7 . 下列说法正确的是
| A.液态HCl、固态AgCl均不导电,所以HCl、AgCl是非电解质 |
| B.NH3、CO2的水溶液均能导电,所以NH3、CO2均是电解质 |
| C.碱性氧化物一定是金属氧化物,金属氧化物一定是碱性氧化物 |
| D.非金属氧化物不一定是酸性氧化物,酸性氧化物不一定都是非金属氧化物 |
您最近一年使用:0次
2019-08-02更新
|
492次组卷
|
11卷引用:【校级联考】安徽省皖中名校联盟2019届高三上学期10月联考化学试题
【校级联考】安徽省皖中名校联盟2019届高三上学期10月联考化学试题安徽省阜阳市第三中学2018-2019学年高一上学期小期末考试(期末模拟)化学试题安徽省亳州市第二中学2018-2019学年高二下学期期末考试化学试题广东省揭阳市惠来县第一中学2018-2019学年高一上学期期中考试化学试题【全国百强校】内蒙古自治区乌兰察布市集宁区第一中学2018-2019学年高一上学期期末考试化学试题(已下线)专题2.1 物质的组成、性质及分类(练)-《2020年高考一轮复习讲练测》四川省邻水实验学校2020届高三上学期第一次月考化学试题四川省乐山市外国语学校2020届高三9月月考化学试题湖南省长沙市周南中学2019—2020学年上学期高一第一次月考化学试题(已下线)【新东方】2020-59海南省三亚市第一中学2023-2024学年高一上学期期中考试化学(B)试题
8 . 按纯净物、混合物、电解质和非电解质顺序排列的一组物质是
| A.胆矾、漂白粉、氯化钾、硫酸钡 |
| B.盐酸、空气、硝酸、干冰 |
| C.冰醋酸、海水、氧化铝、乙醇 |
| D.蛋白质、油脂、烧碱、石灰石 |
您最近一年使用:0次
9 . 下列涉及化学概念和基本原理说法正确的是
| A.12C14C C60互为同分异构体 |
| B.由同种元素组成的物质一定是纯净物 |
| C.金属氧化物存在酸性氧化物 |
| D.N2O3的水溶液能导电,说明N2O3是电解质 |
您最近一年使用:0次
2016-12-09更新
|
170次组卷
|
2卷引用:2015届安徽省淮北市高三第一次模拟考试化学试卷
10 . “类推”的思维方式在化学学习与研究中经常采用。下列类推思维中正确的是( )
| A.NaOH饱和溶液导电能力强,则Ca(OH)2饱和溶液导电能力也强 |
| B.CaC2能水解:CaC2+2H2O→Ca(OH)2+HC≡CH,则Mg2C3也能水解Mg2C3+4H2O→2Mg(OH)2+CH3-C≡CH |
| C.加热时Cu与O2反应生成CuO,则加热时Cu与S反应生成CuS |
| D.BaCl2溶液中通入SO2无沉淀产生,则Ba(NO3)2溶液中通入SO2也无沉淀产生 |
您最近一年使用:0次
2016-12-09更新
|
640次组卷
|
4卷引用:2013届安徽省合肥市高三第一次教学质量检测化学试卷
(已下线)2013届安徽省合肥市高三第一次教学质量检测化学试卷安徽省宿州市萧县鹏程中学2021-2022学年高二下学期第一次质量检测化学试题山东省济南外国语学校2018届高三上学期阶段考试化学试题江西省新余市第一中学2021-2022学年高三上学期第二次模拟考试化学试题



