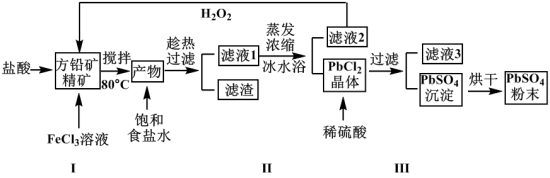
1 . 硫酸铅(PbSO4)广泛应用于制造铅蓄电池、白色颜料等。利用方铅矿精矿(PbS)直接制备硫酸铅粉末的流程如下:
已知:(ⅰ)PbCl2(s)+2Cl-(aq)

 (aq) △H>0
(aq) △H>0
(ⅱ)Ksp(PbSO4)=1.08×10-8,Ksp(PbCl2)=1.6×10-5
(ⅲ)Fe3+、Pb2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、7.04
(1)步骤Ⅰ中FeCl3溶液与PbS反应生成PbCl2和S的离子方程式为_____________________ ,步骤Ⅰ中另一个反应是H2O2与FeCl2、盐酸反应生成FeCl3,实现FeCl3的重复利用,其离子方程式为__________ ,加入盐酸的另一个目的是为了控制pH在0.5~1.0,原因是_____________________________ 。
(2)用化学平衡移动的原理解释步骤Ⅱ中使用冰水浴的原因___________________________ 。
(3)写出PbCl2晶体转化为PbSO4沉淀的离子方程式__________________________________ 。
(4)滤液3是_______________ 。
(5)铅蓄电池的电解液是稀硫酸(22%~28%),充电后两个电极上沉积的PbSO4分别转化为PbO2和Pb,铅蓄电池充电时阴极的电极反应式为________________________________ 。

已知:(ⅰ)PbCl2(s)+2Cl-(aq)


 (aq) △H>0
(aq) △H>0(ⅱ)Ksp(PbSO4)=1.08×10-8,Ksp(PbCl2)=1.6×10-5
(ⅲ)Fe3+、Pb2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、7.04
(1)步骤Ⅰ中FeCl3溶液与PbS反应生成PbCl2和S的离子方程式为
(2)用化学平衡移动的原理解释步骤Ⅱ中使用冰水浴的原因
(3)写出PbCl2晶体转化为PbSO4沉淀的离子方程式
(4)滤液3是
(5)铅蓄电池的电解液是稀硫酸(22%~28%),充电后两个电极上沉积的PbSO4分别转化为PbO2和Pb,铅蓄电池充电时阴极的电极反应式为
您最近一年使用:0次
14-15高三上·广东汕头·期中
解题方法
2 . 明矾[KAl(SO4)2·12H2O] 在生产、生活中有广泛用途:饮用水的净化;造纸工业上作施胶剂;食品工业的发酵剂等。利用炼铝厂的废料——铝灰(含Al 、 Al2O3及少量SiO2和FeO ·xFe2O3)可制备明矾。工艺流程如下:

回答下列问题:
(1)明矾净水的原理是(用离子方程表示)_________________________________ 。
(2)操作Ⅰ是_____________ ,操作Ⅱ是蒸发浓缩、_______________ 、过滤、_____ 、干燥。
(3)检验滤液A中是否存在Fe2+的试剂是(只用一种试剂)_________________ 。
(4)在滤液A中加入高锰酸钾发生反应的离子方程式为(该条件下Fe2+转化为Fe3+,MnO4-转化为Mn2+)_________________________________________________ 。
已知:生成氢氧化物沉淀的pH如下表所示
注:金属离子的起始浓度为0.1 mol·L-1
根据表中数据解释调pH=3的目的_______________________________________ 。
(5)已知:在pH=3、加热条件下,MnO4-可与Mn2+反应生成MnO2。加入MnSO4发生反应的离子方程式为:_______________ 。滤渣2含有的物质是___________ 。

回答下列问题:
(1)明矾净水的原理是(用离子方程表示)
(2)操作Ⅰ是
(3)检验滤液A中是否存在Fe2+的试剂是(只用一种试剂)
(4)在滤液A中加入高锰酸钾发生反应的离子方程式为(该条件下Fe2+转化为Fe3+,MnO4-转化为Mn2+)
已知:生成氢氧化物沉淀的pH如下表所示
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
注:金属离子的起始浓度为0.1 mol·L-1
根据表中数据解释调pH=3的目的
(5)已知:在pH=3、加热条件下,MnO4-可与Mn2+反应生成MnO2。加入MnSO4发生反应的离子方程式为:
您最近一年使用:0次



