解题方法
1 . 二氧化硫脲[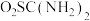 ](
](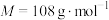 )为氮化合物的重要中间体,微溶于冷水,有还原性(碱性条件下增强)、热稳定性好。某同学利用废石膏制取二氧化硫脲,实验过程如下:
)为氮化合物的重要中间体,微溶于冷水,有还原性(碱性条件下增强)、热稳定性好。某同学利用废石膏制取二氧化硫脲,实验过程如下:
①滤液b主要成份为硫脲[ ](
](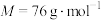 ),该物质易溶于水、有还原性。
),该物质易溶于水、有还原性。
②当pH<2时,硫脲与双氧水发生反应只生成甲脒化二硫。
③二氧化硫脲粗产品中存在尿素[ ]。
]。
请回答:
(1)仪器Y的名称是________________ 。
(2)下列说法正确的是 。
(3)装置A的气密性检查操作为___________ 。
(4)请写出溶液b生成二氧化硫脲的化学方程式_____________ 。
(5)步骤5中将溶液温度下降到5℃的目的是______________ 。
(6)为了检验产品中二氧化硫脲的含量(主要杂质为硫脲,其他杂质不参与反应),该同学设计了如下实验:
①称取5.000g产品,配制成100mL溶液。取10.00mL待测液于碘量瓶中,加入20.00mL 1.500 NaOH溶液,再加入25.00mL 0.5000
NaOH溶液,再加入25.00mL 0.5000 I2标准溶液,静置一段时间,加入适量硫酸进行酸化,改用0.5000
I2标准溶液,静置一段时间,加入适量硫酸进行酸化,改用0.5000
 溶液进行滴定,测得消耗
溶液进行滴定,测得消耗 溶液体积为10.00mL。
溶液体积为10.00mL。
涉及到的反应有:
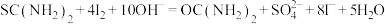
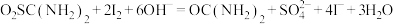

②另取0.1000g产品,加入50.00mL 0.1000 NaOH溶液,再加入30.00mL 3.000%
NaOH溶液,再加入30.00mL 3.000%  溶液,静置2分钟。改用0.1000
溶液,静置2分钟。改用0.1000
 溶液进行滴定,测得消耗
溶液进行滴定,测得消耗 溶液为16.00mL。
溶液为16.00mL。
涉及到的反应有:
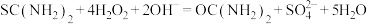


该产品中二氧化硫脲的质量分数为____________ 。
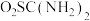 ](
](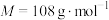 )为氮化合物的重要中间体,微溶于冷水,有还原性(碱性条件下增强)、热稳定性好。某同学利用废石膏制取二氧化硫脲,实验过程如下:
)为氮化合物的重要中间体,微溶于冷水,有还原性(碱性条件下增强)、热稳定性好。某同学利用废石膏制取二氧化硫脲,实验过程如下: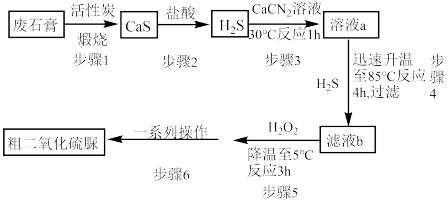

①滤液b主要成份为硫脲[
 ](
](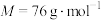 ),该物质易溶于水、有还原性。
),该物质易溶于水、有还原性。②当pH<2时,硫脲与双氧水发生反应只生成甲脒化二硫。
③二氧化硫脲粗产品中存在尿素[
 ]。
]。请回答:
(1)仪器Y的名称是
(2)下列说法正确的是 。
A.装置B中装的X溶液为饱和 溶液 溶液 |
B.装置E中的 与 与 发生氧化还原反应,起到尾气处理的作用 发生氧化还原反应,起到尾气处理的作用 |
| C.装置F中可分多次加入碳酸氢铵,以提高二氧化硫脲的产率 |
| D.步骤6“一系列操作”可为减压过滤,用冷水洗涤沉淀2-3次,一定温度下烘干沉淀 |
(3)装置A的气密性检查操作为
(4)请写出溶液b生成二氧化硫脲的化学方程式
(5)步骤5中将溶液温度下降到5℃的目的是
(6)为了检验产品中二氧化硫脲的含量(主要杂质为硫脲,其他杂质不参与反应),该同学设计了如下实验:
①称取5.000g产品,配制成100mL溶液。取10.00mL待测液于碘量瓶中,加入20.00mL 1.500
 NaOH溶液,再加入25.00mL 0.5000
NaOH溶液,再加入25.00mL 0.5000 I2标准溶液,静置一段时间,加入适量硫酸进行酸化,改用0.5000
I2标准溶液,静置一段时间,加入适量硫酸进行酸化,改用0.5000
 溶液进行滴定,测得消耗
溶液进行滴定,测得消耗 溶液体积为10.00mL。
溶液体积为10.00mL。涉及到的反应有:
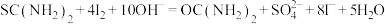
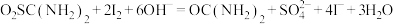

②另取0.1000g产品,加入50.00mL 0.1000
 NaOH溶液,再加入30.00mL 3.000%
NaOH溶液,再加入30.00mL 3.000%  溶液,静置2分钟。改用0.1000
溶液,静置2分钟。改用0.1000
 溶液进行滴定,测得消耗
溶液进行滴定,测得消耗 溶液为16.00mL。
溶液为16.00mL。涉及到的反应有:
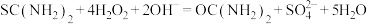


该产品中二氧化硫脲的质量分数为
您最近一年使用:0次
解题方法
2 . 在一定量铁的氧化物 (铁只有
(铁只有 、
、 价)中,加入
价)中,加入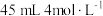 硫酸溶液,恰好使固体完全溶解,所得溶液中
硫酸溶液,恰好使固体完全溶解,所得溶液中 恰好被标准状况下
恰好被标准状况下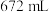 氯气氧化,则该固体中x和y的个数之比为
氯气氧化,则该固体中x和y的个数之比为
 (铁只有
(铁只有 、
、 价)中,加入
价)中,加入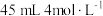 硫酸溶液,恰好使固体完全溶解,所得溶液中
硫酸溶液,恰好使固体完全溶解,所得溶液中 恰好被标准状况下
恰好被标准状况下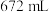 氯气氧化,则该固体中x和y的个数之比为
氯气氧化,则该固体中x和y的个数之比为A.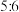 | B.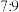 | C.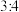 | D. |
您最近一年使用:0次
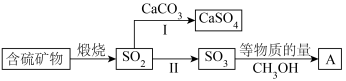
3 . 工业上煅烧含硫矿物产生的 可以按如下流程脱除或利用。
可以按如下流程脱除或利用。
已知: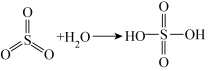
请回答:
(1)富氧煅烧燃煤产生的低浓度的 可以在炉内添加
可以在炉内添加 通过途径Ⅰ脱除,写出反应方程式
通过途径Ⅰ脱除,写出反应方程式___________ 。
(2)煅烧含硫量高的矿物得到高浓度的 ,通过途径Ⅱ最终转化为化合物A。
,通过途径Ⅱ最终转化为化合物A。
①下列说法正确的是___________ 。
A.燃煤中的有机硫主要呈正价 B.化合物A具有酸性
C.化合物A是一种无机酸酯 D.工业上途径Ⅱ产生的 也可用浓
也可用浓 吸收
吸收
②一定压强下,化合物A的沸点低于硫酸的原因是___________ 。
(3)设计实验验证化合物A中含有S元素_____ ;写出实验过程中涉及的反应方程式____ 。
 可以按如下流程脱除或利用。
可以按如下流程脱除或利用。
已知:
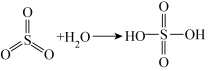
请回答:
(1)富氧煅烧燃煤产生的低浓度的
 可以在炉内添加
可以在炉内添加 通过途径Ⅰ脱除,写出反应方程式
通过途径Ⅰ脱除,写出反应方程式(2)煅烧含硫量高的矿物得到高浓度的
 ,通过途径Ⅱ最终转化为化合物A。
,通过途径Ⅱ最终转化为化合物A。①下列说法正确的是
A.燃煤中的有机硫主要呈正价 B.化合物A具有酸性
C.化合物A是一种无机酸酯 D.工业上途径Ⅱ产生的
 也可用浓
也可用浓 吸收
吸收②一定压强下,化合物A的沸点低于硫酸的原因是
(3)设计实验验证化合物A中含有S元素
您最近一年使用:0次
名校
解题方法
4 . 探究硫及其化合物的性质,下列方案设计、现象和结论中有不正确的是
实验方案 | 现象 | 结论 | |
A | 在过硫化钠(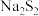 )中加入稀盐酸 )中加入稀盐酸 | 产生淡黄色沉淀和臭鸡蛋气味的气体。 | 发生歧化反应: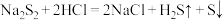 |
B | 已知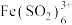 呈红棕色,将 呈红棕色,将 气体通入 气体通入 溶液中 溶液中 | 溶液先变为红棕色,过一段时间又变成浅绿色。 |  与 与 络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大。 络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大。 |
C | 燃着的镁条插入盛有 的集气瓶中。冷却后,往集气瓶中加入适量稀盐酸,静置,取少量上层清液于试管中,滴加少量 的集气瓶中。冷却后,往集气瓶中加入适量稀盐酸,静置,取少量上层清液于试管中,滴加少量 溶液。 溶液。 | 剧烈燃烧,集气瓶口有淡黄色固体附着,集气瓶底有白色固体生成。试管中没有产生黑色沉淀 | 镁能在 中燃烧: 中燃烧: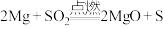 |
D | 探究电石与水的反应 | 将电石与饱和食盐水反应产生的气体通入酸性高锰酸钾溶液,观察现象 | 若酸性高锰酸钾溶液褪色,说明电石与水反应生成了乙炔 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-04-22更新
|
1841次组卷
|
6卷引用:浙江省天域全国名校协作体2022-2023学年高三下学期4月阶段性联考化学试题
浙江省天域全国名校协作体2022-2023学年高三下学期4月阶段性联考化学试题重庆市万州第二高级中学2023-2024学年高三上学期7月月考化学试题(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)湖南省长沙市第一中学2023-2024学年高三上学期月考卷(三)化学试题江西省抚州市乐安县第二中学2023-2024学年高三上学期11月期中化学试题2024年山东省潍坊市高三下学期高考模拟训练调研试题(二)
名校
解题方法
5 . 某钾盐X由四种元素组成,某小组按如下流程进行实验。请回答:
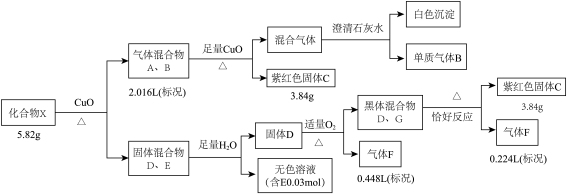
已知:相同条件下,A、B为中学常见气体且密度相同。D、E均为二元化合物,气体F能使品红溶液褪色且通入无色溶液E中,有淡黄色沉淀生成。
(1)气体B的电子式是___________ ,C的化学式是___________ 。
(2)写出固体混合物D、G共热所发生的化学反应方程式___________ 。
(3)无色溶液E中滴加盐酸观察到气泡。收集少量气体通入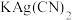 溶液,观察到黑色沉淀生成。写出生成沉淀的离子反应方程式(发生非氧化还原反应)
溶液,观察到黑色沉淀生成。写出生成沉淀的离子反应方程式(发生非氧化还原反应)___________ 。
(4)将G溶于氨水得到一无色溶液,设计实验检验无色溶液中主要离子___________ 。

已知:相同条件下,A、B为中学常见气体且密度相同。D、E均为二元化合物,气体F能使品红溶液褪色且通入无色溶液E中,有淡黄色沉淀生成。
(1)气体B的电子式是
(2)写出固体混合物D、G共热所发生的化学反应方程式
(3)无色溶液E中滴加盐酸观察到气泡。收集少量气体通入
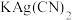 溶液,观察到黑色沉淀生成。写出生成沉淀的离子反应方程式(发生非氧化还原反应)
溶液,观察到黑色沉淀生成。写出生成沉淀的离子反应方程式(发生非氧化还原反应)(4)将G溶于氨水得到一无色溶液,设计实验检验无色溶液中主要离子
您最近一年使用:0次
2023-04-14更新
|
784次组卷
|
3卷引用:浙江省绍兴市2023届高三二模考试化学试题
解题方法
6 . 化合物X由三种元素组成,某学习小组按如下流程进行实验:
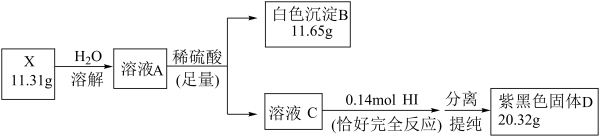
其中,溶液C含有一种摩尔质量为 的含氧弱酸,其物质的量为
的含氧弱酸,其物质的量为 。
。
(1)X的组成元素是_______ ,X的化学式是_______ 。
(2)写出溶液A与足量稀硫酸反应的化学方程式_______ 。
(3)写出生成紫黑色固体D的离子方程式_______ 。
(4)请设计实验检验溶液C中的一种阴离子_______ 。

其中,溶液C含有一种摩尔质量为
 的含氧弱酸,其物质的量为
的含氧弱酸,其物质的量为 。
。(1)X的组成元素是
(2)写出溶液A与足量稀硫酸反应的化学方程式
(3)写出生成紫黑色固体D的离子方程式
(4)请设计实验检验溶液C中的一种阴离子
您最近一年使用:0次
23-24高一上·浙江·期末
7 . 将一定量的铁和铜组成的混合物加入稀硝酸中,金属完全溶解(假设反应中还原产物只有NO)。向反应后的溶液中加入3mol·L-1NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g。下列叙述不正确的是
| A.当生成的沉淀量达到最大时,消耗NaOH溶液的体积V≥100mL |
| B.当金属全部溶解时收集到NO气体的体积折算成标准状况为2.24L |
| C.参加反应的金属的总质量3.6g<m<9.6g |
| D.当金属全部溶解时,参加反应的硝酸的物质的量一定是0.3mol |
您最近一年使用:0次
名校
解题方法
8 . 对于反应: ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是| A.该反应中,有三种元素化合价发生改变 |
B.该反应的还原剂为 和 和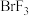 ,氧化产物为 ,氧化产物为 和 和 |
C.1.5mol 参加反应,被 参加反应,被 还原的 还原的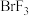 为0.4mol 为0.4mol |
D.1.5mol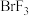 参加反应,有4mol 参加反应,有4mol 转移 转移 |
您最近一年使用:0次
2023-03-11更新
|
1214次组卷
|
4卷引用:浙江省强基联盟2022-2023学年高三上学期选考仿真密卷化学试题
浙江省强基联盟2022-2023学年高三上学期选考仿真密卷化学试题(已下线)化学-2023年高考押题预测卷01(浙江卷)(含考试版、全解全析、参考答案、答题卡)湖南省邵阳市第二中学2023-2024学年高一上学期基础知识竞赛化学试题江西省宜春市丰城市第九中学2023-2024学年高一下学期4月月考化学试题
名校
9 . Ⅰ.回答下列问题:
(1)(NH4)2SO4溶液可以用来除铁锈的原因:_______ (用离子方程式说明)。
(2)部分弱酸的电离平衡常数如表:
室温下①0.1mol·L-1HCOONa②0.1 mol·L-1 NaClO③0.1 mol·L-1Na2CO3④ 0.1 mol·L-1NaHCO3溶液的pH由大到小的关系为_______ 。
(3)根据上述电离平衡常数,试写出下列化学反应的离子方程式:
①向碳酸钠溶液中通入少量二氧化硫气体_______
②向碳酸钠溶液中滴入过量甲酸_______
Ⅱ.常温下,HNO2的电离平衡常数Ka =2.6×10-4,亚硝酸钠(NaNO2)是一种重要的食品添加剂,由于其外观及味道都与食盐非常相似,误食工业用盐造成食物中毒的事件时有发生。
(4)亚硝酸钠有毒,不能随意丢弃,实验室一般将其与饱和氯化铵溶液共热使之转化成无毒无公害的物质,其产物之一为无色无味气体,则反应的化学方程式为_______ 。
(5)某活动小组同学设计实验方案鉴别NaCl溶液和NaNO2溶液,请填写下列表格。
Ⅲ.活动小组同学采用如下装置制备NaNO2(装置可重复使用,部分夹持仪器已省略)。

已知:①2NO+Na2O2=2NaNO2,
②酸性条件下,NO、NO2都能与 反应生成
反应生成 和Mn2+;NaNO2能使酸性高锰酸钾溶液褪色。
和Mn2+;NaNO2能使酸性高锰酸钾溶液褪色。
(6)实验装置的连接顺序为A→_______→_______→_______→_______→B;_
(7)C瓶内发生反应的离子方程式为_______ 。
(8)为了测定亚硝酸钠的含量,称取4.0g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.10mol·L-1的酸性KMnO4溶液进行滴定,实验所得数据如下表。
①第一组实验数据出现较明显异常,造成异常的原因可能是_______ (填字母序号)。
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.滴定前滴定管尖嘴中有气泡,滴定后滴定管尖嘴无气泡
c.判断终点时,滴入一滴酸性KMnO4溶液,锥形瓶内溶液呈浅红色,振荡后立即褪色
d.观察滴定终点时俯视读数
②根据表中数据进行计算,所制得的固体中亚硝酸钠的质量分数为_______ 。
(1)(NH4)2SO4溶液可以用来除铁锈的原因:
(2)部分弱酸的电离平衡常数如表:
| 弱酸 | HCOOH | HClO | H2CO3 | H2SO3 |
| 电离平衡常数(25℃) | Ka =1.77×10-4 | Ka= 4.0×10-8 | Ka1=4.3 ×10-7 Ka2=4.7×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
(3)根据上述电离平衡常数,试写出下列化学反应的离子方程式:
①向碳酸钠溶液中通入少量二氧化硫气体
②向碳酸钠溶液中滴入过量甲酸
Ⅱ.常温下,HNO2的电离平衡常数Ka =2.6×10-4,亚硝酸钠(NaNO2)是一种重要的食品添加剂,由于其外观及味道都与食盐非常相似,误食工业用盐造成食物中毒的事件时有发生。
(4)亚硝酸钠有毒,不能随意丢弃,实验室一般将其与饱和氯化铵溶液共热使之转化成无毒无公害的物质,其产物之一为无色无味气体,则反应的化学方程式为
(5)某活动小组同学设计实验方案鉴别NaCl溶液和NaNO2溶液,请填写下列表格。
| 选用药品 | 实验现象(NaNO2溶液) | 利用NaNO2的性质 |
| ①酚酞试液 | ||
| ②淀粉-KI试纸 |
Ⅲ.活动小组同学采用如下装置制备NaNO2(装置可重复使用,部分夹持仪器已省略)。

已知:①2NO+Na2O2=2NaNO2,
②酸性条件下,NO、NO2都能与
 反应生成
反应生成 和Mn2+;NaNO2能使酸性高锰酸钾溶液褪色。
和Mn2+;NaNO2能使酸性高锰酸钾溶液褪色。(6)实验装置的连接顺序为A→_______→_______→_______→_______→B;
(7)C瓶内发生反应的离子方程式为
(8)为了测定亚硝酸钠的含量,称取4.0g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.10mol·L-1的酸性KMnO4溶液进行滴定,实验所得数据如下表。
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.滴定前滴定管尖嘴中有气泡,滴定后滴定管尖嘴无气泡
c.判断终点时,滴入一滴酸性KMnO4溶液,锥形瓶内溶液呈浅红色,振荡后立即褪色
d.观察滴定终点时俯视读数
②根据表中数据进行计算,所制得的固体中亚硝酸钠的质量分数为
您最近一年使用:0次
22-23高一上·天津南开·期末
名校
解题方法
10 . 从某含有 、
、 、
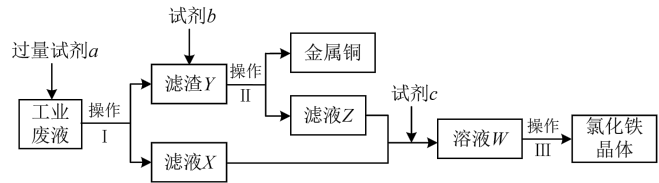
、 的工业废液中回收铜并制备氯化铁晶体的流程如下,则下列说法不正确的是
的工业废液中回收铜并制备氯化铁晶体的流程如下,则下列说法不正确的是
 、
、 、
、 的工业废液中回收铜并制备氯化铁晶体的流程如下,则下列说法不正确的是
的工业废液中回收铜并制备氯化铁晶体的流程如下,则下列说法不正确的是
| A.试剂a为铁,试剂b为稀硫酸 |
B.加入试剂a过程中,有红色固体析出后,说明溶液中 已经反应完全 已经反应完全 |
C.试剂c可为 溶液,相应的反应为 溶液,相应的反应为 |
| D.溶液W可作“腐蚀液”腐蚀覆铜板 |
您最近一年使用:0次
2023-01-07更新
|
1439次组卷
|
5卷引用:【2023】【高一下】【期中考】【328】【高中化学】
(已下线)【2023】【高一下】【期中考】【328】【高中化学】浙江省余姚中学2023-2024学年高一下学期3月质量检测化学(选考)试题天津市南开中学2022-2023学年高一上学期期末考试化学试题(已下线)专项02 氧化还原反应的概念、规律及综合应用-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(天津专用)安徽省安庆市第七中学2023-2024学年高一下学期开学考试化学试题



