1 . 向 和
和 的混合溶液中不断通入
的混合溶液中不断通入 ,溶液中n(含碘的某微粒)和n(含铁的某微粒)随
,溶液中n(含碘的某微粒)和n(含铁的某微粒)随 的变化曲线如图所示。(已知:①
的变化曲线如图所示。(已知:① 可将
可将 氧化成
氧化成 ;②
;②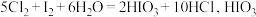 为强酸)下列说法中错误的是
为强酸)下列说法中错误的是

 和
和 的混合溶液中不断通入
的混合溶液中不断通入 ,溶液中n(含碘的某微粒)和n(含铁的某微粒)随
,溶液中n(含碘的某微粒)和n(含铁的某微粒)随 的变化曲线如图所示。(已知:①
的变化曲线如图所示。(已知:① 可将
可将 氧化成
氧化成 ;②
;②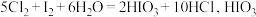 为强酸)下列说法中错误的是
为强酸)下列说法中错误的是
A.还原性: |
B.b点溶液中 |
C.a点时已通入标准状况下氯气的总体积为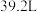 |
D.c点溶液中阴离子的个数为 |
您最近一年使用:0次
2023-12-01更新
|
878次组卷
|
4卷引用:广东省深圳市七校2023-2024学年高一上学期期中联考化学试题
解题方法
2 . 某小组对Cu和 的反应进行相关实验探究。
的反应进行相关实验探究。
【实验探究】实验i:向装有0.5gCu的烧杯中加入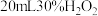 溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
(1)写出该反应的化学方程式:___________ 。
【继续探究】针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
(2)实验ii中:溶液变蓝的原因是___________ (用离子反应方程式表示);经检验产生的气体为氧气,产生氧气先慢后快的原因是___________ 。(不考虑温度的影响)。
(3)对比实验i和iii,为探究氨水对Cu的还原性或 氧化性的影响,该同学利用如图装置继续实验。
氧化性的影响,该同学利用如图装置继续实验。
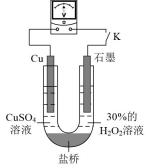
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
①解释步骤c中电压增大的原因:___________ 。
②若向U型管左侧溶液中滴加硫酸后,电压不变,继续向U型管右侧溶液中滴加硫酸后,电压增大了z。则可以得出的结论是:___________ 。
(4)基于以上实验,影响Cu与 反应的因素有
反应的因素有___________ 。(任写一条)
(5)结合上述实验,下列说法正确的是___________ 。
A.电化学是研究物质氧化性、还原性的重要手段之一
B.实验ii中发生的反应中, 只体现氧化性
只体现氧化性
C.在还原反应(氧化反应)中,增大反应物浓度或降低生成物浓度,氧化剂(还原剂)的氧化性(还原性)增强
 的反应进行相关实验探究。
的反应进行相关实验探究。【实验探究】实验i:向装有0.5gCu的烧杯中加入
 溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。(1)写出该反应的化学方程式:
【继续探究】针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
| 装置 | 序号 | 试剂a | 现象 |
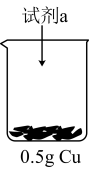 | ii |  与 与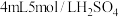 混合液 混合液 | Cu表面产生少量气泡,溶液逐渐变蓝,后产生较多气泡 |
| iii | 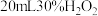 与 与 氨水混合液 氨水混合液 | 溶液立即变为深蓝色,产生大量气泡,Cu表面有少量蓝色不溶物 |
(3)对比实验i和iii,为探究氨水对Cu的还原性或
 氧化性的影响,该同学利用如图装置继续实验。
氧化性的影响,该同学利用如图装置继续实验。
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
①解释步骤c中电压增大的原因:
②若向U型管左侧溶液中滴加硫酸后,电压不变,继续向U型管右侧溶液中滴加硫酸后,电压增大了z。则可以得出的结论是:
(4)基于以上实验,影响Cu与
 反应的因素有
反应的因素有(5)结合上述实验,下列说法正确的是
A.电化学是研究物质氧化性、还原性的重要手段之一
B.实验ii中发生的反应中,
 只体现氧化性
只体现氧化性C.在还原反应(氧化反应)中,增大反应物浓度或降低生成物浓度,氧化剂(还原剂)的氧化性(还原性)增强
您最近一年使用:0次
3 . 有机化学中的氧化还原反应是一门艺术,如何选择温和的氧化剂,在提高反应效率的同时,不破坏底物分子的结构,是科学家们不断追求的目标。DMP(Dess-Martin periodinane)是现代有机合成中应用最为广泛的、温和型和高选择性氧化剂之一,它的分子结构和氧化机理如图所示,下列有关说法错误的是
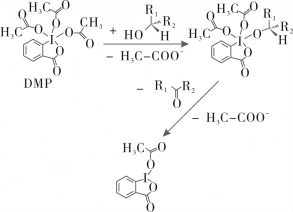

| A.DMP是一种高价碘氧化剂 | B.氧化过程中,Ⅰ的化合价降低1 |
| C.反应产生了醋酸根离子 | D.还原产物中的Ⅰ满足8隅律 |
您最近一年使用:0次
名校
解题方法
4 . 1.52g铜镁合金完全溶解于50mL14mol/L的浓硝酸中,得到NO2和NO的混合气体896mL(标准状况),向反应后的溶液中加入1.0mol·L-1NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀。下列说法不正确的是
| A.该合金中铜与镁的物质的量之比是2∶1 |
| B.固体溶解后的溶液中硝酸的物质的量为0.6mol |
| C.得到2.54g沉淀时,加入NaOH溶液的体积至少为600mL |
| D.反应过程中转移的电子数是0.06NA(NA代表阿伏加德罗常数的值) |
您最近一年使用:0次
名校
解题方法
5 . 工业上以赤泥[主要成分是Sc2O3,另含有少量Fe2O3、SiO2(不溶于酸)、Al2O3等]为主要原料提取氧化钪,其工艺流程如图所示(P2O4是一种磷酸酯萃取剂,草酸化学式为H2C2O4)。
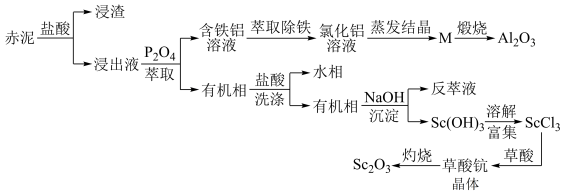
回答下列问题:
(1)赤泥经盐酸处理后所得“浸渣”主要成分为____ (化学式)。
(2)赤泥“盐酸酸浸”时不宜温度过高,原因是____ 。
(3)P2O4萃取浸出液,其浓度、料液温度对萃取率的影响如表所示,萃取时P2O4最佳浓度及料液温度分别为____ 、____ ;
P2O4浓度对萃取率的影响如表:
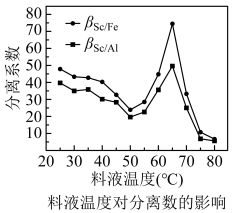
料液温度对分离系数的影响如图:
(4)M经煅烧后可得到Al2O3,则M成分为____ 。
(5)为探究所得草酸钪晶体Sc2(C2O4)3·xH2O中结晶水的含量,取2.96g样品(纯度为75%),灼烧得到0.69gSc2O3固体,则x=____ 。
(6)草酸钪晶体在空气中灼烧分解反应方程式为____ 。

回答下列问题:
(1)赤泥经盐酸处理后所得“浸渣”主要成分为
(2)赤泥“盐酸酸浸”时不宜温度过高,原因是
(3)P2O4萃取浸出液,其浓度、料液温度对萃取率的影响如表所示,萃取时P2O4最佳浓度及料液温度分别为
P2O4浓度对萃取率的影响如表:
试验编号 | P2O4浓度/% | 分相情况 | 钪萃取率/% | 铁萃取率/% |
1-1 | 1 | 分相快 | 90.76 | 15.82 |
1-2 | 2 | 分相容易 | 91.53 | 19.23 |
1-3 | 3 | 分相容易 | 92.98 | 13.56 |
1-4 | 4 | 有第三相 | 90.69 | 30.12 |
1-5 | 5 | 轻微乳化 | 91.74 | 39.79 |
料液温度对分离系数的影响如图:

(4)M经煅烧后可得到Al2O3,则M成分为
(5)为探究所得草酸钪晶体Sc2(C2O4)3·xH2O中结晶水的含量,取2.96g样品(纯度为75%),灼烧得到0.69gSc2O3固体,则x=
(6)草酸钪晶体在空气中灼烧分解反应方程式为
您最近一年使用:0次
名校
解题方法
6 . 将一定量的氯气通入 的氢氧化钾浓溶液中,加热少许时间后,恰好完全反应,测得溶液中含氯元素的离子有:
的氢氧化钾浓溶液中,加热少许时间后,恰好完全反应,测得溶液中含氯元素的离子有: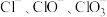 。下列说法
。下列说法不正确 的是
 的氢氧化钾浓溶液中,加热少许时间后,恰好完全反应,测得溶液中含氯元素的离子有:
的氢氧化钾浓溶液中,加热少许时间后,恰好完全反应,测得溶液中含氯元素的离子有: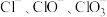 。下列说法
。下列说法A.一共消耗了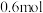 氯气 氯气 |
B.当溶液中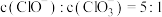 时,反应的离子方程式为: 时,反应的离子方程式为: |
C.若反应中转移的电子为 ,则 ,则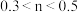 |
D.反应生成的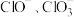 有一定的氧化性 有一定的氧化性 |
您最近一年使用:0次
2023-02-16更新
|
990次组卷
|
2卷引用:广东省大湾区2022-2023学年高一上学期期末联考化学试题
2023·重庆·模拟预测
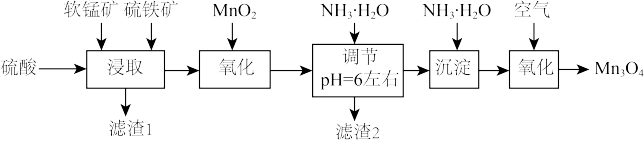
7 . 四氧化三锰是一种重要的电子和新能源基础原材料,可以用于生产软磁锰锌铁氧体、锂电正极材料锰酸锂和负温度系数热敏电阻等。以软锰矿(主要成分为 还含少量Fe、Si、Al等的氧化物)和硫铁矿(主要成分
还含少量Fe、Si、Al等的氧化物)和硫铁矿(主要成分 )为原料制备大颗粒的电池
)为原料制备大颗粒的电池 。
。
说明:
Ⅰ.“浸取”:研究发现,酸浸时 和
和 颗粒反应的原理如图1所示(部分产物未标出)。
颗粒反应的原理如图1所示(部分产物未标出)。
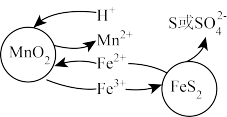
图1
Ⅱ.通空气“氧化”:将“沉淀”步骤所得含少量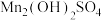 的
的 固体滤出,洗净,加水打成浆,浆液边加热边持续通入空气,制得
固体滤出,洗净,加水打成浆,浆液边加热边持续通入空气,制得 。
。
Ⅲ.氢氧化物形式完全沉淀时溶液的pH见表:
(1)滤渣1中主要成分的化学式为_______ 。
(2)随硫铁矿的增加,锰的浸出率降低,可能的原因是_______ 。
(3)写出“浸取”时 与
与 反应的离子方程式为
反应的离子方程式为_______ 。
(4)加入 “氧化”的目的是
“氧化”的目的是_______ 。
(5)检验“沉淀”已洗净的操作是_______ 。
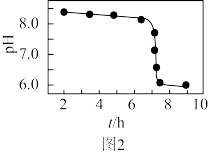
(6)“沉淀”加热通空气过程中溶液pH随时间变化如图2所示,其中pH先基本不变后迅速下降的原因是_______ 。
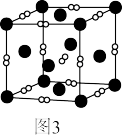
(7)一个立方体结构的 晶胞如图3所示,距离
晶胞如图3所示,距离 最近的
最近的 有
有_______ 个,已知阿伏加德罗数值为 ,则
,则 的晶体密度为
的晶体密度为 ,则晶胞的边长为
,则晶胞的边长为_______ nm(用含ρ、 的代数式表示)。
的代数式表示)。
 还含少量Fe、Si、Al等的氧化物)和硫铁矿(主要成分
还含少量Fe、Si、Al等的氧化物)和硫铁矿(主要成分 )为原料制备大颗粒的电池
)为原料制备大颗粒的电池 。
。
说明:
Ⅰ.“浸取”:研究发现,酸浸时
 和
和 颗粒反应的原理如图1所示(部分产物未标出)。
颗粒反应的原理如图1所示(部分产物未标出)。
图1
Ⅱ.通空气“氧化”:将“沉淀”步骤所得含少量
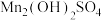 的
的 固体滤出,洗净,加水打成浆,浆液边加热边持续通入空气,制得
固体滤出,洗净,加水打成浆,浆液边加热边持续通入空气,制得 。
。Ⅲ.氢氧化物形式完全沉淀时溶液的pH见表:
| 沉淀物 |  |  |  |  |
| 开始沉淀的pH | 3.4 | 2.2 | 6.3 | 8.1 |
| 完全沉淀的pH | 5.2 | 3.2 | 9.7 | 10.4 |
(2)随硫铁矿的增加,锰的浸出率降低,可能的原因是
(3)写出“浸取”时
 与
与 反应的离子方程式为
反应的离子方程式为(4)加入
 “氧化”的目的是
“氧化”的目的是(5)检验“沉淀”已洗净的操作是
(6)“沉淀”加热通空气过程中溶液pH随时间变化如图2所示,其中pH先基本不变后迅速下降的原因是

(7)一个立方体结构的
 晶胞如图3所示,距离
晶胞如图3所示,距离 最近的
最近的 有
有 ,则
,则 的晶体密度为
的晶体密度为 ,则晶胞的边长为
,则晶胞的边长为 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
解题方法
8 . “84消毒液”广泛应用于杀菌消毒,其有效成分是 。实验小组制备消毒液,并利用其性质探究制备碘水的方法。
。实验小组制备消毒液,并利用其性质探究制备碘水的方法。
资料:i. 的电离常数为
的电离常数为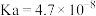 ;
; 的电离常数为
的电离常数为 、
、
ii.碘的化合物主要以 和
和 的形式存在,
的形式存在, 。
。
iii.碘单质能与 反应:
反应: (
( 低浓度时显黄色,高浓度时为棕色)。
低浓度时显黄色,高浓度时为棕色)。
I.制备消毒液(夹持装置略)

(1)制备 的离子反应方程式
的离子反应方程式_______ 。
(2)结合资料i,写出D中反应的化学方程式_______ 。
II.利用消毒液的性质探究碘水的制备方法
将某品牌“84消毒液”稀释10倍,各取100mL于三个烧杯中,设计如下实验方案制备碘水:
(3)针对烧杯3“滴加淀粉溶液不变蓝”的原因,提出两种假设:
假设1:生成的I2在碱性溶液中不能存在。
设计实验a证实了假设1成立,实验a的操作及现象是_______ 。
假设2:过量的 将反应生成的
将反应生成的 氧化为
氧化为 。
。
设计实验b证实了假设2成立。 氧化
氧化 生成
生成 的离子方程式是
的离子方程式是_______ 。
(4)某小组检验烧杯3所得溶液中含 :取烧杯3所得无色溶液少许,加入稀硫酸酸化的
:取烧杯3所得无色溶液少许,加入稀硫酸酸化的 溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在
溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在 ,说明理由
,说明理由_______ 。
(5)预测烧杯1反应后加淀粉溶液的实验现象,结合方程式说明预测依据_______ 。
(6)对比不同方案的实验现象,得出制取碘水的最佳方法要关注的因素是_______ 。
 。实验小组制备消毒液,并利用其性质探究制备碘水的方法。
。实验小组制备消毒液,并利用其性质探究制备碘水的方法。资料:i.
 的电离常数为
的电离常数为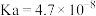 ;
; 的电离常数为
的电离常数为 、
、
ii.碘的化合物主要以
 和
和 的形式存在,
的形式存在, 。
。iii.碘单质能与
 反应:
反应: (
( 低浓度时显黄色,高浓度时为棕色)。
低浓度时显黄色,高浓度时为棕色)。I.制备消毒液(夹持装置略)

(1)制备
 的离子反应方程式
的离子反应方程式(2)结合资料i,写出D中反应的化学方程式
II.利用消毒液的性质探究碘水的制备方法
将某品牌“84消毒液”稀释10倍,各取100mL于三个烧杯中,设计如下实验方案制备碘水:
| 方案 | 操作 | 现象 | 反应后加淀粉溶液 |
| 1 | 烧杯1溶液中加入9g 固体 固体 | 溶液为橙黄色 | …… |
| 2 | 烧杯2溶液中加入9g 固体,再加入1 固体,再加入1 盐酸10mL 盐酸10mL | 溶液颜色快速加深,呈紫红色 | 变蓝 |
| 3 | 烧杯3溶液中加入少量 固体(小于0.5g) 固体(小于0.5g) | 振荡后溶液保持无色 | 不变蓝 |
假设1:生成的I2在碱性溶液中不能存在。
设计实验a证实了假设1成立,实验a的操作及现象是
假设2:过量的
 将反应生成的
将反应生成的 氧化为
氧化为 。
。设计实验b证实了假设2成立。
 氧化
氧化 生成
生成 的离子方程式是
的离子方程式是(4)某小组检验烧杯3所得溶液中含
 :取烧杯3所得无色溶液少许,加入稀硫酸酸化的
:取烧杯3所得无色溶液少许,加入稀硫酸酸化的 溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在
溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在 ,说明理由
,说明理由(5)预测烧杯1反应后加淀粉溶液的实验现象,结合方程式说明预测依据
(6)对比不同方案的实验现象,得出制取碘水的最佳方法要关注的因素是
您最近一年使用:0次
2022-12-30更新
|
1167次组卷
|
4卷引用:广东省珠海市第一中学2022-2023学年高三下学期2月月考化学试题
21-22高三上·广东广州·期末
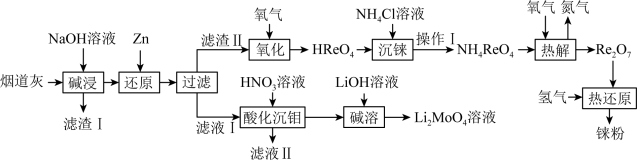
9 . 铼(Re)是熔点和沸点较高的金属单质之一,用于制造高效能喷射引擎和火箭引擎。钼酸锂(Li2MoO4)的外观为白色结晶粉末,用于电极材料、金属陶瓷的制作。从辉钼矿氧化焙烧后的烟道灰(主要成分有SiO2、Re2O7、MoO3、CuO、Fe3O4)中提取铼粉和制钼酸锂的流程如下图所示。
已知:
I.Re2O7是酸性氧化物,过铼酸(HReO4)是易溶于水的一元强酸,但不具有强氧化性。
Ⅱ.过铼酸铵(NH4ReO4)是白色片状晶体,微溶于冷水,溶于热水。
回答下列问题:
(1)“碱浸”时,Re2O7和MoO3分别与NaOH发生以下反应_______ (填写化学方程式)、MoO3+2NaOH=NaMoO4+H2O,则“滤渣I”的主要成分为_______ (填化学式)。
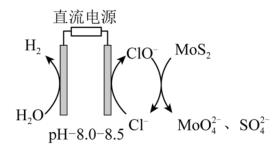
(2)“还原”时,Zn被氧化成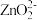 ,铼的化合物被还原生成难溶的2ReO2·2H2O,该反应的离子方程式为
,铼的化合物被还原生成难溶的2ReO2·2H2O,该反应的离子方程式为___________ 。
(3)“沉铼”时,加入热NH4C1溶液至产生白色沉淀,为使沉淀充分析出并分离得到纯净NH4ReO4晶体,“操作I”包括___________ 、___________ 、洗涤、干燥。
(4)“热解”时,发生反应的化学方程式为___________ 。
(5)“酸化沉钼”过程溶液pH和反应时间对钼酸的析出有很大影响,根据下图中数据判断最佳的“酸化沉钼”条件:反应时间为___________ min、pH为___________ 。
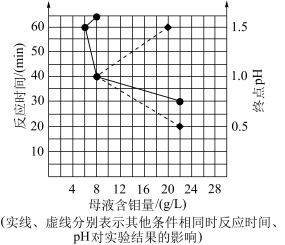
(6)电氧化法是一种极具发展前景的钼精矿冶金工艺,其工作原理如图所示。电解时,若维持电流强度为0.5A(相当于每秒通过5×10-6mol电子),电解90min,理论上消耗MoS2的质量为______ g。

已知:
I.Re2O7是酸性氧化物,过铼酸(HReO4)是易溶于水的一元强酸,但不具有强氧化性。
Ⅱ.过铼酸铵(NH4ReO4)是白色片状晶体,微溶于冷水,溶于热水。
回答下列问题:
(1)“碱浸”时,Re2O7和MoO3分别与NaOH发生以下反应
(2)“还原”时,Zn被氧化成
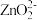 ,铼的化合物被还原生成难溶的2ReO2·2H2O,该反应的离子方程式为
,铼的化合物被还原生成难溶的2ReO2·2H2O,该反应的离子方程式为(3)“沉铼”时,加入热NH4C1溶液至产生白色沉淀,为使沉淀充分析出并分离得到纯净NH4ReO4晶体,“操作I”包括
(4)“热解”时,发生反应的化学方程式为
(5)“酸化沉钼”过程溶液pH和反应时间对钼酸的析出有很大影响,根据下图中数据判断最佳的“酸化沉钼”条件:反应时间为

(6)电氧化法是一种极具发展前景的钼精矿冶金工艺,其工作原理如图所示。电解时,若维持电流强度为0.5A(相当于每秒通过5×10-6mol电子),电解90min,理论上消耗MoS2的质量为

您最近一年使用:0次
2022-03-08更新
|
857次组卷
|
6卷引用:广东省华师附中、实验中学、深圳中学、广雅中学四校2021-2022学年高三上学期期末联考化学试题
(已下线)广东省华师附中、实验中学、深圳中学、广雅中学四校2021-2022学年高三上学期期末联考化学试题广东名校2021-2022学年高三下学期开学测试化学试题湖南省衡阳市第八中学2021-2022学年高三下学期开学考试(第六次月考)化学试题湖南省永州市第四中学2022届高三下学期期中考试化学试题湖南省株洲市第四中学2022-2023学年高三上学期第四次月考化学试题湖南省株洲市九方中学2022-2023学年高三上学期第二次月考化学试题
名校
解题方法
10 . 取一定质量的NaBr、NaI的混合物平均分成五等分,分别加水配成溶液并编号为甲、乙、丙、丁、戊,再分别向各溶液中通入一定体积的氯气,将反应后所得溶液蒸干灼烧得固体,通入氯气的体积与最终所得固体质量记录如下:
下列实验结论正确的是
| 编号 | 甲 | 乙 | 丙 | 丁 | 戊 |
| 固体组成 | NaCl | ||||
| Cl2的体积/mL | V | 2V | 3V | 4V | 5V |
| 固体质量/g | 54.62 | 43.64 | 35.48 | 30.14 | 29.25 |
| A.甲溶液中发生的反应是Cl2+2Br-=2Cl-+Br2 |
| B.乙中固体组成为NaBr、NaCl |
| C.标准状况下Cl2的体积V为2688mL |
| D.原混合物中NaBr的物质的量为1mol |
您最近一年使用:0次
2020-11-19更新
|
1658次组卷
|
5卷引用:广东省深圳外国语学校2021届高三第二次月考化学试题
广东省深圳外国语学校2021届高三第二次月考化学试题(已下线)解密07 非金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密07 非金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密07 非金属及其化合物(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)江西省赣州市全南中学2023-2024学年高三上学期11月期中考试化学试题



