1 . 亚硝酸钠是一种工业盐,用途广泛;外观与食盐非常相似,但毒性较强。某化学兴趣小组对食盐与亚硝酸钠进行了如下探究:
㈠鉴别NaCl和NaNO2
(1)测定溶液pH
用pH试纸分别测定0.1mol•L-1两种盐溶液的pH,测得NaNO2溶液呈碱性.NaNO2溶液呈碱性的原因是__________ (用离子方程式解释),NaNO2溶液中c(HNO2)=__________ (用溶液中其它离子的浓度关系式表示)。
(2)沉淀法
取2mL0.1mol•L-1两种盐溶液于试管中,分别滴加几滴稀硝酸银溶液,两支试管均产生白色沉淀,分别滴加几滴稀硝酸并振荡,盛NaNO2溶液的试管中沉淀溶解。该温度下Ksp(AgNO2)=2×10-8 (mol•L-1)2; Ksp(AgCl)=1.8×10-10(mol•L-1)2,则反应AgNO2(s)+Cl-(aq)═AgCl(s)+NO2-(aq)的化学平衡常数K=__________ (计算结果写成分数)。
(二)实验室可用如下装置(略去部分夹持仪器)备亚硝酸钠。
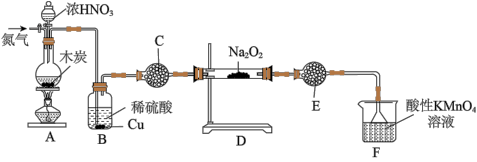
已知:①2NO+Na2O2=2NaNO2;②酸性条件下,NO和NO2都能与MnO4-反应生成NO3-和Mn2+;Na2O2能使酸性高锰酸钾溶液褪色.
(3)加热装置A前,先通一段时间N2,目的是__________ 。
(4)装置A中发生反应的化学方程式为__________ ,装置B的作用是__________ 。
(5)仪器C的名称为__________ ,其中盛放的药品为__________ (填名称)。
㈠鉴别NaCl和NaNO2
(1)测定溶液pH
用pH试纸分别测定0.1mol•L-1两种盐溶液的pH,测得NaNO2溶液呈碱性.NaNO2溶液呈碱性的原因是
(2)沉淀法
取2mL0.1mol•L-1两种盐溶液于试管中,分别滴加几滴稀硝酸银溶液,两支试管均产生白色沉淀,分别滴加几滴稀硝酸并振荡,盛NaNO2溶液的试管中沉淀溶解。该温度下Ksp(AgNO2)=2×10-8 (mol•L-1)2; Ksp(AgCl)=1.8×10-10(mol•L-1)2,则反应AgNO2(s)+Cl-(aq)═AgCl(s)+NO2-(aq)的化学平衡常数K=
(二)实验室可用如下装置(略去部分夹持仪器)备亚硝酸钠。

已知:①2NO+Na2O2=2NaNO2;②酸性条件下,NO和NO2都能与MnO4-反应生成NO3-和Mn2+;Na2O2能使酸性高锰酸钾溶液褪色.
(3)加热装置A前,先通一段时间N2,目的是
(4)装置A中发生反应的化学方程式为
(5)仪器C的名称为
您最近一年使用:0次
解题方法
2 . 铁及其化合物在日常生活、生产中应用广泛。
(1)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,工业上利用NaClO 和NaOH的混合溶液将2Fe(OH)3氧化性制备高铁酸钠,反应的化学方程式为______________________ ;高铁酸钠能用作新型净水剂的原理是____________________________ ;
(2)氧化铁红颜料跟某些油料混合,可以制成防锈油漆。以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下:
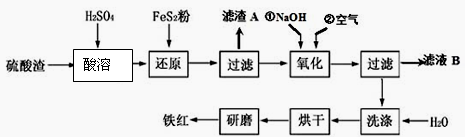
①酸溶过程中发生反应的化学方程式为___________ ,_____________ ,___________ ;“滤渣A”主要成分的化学式为_____________________ 。
②还原过程中加入FeS2的目的是将溶液中的Fe3 +还原为Fe2 +,而本身被氧化为H2SO4,请写出该反应的离子方程式_______________________________ ;
③氧化过程中,O2、NaOH与Fe2+反应的离子方程式为_____________ 。
④为了确保铁红的质量和纯度,氧化过程需要调节溶液的pH的范围是____________ ,
如果pH过大,可能引起的后果是_____________________ 。
(1)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,工业上利用NaClO 和NaOH的混合溶液将2Fe(OH)3氧化性制备高铁酸钠,反应的化学方程式为
(2)氧化铁红颜料跟某些油料混合,可以制成防锈油漆。以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下:

①酸溶过程中发生反应的化学方程式为
②还原过程中加入FeS2的目的是将溶液中的Fe3 +还原为Fe2 +,而本身被氧化为H2SO4,请写出该反应的离子方程式
③氧化过程中,O2、NaOH与Fe2+反应的离子方程式为
④为了确保铁红的质量和纯度,氧化过程需要调节溶液的pH的范围是
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
如果pH过大,可能引起的后果是
您最近一年使用:0次
2016-12-09更新
|
986次组卷
|
2卷引用:2016届宁夏回族自治区银川一中高三上第三次月考化学试卷



