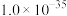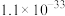1 . 中国科学院将分子 引入电解质中调整充电和放电反应途径,研制出了高功率可充电
引入电解质中调整充电和放电反应途径,研制出了高功率可充电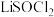 电池,工作原理如图所示,已知
电池,工作原理如图所示,已知 可与水发生反应。下列有关说法正确的是
可与水发生反应。下列有关说法正确的是
 引入电解质中调整充电和放电反应途径,研制出了高功率可充电
引入电解质中调整充电和放电反应途径,研制出了高功率可充电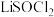 电池,工作原理如图所示,已知
电池,工作原理如图所示,已知 可与水发生反应。下列有关说法正确的是
可与水发生反应。下列有关说法正确的是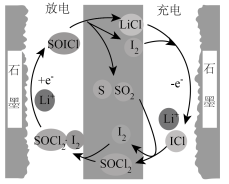
| A.该电池既可选用含水电解液,也可选无水电解液 |
B.放电时, 最终被氧化为 最终被氧化为 |
C.充电时,阴极反应式: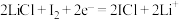 |
D.放电时,每产生 (标准状况下) (标准状况下) 时,电路中转移 时,电路中转移 电子 电子 |
您最近一年使用:0次
2024-03-21更新
|
526次组卷
|
3卷引用:黑龙江省部分学校2024届高三第二次模拟考试化学试题
名校
解题方法
2 . 镓是优良的半导体材料。氮化镓是制作发光二极管的新材料,用于雷达、卫星通信设备等。某工厂利用铝土矿(主要成分为 、
、 ,还有少量
,还有少量 等杂质)制备氮化镓流程如下:
等杂质)制备氮化镓流程如下:
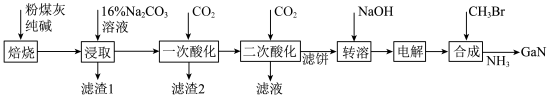
已知:①镓性质与铝相似,金属活动性介于锌和铁之间。
②当溶液中可溶组分浓度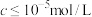 时,可认为已除尽。
时,可认为已除尽。
③金属离子氢氧化物的溶度积(25℃)
④ 、
、 均为两性,
均为两性, 的酸性略强于
的酸性略强于 。
。
回答下列问题:
(1)写出元素镓在周期表中的位置______ ,其简化电子排布式为______ 。
(2)“焙烧”后所得产物主要有______ (写化学式)。
(3)“一次酸化”的目的是______ 。
(4)“二次酸化”中 与足量
与足量 发生反应的离子方程式为
发生反应的离子方程式为______ 。
(5)“电解”可得金属镓(铝不干扰镓盐的电解),写出阴极电极反应式______ 。
(6)“合成”得到的三甲基镓与氨反应得到氮化镓,写出此反应的化学方程式______ 。
(7)25℃时,已知: 可溶于氨水中,
可溶于氨水中,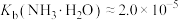 ,反应
,反应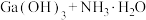
 的平衡常数
的平衡常数 ,计算反应
,计算反应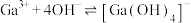 的平衡常数
的平衡常数
______ 。
 、
、 ,还有少量
,还有少量 等杂质)制备氮化镓流程如下:
等杂质)制备氮化镓流程如下:
已知:①镓性质与铝相似,金属活动性介于锌和铁之间。
②当溶液中可溶组分浓度
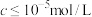 时,可认为已除尽。
时,可认为已除尽。③金属离子氢氧化物的溶度积(25℃)
|
|
| |
|
|
|
|
 、
、 均为两性,
均为两性, 的酸性略强于
的酸性略强于 。
。回答下列问题:
(1)写出元素镓在周期表中的位置
(2)“焙烧”后所得产物主要有
(3)“一次酸化”的目的是
(4)“二次酸化”中
 与足量
与足量 发生反应的离子方程式为
发生反应的离子方程式为(5)“电解”可得金属镓(铝不干扰镓盐的电解),写出阴极电极反应式
(6)“合成”得到的三甲基镓与氨反应得到氮化镓,写出此反应的化学方程式
(7)25℃时,已知:
 可溶于氨水中,
可溶于氨水中,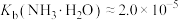 ,反应
,反应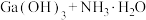
 的平衡常数
的平衡常数 ,计算反应
,计算反应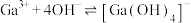 的平衡常数
的平衡常数
您最近一年使用:0次
3 . 铬酸铅俗称铬黄,是一种难溶于水的黄色固体,也是一种重要的黄色颜料,常用作橡胶、油墨、水彩、色纸等的着色剂。工业上用草酸泥渣(主要含草酸铅、硫酸铅)和铬矿渣(主要成分为 ,含有少量的
,含有少量的 )为原料制备铬酸铅,实现资源的回收再利用,其流程如下:
)为原料制备铬酸铅,实现资源的回收再利用,其流程如下:
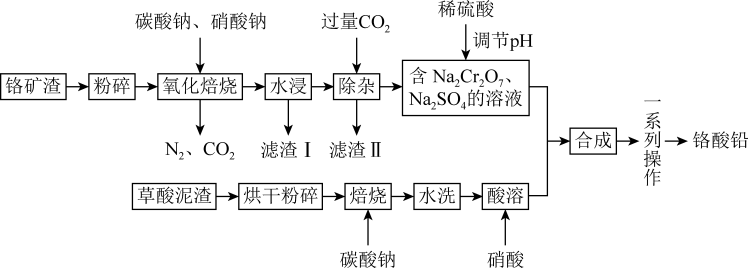
回答下列问题:
(1)将铬矿渣“粉碎"”的目的是_______ ;草酸泥渣“焙烧”后“水洗”的作用是_______ 。
(2)“滤渣Ⅱ”的主要成分是_______ (填化学式)。
(3)“氧化焙烧”时, 被氧化的反应的化学方程式为
被氧化的反应的化学方程式为_______ 。
(4)“一系列操作”包括_______ 、粉碎。
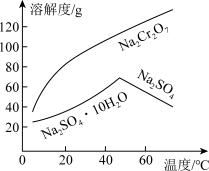
(5)为了使产品更纯,需将“含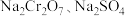 的溶液”分离提纯,依据如图所示的溶解度信息,“含
的溶液”分离提纯,依据如图所示的溶解度信息,“含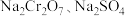 的溶液”分离提纯的操作是
的溶液”分离提纯的操作是_______ 。分离提纯后得到的固体的化学式为_______ 。
(6)“焙烧”时加入碳酸钠是为了将硫酸铅转化为氧化铅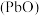 ,同时放出二氧化碳,该转化过程的化学方程式为
,同时放出二氧化碳,该转化过程的化学方程式为_______ 。
 ,含有少量的
,含有少量的 )为原料制备铬酸铅,实现资源的回收再利用,其流程如下:
)为原料制备铬酸铅,实现资源的回收再利用,其流程如下:
回答下列问题:
(1)将铬矿渣“粉碎"”的目的是
(2)“滤渣Ⅱ”的主要成分是
(3)“氧化焙烧”时,
 被氧化的反应的化学方程式为
被氧化的反应的化学方程式为(4)“一系列操作”包括
(5)为了使产品更纯,需将“含
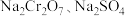 的溶液”分离提纯,依据如图所示的溶解度信息,“含
的溶液”分离提纯,依据如图所示的溶解度信息,“含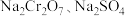 的溶液”分离提纯的操作是
的溶液”分离提纯的操作是
(6)“焙烧”时加入碳酸钠是为了将硫酸铅转化为氧化铅
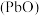 ,同时放出二氧化碳,该转化过程的化学方程式为
,同时放出二氧化碳,该转化过程的化学方程式为
您最近一年使用:0次
名校
4 . 将铁粉和铜粉的均匀混合物平均分成四等份,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成 的体积和剩余金属的质量如下表(设硝酸的还原产物只有
的体积和剩余金属的质量如下表(设硝酸的还原产物只有 )。下列说法正确的是
)。下列说法正确的是
 的体积和剩余金属的质量如下表(设硝酸的还原产物只有
的体积和剩余金属的质量如下表(设硝酸的还原产物只有 )。下列说法正确的是
)。下列说法正确的是| 编号 | ① | ② | ③ | ④ |
| 硝酸体积/mL | 100 | 200 | 300 | 400 |
| 剩余金属/g | 18.6 | 9.6 | 0 | 0 |
| NO体积/L | 2.24 | 4.48 | 6.72 | V |
A.①中溶液存在 | B.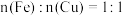 |
C.硝酸的浓度为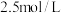 | D.④中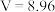 |
您最近一年使用:0次
2022-05-03更新
|
1508次组卷
|
3卷引用:黑龙江省鹤岗市第一中学2022-2023学年高一下学期5月期中考试化学试题
名校
解题方法
5 . 向mg由铁粉和铜粉组成的混合物中,加入某浓度的稀硝酸,充分反应后测得生成NO的体积[V(NO)](已换算成标准状况下)、m(固体剩余质量)随加入的稀硝酸的体积的变化如图所示(设硝酸的还原产物只有NO)。下列说法中正确的是
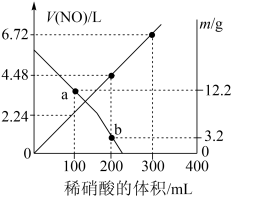

| A.稀硝酸的浓度为0.4mol·L-1 |
| B.a点时,100mL稀硝酸中溶解了Fe和Cu共8.4g |
| C.b点对应的溶液中可能含有的金属阳离子为Fe2+、Fe3+、Cu2+ |
| D.加入稀硝酸至400mL时,收集到的V(NO)约为6.91L |
您最近一年使用:0次
2022-05-03更新
|
3550次组卷
|
14卷引用:黑龙江省哈尔滨市第三中学校2022-2023学年高一下学期第一次验收考试化学试题
黑龙江省哈尔滨市第三中学校2022-2023学年高一下学期第一次验收考试化学试题湖北省黄冈市部分重点中学2021-2022学年高一下学期4月期中联考化学试题辽宁省县级重点高中协作体2021-2022学年高一下学期期中考试化学试题江西省重点2021-2022学年高一下学期5月联考化学试题湖南省衡阳市部分校2021-2022学年高一下学期期末考试化学试题山西省长治市2021-2022学年高一下学期期末联合考化学试题(已下线)微专题23 金属与硝酸反应的规律与计算-备战2023年高考化学一轮复习考点微专题(已下线)第13练 氮及其化合物-2023年高考化学一轮复习小题多维练(全国通用)辽宁省沈阳实验中学2022-2023学年高二上学期开学考试化学试题湖北省华中师范大学第一附属中学2022-2023学年高一上学期竞赛生10月测试化学试题江西省上饶市民校考试联盟2022—2023学年高一下学期阶段测试(四)化学试题新疆维吾尔自治区和田地区策勒县2022-2023学年高三上学期11月期中考试化学试题山东新高考2022-2023学年高一上学期质量测评模拟演练化学试题 四川省泸州市泸县第一中学2023-2024学年高一上学期1月期末化学试题
名校
解题方法
6 . 已知还原性:SO >I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是 ( )
>I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是 ( )
 >I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是 ( )
>I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是 ( )A.当a=b时,发生的离子反应为SO +Cl2+H2O=SO +Cl2+H2O=SO +2H++2Cl- +2H++2Cl- |
B.当5a=4b时,发生的离子反应为4SO +2I-+5Cl2+4H2O=4SO +2I-+5Cl2+4H2O=4SO +I2+8H++10Cl- +I2+8H++10Cl- |
C.当a≤b≤ a时,反应中转移电子的物质的量n(e-)为a mol≤n(e-)≤3a mol a时,反应中转移电子的物质的量n(e-)为a mol≤n(e-)≤3a mol |
D.当a<b< a时,溶液中SO a时,溶液中SO 、I-与Cl-的物质的量之比为a∶(3a-2b)∶2b 、I-与Cl-的物质的量之比为a∶(3a-2b)∶2b |
您最近一年使用:0次
2020-08-18更新
|
3378次组卷
|
7卷引用:黑龙江省哈尔滨师范大学附属中学2020-2021学年高二下学期期末考试化学试题
黑龙江省哈尔滨师范大学附属中学2020-2021学年高二下学期期末考试化学试题浙江省瑞安市上海新纪元高级中学2019-2020学年高一下学期期末考试化学试题(2)(已下线)解密04 离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密04 离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)课时06 与量有关的离子方程式书写-2022年高考化学一轮复习小题多维练(全国通用)辽宁省实验中学2021-2022学年高一上学期11月期中阶段测试化学试题福建省泉州市永春第一中学2022-2023学年高一上学期期末考试化学试题
名校
7 . 足量的铜与一定量的浓硝酸充分反应,得到4.48L(标准状况)NO2与NO的混合气体,这些气体与一定体积的O2混合后通入水中,恰好被完全吸收生成硝酸。向所得硝酸铜溶液中加入100mL4mol·L-1NaOH溶液,Cu2+恰好沉淀完全。下列说法正确的是
| A.此反应过程中转移了0.5mol的电子 |
| B.消耗氧气的体积为1.12L(标准状况) |
| C.参加反应的HNO3是0.45mol |
| D.混合气体中含2.24L(标准状况)NO |
您最近一年使用:0次
2020-07-22更新
|
2922次组卷
|
11卷引用:黑龙江省鹤岗市第一中学2021-2022学年高一下学期4月月考化学试题
黑龙江省鹤岗市第一中学2021-2022学年高一下学期4月月考化学试题辽宁省大连市旅顺口区2019-2020学年高一下学期期末考试化学试题辽宁省大连市2019-2020学年高一下学期期末考试化学试题重庆市缙云教育联盟2020-2021学年高一9月月考化学试题山西省实验中学2020-2021学年高一下学期第一次月考化学试题辽宁省大连市一0三中学2020-2021学年高一4月月考化学试题辽宁省部分中学2019-2020高一下学期期末考试化学试题云南省曲靖市第一中学2022-2023学年高一下学期期末考试化学试题安徽省铜陵市第一中学2022-2023 学年高一下学期期中教学质量检测化学试题云南省开远市第一中学校2022-2023学年高一下学期期末考试化学试题重庆市万州第二高级中学2023-2024学年高一下学期3月月考试题 化学试题
名校
8 . 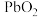 是褐色固体,受热分解为Pb的
是褐色固体,受热分解为Pb的 和
和 价的混合氧化物,
价的混合氧化物, 价的Pb能氧化浓盐酸生成
价的Pb能氧化浓盐酸生成 ,
, 价的Pb还原成
价的Pb还原成 价的Pb;现将
价的Pb;现将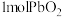 加热分解得到
加热分解得到 ,向剩余固体中加入足量的浓盐酸得到
,向剩余固体中加入足量的浓盐酸得到 ,
, 和
和 的物质的量之比为
的物质的量之比为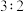 ,则剩余固体的组成及物质的量比是
,则剩余固体的组成及物质的量比是
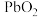 是褐色固体,受热分解为Pb的
是褐色固体,受热分解为Pb的 和
和 价的混合氧化物,
价的混合氧化物, 价的Pb能氧化浓盐酸生成
价的Pb能氧化浓盐酸生成 ,
, 价的Pb还原成
价的Pb还原成 价的Pb;现将
价的Pb;现将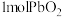 加热分解得到
加热分解得到 ,向剩余固体中加入足量的浓盐酸得到
,向剩余固体中加入足量的浓盐酸得到 ,
, 和
和 的物质的量之比为
的物质的量之比为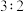 ,则剩余固体的组成及物质的量比是
,则剩余固体的组成及物质的量比是A. 混合的 混合的 、 、 | B.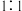 混合的 混合的 、PbO 、PbO |
C.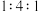 混合的 混合的 、 、 、PbO 、PbO | D.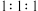 混合的 混合的 、 、 、PbO 、PbO |
您最近一年使用:0次
2020-02-06更新
|
1460次组卷
|
5卷引用:2016-2017学年黑龙江大庆实验中学高一12月月考化学卷
名校
解题方法
9 . 有关 反应的叙述正确的为
反应的叙述正确的为
 反应的叙述正确的为
反应的叙述正确的为| A.还原剂与氧化剂物质的量之比为5:3 |
| B.生成lmolO2,反应共转移4mol电子 |
C.若有5mol水做还原剂时,被BrF3还原的BrF3为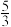 mol mol |
| D.若有5mol水参与反应时,被水还原的BrF3为2mol |
您最近一年使用:0次
2019-11-24更新
|
2646次组卷
|
7卷引用:黑龙江省鹤岗市第一中学2020届高三12月月考化学试题
名校
10 . 高锰酸钾是锰的重要化合物和常用的氧化剂。以下是工业上用软锰矿制备高锰酸钾的一种工艺流程:
(1) KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列_____ 物质相似。
A.75%酒精 B.双氧水 C.苯酚 D.“84”消毒液(NaClO溶液)
(2)操作Ⅰ的名称是________ ;操作Ⅱ是根据KMnO4和K2CO3两物质在__________ (填性质)上差异,采用 __________ (填操作步骤)、趁热过滤得到KMnO4粗晶体的。
(3)上述流程中可以循环使用的物质有石灰、CO2、____ 和____ (写化学式)。
(4) 向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是_______ 。
(5) 铋酸钠(NaBiO3,不溶于水)用于定性检验酸性溶液中Mn2+的存在(铋元素的还原产物为Bi3+,Mn的氧化产物为+7价),写出反应的离子方程式:__________________ 。
(6) 写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:________________ 。
(7)若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得_____ mol KMnO4。

(1) KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列
A.75%酒精 B.双氧水 C.苯酚 D.“84”消毒液(NaClO溶液)
(2)操作Ⅰ的名称是
(3)上述流程中可以循环使用的物质有石灰、CO2、
(4) 向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是
(5) 铋酸钠(NaBiO3,不溶于水)用于定性检验酸性溶液中Mn2+的存在(铋元素的还原产物为Bi3+,Mn的氧化产物为+7价),写出反应的离子方程式:
(6) 写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:
(7)若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得
您最近一年使用:0次
2019-09-24更新
|
1212次组卷
|
3卷引用:黑龙江省齐齐哈尔市第八中学2020届高三10月月考化学试题