1 . 在400°C,0.1MPa 以及Xe过量条件下,Xe和F2可以直接反应生成+2价态的化合物。反应的方程式是___________ 。所生成的氟化物与碘阴离子在常温下即可以反应,相应的反应式是___________ 。该反应说明氟化物具有(氧化性、还原性中选一项回答)___________ 。该氟化物溶于水,且缓慢地与水产生反应,反应式是___________ 。
您最近一年使用:0次
2 . 氧和硫是同族元素,因而其性质有相似性。完成下列化学反应: Na2S +CS2 =___________ ;Na2S +SnS2=___________
您最近一年使用:0次
3 . HN3(叠氮酸)是一种易爆炸的油状物,在水中稳定,是一种弱酸。分子中N的化合价是___________ ,HN3与KOH反应的方程式是___________ 。HN3受热时反应的方程式是___________ ,在水溶液中的电离方程式是___________ 。H3N的氧化性与HNO3相似,请完成下列方程式Cu +3HN3=___________ + N2 +NH3
您最近一年使用:0次
4 . 已知二元化合物A可以用次氯酸钠和过量的氨气制得,6.4gA完全燃烧得到4.48L的氮气(已折算成标准状况)。A可以与新制Cu(OH)2反应生成砖红色沉淀,同时生成密度为1.25g·L-1的无色无味的气体(已折算成标准状况)。请回答下列问题:
(1) A的化学式为___________ 。
(2)写出次氯酸钠与过量氨气反应生成A的化学方程式___________ 。
A的制备过程中氨气需要过量的理由是___________ 。
(3)写出A与新制Cu(OH)2反应的化学方程式___________ 。
(4)已知在一定条件下,A可与等物质的量H2O2恰好完全反应得到化合物B, B所含元素与A相同,其摩尔质量小于A,实验表明,B可能存在两种异构体。
①B的电子式为___________ 。
②写出B的两种可能异构体的结构式___________ 、___________ 。
(1) A的化学式为
(2)写出次氯酸钠与过量氨气反应生成A的化学方程式
A的制备过程中氨气需要过量的理由是
(3)写出A与新制Cu(OH)2反应的化学方程式
(4)已知在一定条件下,A可与等物质的量H2O2恰好完全反应得到化合物B, B所含元素与A相同,其摩尔质量小于A,实验表明,B可能存在两种异构体。
①B的电子式为
②写出B的两种可能异构体的结构式
您最近一年使用:0次
5 . 钯(Pd)是一种不活泼金属,性质与铂相似。含钯催化剂不仅在科研和工业生产中用途广泛,而且用量大,因此从废催化剂中回收钯具有巨大的经济效益。已知某废催化剂的主要成分是钯和活性炭,还含有少量铁、镁、铝、硅、铜等杂质元素,提取海绵钯的工艺流程如下:
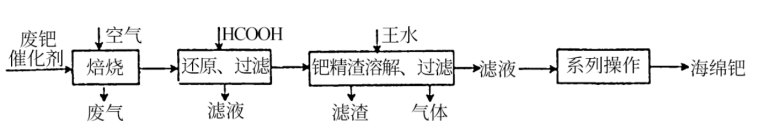
(1)Pd的价电子排布式为4d10,指出它在元素周期表中的位置_______ 。
(2)“焙烧”步骤中,通入的空气一定要足量,理由是_______ 。
(3)写出甲酸还原过程发生反应的化学方程式_______ 。
(4)钯在王水中溶解生成化合物X(由3种元素组成)、种无色有毒的气体Y和水。
①如何配置王水_______ 。
②写出钯与王水反应的化学方程式_______ 。
(5)金属钯具有显著的吸氢性能,其密度为12.0g·cm-3。
①在标准状况下,海绵钯吸收氢气的体积约为其体积的840倍,求海绵钯的吸附容量R=_______ (mL·g-1)、氢气的浓度r=_______ (1molPd吸收氢气的物质的量)。
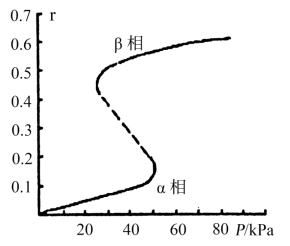
②金属钯中,氢气的r与压强之间的变化关系如图所示,试解释该图的变化趋势_______ 。
(相对原子质量:Pd106.4,理想气体常数R=8.314J·mol-l·K-1)

(1)Pd的价电子排布式为4d10,指出它在元素周期表中的位置
(2)“焙烧”步骤中,通入的空气一定要足量,理由是
(3)写出甲酸还原过程发生反应的化学方程式
(4)钯在王水中溶解生成化合物X(由3种元素组成)、种无色有毒的气体Y和水。
①如何配置王水
②写出钯与王水反应的化学方程式
(5)金属钯具有显著的吸氢性能,其密度为12.0g·cm-3。
①在标准状况下,海绵钯吸收氢气的体积约为其体积的840倍,求海绵钯的吸附容量R=
②金属钯中,氢气的r与压强之间的变化关系如图所示,试解释该图的变化趋势

(相对原子质量:Pd106.4,理想气体常数R=8.314J·mol-l·K-1)
您最近一年使用:0次
名校
6 . 氨硼烷(NH3BH3)是一种储氢量较高的储氢材料,室温下是一种无色分子晶体,可与水发生催化脱氢反应生成NH4BO2和H2.少量氨硼烷可以由硼烷(B2H6)和NH3合成。下列有关说法不正确的是
| A.元素N的第一电离能高于同周期相邻元素的第一电离能 |
| B.催化脱氢反应中,H2既是还原产物、又是氧化产物 |
| C.0.1 mol NH3BH3发生催化脱氢反应,可生成6.72L H2 (标准状况) |
| D.B2H6和NH3合成NH3BH3的反应为氧化还原反应,NH3 是还原剂 |
您最近一年使用:0次
7 . 现有CuO、MnO2、PbO2和Co2O3四种黑色或近黑色粉状固体,除蒸馏水外,仅用一种试剂判别之。请用表格形式写出判别步骤和现象、相应的化学反应方程式_______ 。
您最近一年使用:0次
8 . 某同学利用6种试剂中的4种进行实验[(a)0.1mol·L-1KI-淀粉溶液、(b)0.1mol·L-1KClO3溶液、(c)0.1mol·L-1KClO4溶液、(d)新制氯水、(e)稀硫酸、(f)1mol·L-1NaOH溶液]:向一支试管中按照一定顺序分别加入这些物质,且每种物质最多只加入一次,观察到的现象是:①无色→②无色→③蓝色→④无色→⑤蓝色。对该过程的下列分析中,正确的是
| A.试剂的加入顺序是:a→c→e→f→d |
B.②→③反应的离子方程式为:C1O +8I-+8H+=Cl-+4I2+4H2O +8I-+8H+=Cl-+4I2+4H2O |
| C.③蓝色→④无色,是因为加入NaOH溶液后,单质碘发生歧化反应 |
| D.④无色→⑤蓝色,一定是因为加入氯水后,将溶液中的I-氧化为单质碘 |
您最近一年使用:0次
9 . 科学家对络合氢化物的储氢特性进行了系列研究。
(1) LiA1H4在不同温度下分解放氢反应为:
当温度为160 ℃ - 180 ℃时,反应1: 3LiAIH6= Li3AlH6+2A1+3H2
当温度为180 ℃ -220 ℃时,反应2: Li3AlH6=3LiH+A1+3/2H2
上述两步反应总的放氢量是_______ (放氢量即为氢元素的质量占总质量的百分含量)。
(2)已知Mg(A1H4)2在400 ℃ 下分解,理论上放氢量为9.34%现取4.316gMg(AlH4)2在该温度下分解生成1.798g单质Al和一种金属互化物。写出该反应的化学方程式_______ 。
(1) LiA1H4在不同温度下分解放氢反应为:
当温度为160 ℃ - 180 ℃时,反应1: 3LiAIH6= Li3AlH6+2A1+3H2
当温度为180 ℃ -220 ℃时,反应2: Li3AlH6=3LiH+A1+3/2H2
上述两步反应总的放氢量是
(2)已知Mg(A1H4)2在400 ℃ 下分解,理论上放氢量为9.34%现取4.316gMg(AlH4)2在该温度下分解生成1.798g单质Al和一种金属互化物。写出该反应的化学方程式
您最近一年使用:0次
10 . 烟花爆竹常常在重大节日庆典中燃放。烟花的主要成分可以分成氧化剂、还原剂、发色剂、黏合剂等。
(1)爆竹的主要成分是黑火药,含有硝酸钾、硫黄和木炭。生成物中有一种单质,该单质分子的电子式是___________ 。
(2)用高氯酸钾代替硝酸钾,用糖类代替木炭和硫黄,可避免硫化钾、二氧化硫等有害物质的排放。请写出高氯酸钾(KClO4)与葡萄糖(C6H12O6)反应的化学方程式:___________ 。
(3)烟花中的发光剂,可用短周期金属的粉末,其燃烧时会发出白炽的强光。写出该金属的化学符号___________ 。
(4)烟花中还含有发色剂,利用焰色反应可使烟花放出五彩缤纷的色彩。焰色反应的原理是___________ 。
(1)爆竹的主要成分是黑火药,含有硝酸钾、硫黄和木炭。生成物中有一种单质,该单质分子的电子式是
(2)用高氯酸钾代替硝酸钾,用糖类代替木炭和硫黄,可避免硫化钾、二氧化硫等有害物质的排放。请写出高氯酸钾(KClO4)与葡萄糖(C6H12O6)反应的化学方程式:
(3)烟花中的发光剂,可用短周期金属的粉末,其燃烧时会发出白炽的强光。写出该金属的化学符号
(4)烟花中还含有发色剂,利用焰色反应可使烟花放出五彩缤纷的色彩。焰色反应的原理是
您最近一年使用:0次



