1 . 书写方程式
(1)硫酸铝和硅酸钠溶液反应的离子方程式_______ 。
(2)酚醛树脂的合成_______ 。
(3)用重铬酸钾和浓盐酸制氯气_______ 。
(4) 和
和 固体混合物在高温下发生反应,放出的气体均为黄绿色(
固体混合物在高温下发生反应,放出的气体均为黄绿色( 为黄绿色)
为黄绿色)_______ 。
(5) 将雌黄铁矿(
将雌黄铁矿(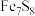 )中的S氧化成
)中的S氧化成
_______ 。
(1)硫酸铝和硅酸钠溶液反应的离子方程式
(2)酚醛树脂的合成
(3)用重铬酸钾和浓盐酸制氯气
(4)
 和
和 固体混合物在高温下发生反应,放出的气体均为黄绿色(
固体混合物在高温下发生反应,放出的气体均为黄绿色( 为黄绿色)
为黄绿色)(5)
 将雌黄铁矿(
将雌黄铁矿(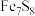 )中的S氧化成
)中的S氧化成
您最近一年使用:0次
名校
2 . 现有 的
的 ,将其加热并发生反应,并检测放出的气体1的质量,后向剩余固体a中加入足量的浓盐酸,并检测放出的气体2的质量。(已知,+4价的
,将其加热并发生反应,并检测放出的气体1的质量,后向剩余固体a中加入足量的浓盐酸,并检测放出的气体2的质量。(已知,+4价的 能和浓盐酸反应放出
能和浓盐酸反应放出 。
。 受热可分解为
受热可分解为 的+4、+2价的混合氧化物并放出
的+4、+2价的混合氧化物并放出 )。则下列说法中正确的是
)。则下列说法中正确的是
 的
的 ,将其加热并发生反应,并检测放出的气体1的质量,后向剩余固体a中加入足量的浓盐酸,并检测放出的气体2的质量。(已知,+4价的
,将其加热并发生反应,并检测放出的气体1的质量,后向剩余固体a中加入足量的浓盐酸,并检测放出的气体2的质量。(已知,+4价的 能和浓盐酸反应放出
能和浓盐酸反应放出 。
。 受热可分解为
受热可分解为 的+4、+2价的混合氧化物并放出
的+4、+2价的混合氧化物并放出 )。则下列说法中正确的是
)。则下列说法中正确的是A.气体1的物质的量最多为 |
B.若物质的量,气体 气体 气体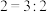 ,则固体的成分为物质的量之比可能为 ,则固体的成分为物质的量之比可能为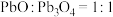 |
C.若物质的量,气体 气体 气体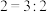 ,则固体a的成分为物质的量之比可能为 ,则固体a的成分为物质的量之比可能为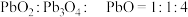 |
D.气体总物质的量可能为 |
您最近一年使用:0次
2022-08-17更新
|
480次组卷
|
2卷引用:2022年山东省第三届学科素养知识竞赛(高中组)化学试题
3 . 根据要求回答下列问题:
(1)拟除掉BaCl2溶液中的少量FeCl3杂质,加入Ba(OH)2或BaCO3,选用哪种试剂更好_______ 。
(2)AlCl3溶液和Na2S溶液混合产生白色沉淀和有刺激性气味的气体,该气体产物是_______ 。
(3)将CO通入到PdCl2溶液中,观察到有黑色沉淀(Pd) 生成,则氧化剂与还原剂的物质的量之比是_______ 。
(4)向硫化钠和碳酸钠混合溶液中通入SO2可制备硫代硫酸钠,写出反应的化学方程式_______ 。
(5)新型自来水消毒剂ClO2可由KClO3在H2SO4存在下与甲醇反应制备,反应产生两种气体,写出反应的化学方程式_______ 。
(1)拟除掉BaCl2溶液中的少量FeCl3杂质,加入Ba(OH)2或BaCO3,选用哪种试剂更好
(2)AlCl3溶液和Na2S溶液混合产生白色沉淀和有刺激性气味的气体,该气体产物是
(3)将CO通入到PdCl2溶液中,观察到有黑色沉淀(Pd) 生成,则氧化剂与还原剂的物质的量之比是
(4)向硫化钠和碳酸钠混合溶液中通入SO2可制备硫代硫酸钠,写出反应的化学方程式
(5)新型自来水消毒剂ClO2可由KClO3在H2SO4存在下与甲醇反应制备,反应产生两种气体,写出反应的化学方程式
您最近一年使用:0次
名校
4 . 碘及其化合物广泛用于医药、染料等方面。I2的一种制备方法如图所示:

下列说法正确的是

下列说法正确的是
| A.加入铁粉转化的离子方程式为Fe+ 2Ag+=Fe2++ 2Ag |
| B.滤渣用过量硝酸溶解除铁可以回收单质银 |
| C.当n(Cl2):n(FeI2)<3:2时,氧化产物只有I2 |
| D.若通入过量Cl2,则单质碘的收率会降低 |
您最近一年使用:0次
2022-06-11更新
|
345次组卷
|
2卷引用:重庆市2021-2022学年高二下学期5月化学竞赛试题
名校
解题方法
5 . 向mg由铁粉和铜粉组成的混合物中,加入某浓度的稀硝酸,充分反应后测得生成NO的体积[V(NO)](已换算成标准状况下)、m(固体剩余质量)随加入的稀硝酸的体积的变化如图所示(设硝酸的还原产物只有NO)。下列说法中正确的是
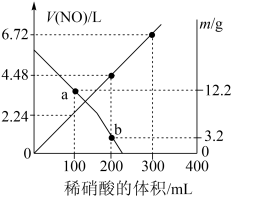

| A.稀硝酸的浓度为0.4mol·L-1 |
| B.a点时,100mL稀硝酸中溶解了Fe和Cu共8.4g |
| C.b点对应的溶液中可能含有的金属阳离子为Fe2+、Fe3+、Cu2+ |
| D.加入稀硝酸至400mL时,收集到的V(NO)约为6.91L |
您最近一年使用:0次
2022-05-03更新
|
3626次组卷
|
14卷引用:湖北省华中师范大学第一附属中学2022-2023学年高一上学期竞赛生10月测试化学试题
湖北省华中师范大学第一附属中学2022-2023学年高一上学期竞赛生10月测试化学试题湖北省黄冈市部分重点中学2021-2022学年高一下学期4月期中联考化学试题辽宁省县级重点高中协作体2021-2022学年高一下学期期中考试化学试题江西省重点2021-2022学年高一下学期5月联考化学试题湖南省衡阳市部分校2021-2022学年高一下学期期末考试化学试题山西省长治市2021-2022学年高一下学期期末联合考化学试题(已下线)微专题23 金属与硝酸反应的规律与计算-备战2023年高考化学一轮复习考点微专题(已下线)第13练 氮及其化合物-2023年高考化学一轮复习小题多维练(全国通用)辽宁省沈阳实验中学2022-2023学年高二上学期开学考试化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高一下学期第一次验收考试化学试题江西省上饶市民校考试联盟2022—2023学年高一下学期阶段测试(四)化学试题新疆维吾尔自治区和田地区策勒县2022-2023学年高三上学期11月期中考试化学试题山东新高考2022-2023学年高一上学期质量测评模拟演练化学试题 四川省泸州市泸县第一中学2023-2024学年高一上学期1月期末化学试题
名校
6 . 水体中氨氮含量会造成水体富营养化,用次氯酸钠除去氨氮的原理如图所示。下列说法错误的是


| A.去除过程中,每一步反应都是氧化还原反应 |
B.每除去1mol ,转移3mol电子 ,转移3mol电子 |
| C.该过程需控制温度,温度过高时氨氮去除率会降低 |
D.去除过程的总反应方程式为: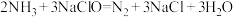 |
您最近一年使用:0次
2022-01-16更新
|
901次组卷
|
8卷引用:甘肃省天水市2023-2024学年高一上学期10月份化学竞赛试卷
甘肃省天水市2023-2024学年高一上学期10月份化学竞赛试卷 湖北省黄冈市2021-2022学年高一上学期期末调研考试化学试题湖北省荆州中学2021-2022学年高一上学期期末考试化学试题(已下线)微专题20 新型含氯化合物的制备与性质探究(ClO2、NOCl等)-备战2023年高考化学一轮复习考点微专题内蒙古鄂尔多斯市第一中学2022-2023 学年高一上学期期末考试化学试题湖北省黄冈市2022-2023学年高一上学期期末调研考试化学试题湖北省十堰市部分重点中学2022-2023学年高一下学期3月联考化学试题四川省南充高级中学2021-2022学年高一下学期开学考试化学试题
名校
解题方法
7 . X、Y、Z、M为短周期元素,原子序数依次增大。A~J均由该四种元素构成的单质或化合物,其转化关系如图所示,部分生成物省略。
已知:①A、B、C、G都是由两种元素构成的化合物,其中A、G分子所含的电子数为10e-,B、C分子所含的电子数为18e-;D为空气的主要成分之一、
②另取16.8gJ在真空条件下,控制温度350~400oC加热至完全分解,得到F和8.96L(已折算成标准状况)A两种物质。

请回答下列问题:
(1)写出C的化学式是___________ ;D的电子式是___________ 。
(2)请写出金属单质E在生产生活中的一种作用___________ 。
(3)写出次氯酸钠与过量气体A反应生成B的化学方程式是___________ ;B在制备过程中,气体A需要过量的理由是___________ 。
(4)写出F和G反应生成H和A的化学方程式是___________ 。
(5)B在加热条件下与CuO反应可生成气体D和金属单质,请设计实验方案,验证B与CuO反应后固体的成分(不考虑其他反应)___________ 。
(6)写出J在已知②条件下受热分解的化学方程式是___________ 。
已知:①A、B、C、G都是由两种元素构成的化合物,其中A、G分子所含的电子数为10e-,B、C分子所含的电子数为18e-;D为空气的主要成分之一、
②另取16.8gJ在真空条件下,控制温度350~400oC加热至完全分解,得到F和8.96L(已折算成标准状况)A两种物质。

请回答下列问题:
(1)写出C的化学式是
(2)请写出金属单质E在生产生活中的一种作用
(3)写出次氯酸钠与过量气体A反应生成B的化学方程式是
(4)写出F和G反应生成H和A的化学方程式是
(5)B在加热条件下与CuO反应可生成气体D和金属单质,请设计实验方案,验证B与CuO反应后固体的成分(不考虑其他反应)
(6)写出J在已知②条件下受热分解的化学方程式是
您最近一年使用:0次
2021-11-05更新
|
1091次组卷
|
2卷引用:湖北省华中师范大学第一附属中学2022-2023学年高一上学期竞赛生10月测试化学试题
解题方法
8 . SO2和S混合物经低压放电得产物A,它在液态空气冷阱中成橘红色液体。A受热生成等物质的量的S和SO2。写出以下两个反应的方程式。
(1)和微量 H2O反应得H2S、S、SO2 (已知有1/5mol的A转化为 S)_______ 。
(2)和金属 M反应生成金属硫化物(设为MS)_______ 。
(1)和微量 H2O反应得H2S、S、SO2 (已知有1/5mol的A转化为 S)
(2)和金属 M反应生成金属硫化物(设为MS)
您最近一年使用:0次
解题方法
9 . 金属钛无毒、密度小而强度高,广泛用于航天材料、人造骨骼的制造等,有航天金属和生命金属的美誉。
(1)A为+ 4价钛的卤化物,A在潮湿的空气中因水解而冒白烟。向硝酸银-硝酸溶液中滴入A,有白色沉淀B生成,B易溶于氨水。取少量锌粉投入A的盐酸溶液中,可得到含TiCl3的紫色溶液C。将C溶液与适量氯化铜溶液混合有白色沉淀D生成,混合溶液褪为无色。
①B的化学式为:_______ ;B溶于氨水所得产物为:_______ ;
②A水解的化学反应方程式为:_______ ,理论计算可知,该反应的平衡常数很大,增加HCl浓度不足以抑制反应的进行,可是在浓盐酸中,A却几乎不水解,原因是:_______ ;
③C溶液与适量氯化铜溶液反应的化学方程式为:_______
(2)已知钛的元素电势图(E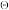 /V)为:
/V)为:
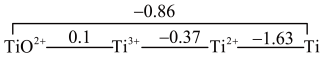
则:Ti2+_______ (填“能”或“不能”)在水溶液中稳定存在;Ti溶于热浓盐酸的化学反应方程式为_______ 。
(1)A为+ 4价钛的卤化物,A在潮湿的空气中因水解而冒白烟。向硝酸银-硝酸溶液中滴入A,有白色沉淀B生成,B易溶于氨水。取少量锌粉投入A的盐酸溶液中,可得到含TiCl3的紫色溶液C。将C溶液与适量氯化铜溶液混合有白色沉淀D生成,混合溶液褪为无色。
①B的化学式为:
②A水解的化学反应方程式为:
③C溶液与适量氯化铜溶液反应的化学方程式为:
(2)已知钛的元素电势图(E
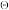 /V)为:
/V)为: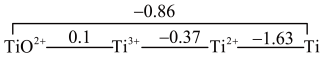
则:Ti2+
您最近一年使用:0次
10 . 若以I2(l)为溶剂,下列四个反应中何者为歧化、反歧化、溶剂合、复分解:
(1)KI+IBr=KBr+I2_______
(2)NaCN+I2=NaI+ICN_______
(3)KI+I2=KI3_______
(4)PbC12+2KI=PbI2+2KCl_______
(1)KI+IBr=KBr+I2
(2)NaCN+I2=NaI+ICN
(3)KI+I2=KI3
(4)PbC12+2KI=PbI2+2KCl
您最近一年使用:0次



